高考化学试题
常温下,将 1molCaC2O4 粉末置于盛有500mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3 固体的过程中,溶液中Ca2+ 和 CO32-的浓度变化曲线如图所示,下列说法中不正确的是
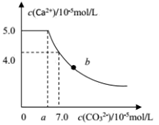
A. a=5.6
B. 常温下,Ksp(CaC2O4)>Ksp(CaCO3)
C. b 点对应的溶液中,离子浓度关系为c(C2O42-) <c(CO32-)
D. 若使 1molCaC2O4 全部转化为 CaCO3,至少要加入 2.12molNa2CO3
A. CO2(CO)——通入氧气中,点燃
B. C12( HCl)——通入足量饱和食盐水中,再干燥
C. FeCl2溶液(FeC13)——加入过量铜粉,再过滤
D. NaHCO3溶液(Na2CO3)——加入适量氯化钙溶液,再过滤
A. 锌 B. 碳 C. 氯化钠 D. 硫化钠
依据下列实验现象,得出的结论正确的是
| 操作 | 实验现象 | 结论 | |
| A | 向NaBr 溶液中加入过量氯水,再加入淀粉 KI 溶液 | 最终溶液变蓝 | 氧化性:Cl2>Br2>I2 |
| B | 向某无色溶液中滴加浓盐酸 | 产生能使品红溶液褪色的气体 | 不能证明原溶液中含有SO32-或HSO3- |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后, 加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
| D | 向2mL 0.01mol/L的AgNO3溶液中滴加几滴同浓度的NaCl溶液后,滴加 KI 溶液 | 先产生白色沉淀,后出现黄色沉淀 | 证明Ksp(AgI)<Ksp(AgCl) |
A. A B. B C. C D. D

A. 甲池中得到H2O2的反应,H2O2既是氧化产物也是还原产物
B. 电路中每转移0.2mol电子,甲池溶液质量变化3.4g,乙池溶液质量保持不变
C. 光照时乙池电极上发生的反应为:H2S+I3-=3I-+S+2H+
D. 甲池中炭棒上发生的电极反应为:AQ+2H+-2e-=H2AQ
A. 该原电池是实现电能转化为化学能的装置
B. 该原电池在工作时,Zn2+ 向铜片附近迁移
C. 该原电池的正极是铜,发生氧化反应
D. 该原电池的电子从铜出发通过外电路流向锌

A. 曲线Ⅱ表示lg
B. a~b的过程中,水的电离程度逐渐增大
C. 当c(H2CO3) ═c (HCO3—)时,c(HPO42—)=c(H2PO4—)
D. 当pH增大时,

A. 二甲胺溶液的浓度为0.2mol·L-1
B. 在Y和Z点之间某点溶液pH=7
C. Y点存在:c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-)
D. 常温下,(CH3)2NH2Cl水解常数Kh≈5.0×10-11
首先用废铝渣制取AI(OH)3固体,流程如下:
(1)调节pH用_________试剂为好。某同学在减压过滤时,布氏漏斗内没有得到产品,可能原因是______________________。
然后将氢氧化铝和甲醛依次加入到质量分数为50%的过氧化氢溶液中(投料物质的量之比依次为1∶3∶2),装置如图1.最终可得到含甲酸铝90%以上的优质产品。反应式为:2Al(OH)3+6HCHO+3H2O2=2Al(HCOO)3+6H2O+3H2↑。

(2)反应过程可看作两步进行,第一步______________(写出化学方程式),第二步为甲酸与Al(OH)3 反应生成甲酸铝。
(3)反应温度最好控制在30—70℃之间,温度不宜过高,主要原因是_________________。
(4)实验时需强力搅拌45 min,最后将溶液____________,抽滤,洗涤,干燥得产品。可用酸性KmnO4标准溶液滴定法来测定产品纯度,滴定起始和终点的滴定管液面位置见上图2, 则消耗的酸性KmnO4标准溶液体积为__________________mL。
如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中 W 、 X 、 Y 、 Z 为原子序数依次增大的短周期元素, X 和 Z 同主族, Y 原子序数为 W 原子价电子数的 3 倍。下列说法正确的是

A . X 和 Z 的最高化合价均为 +7 价
B . HX 和 HZ 在水中均为强酸,电子式可表示为 ![]() 与
与 ![]()
C . 四种元素中, Y 原子半径最大, X 原子半径最小
D . Z 、 W 和氢三种元素可形成同时含有离子键和共价键的化合物
A. 加热
 B. 分液
B. 分液
C. 过滤
 D. 蒸馏
D. 蒸馏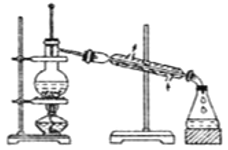
工业上用低品铜矿(主要含CuS、FeO等)制备氯化亚铜(CuCl)的一种工艺流程如图:

已知:①CuCl微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化。
②“氧化”时,NO![]() 中N元素主要被还原为最低价态,少部分被还原为NO。
中N元素主要被还原为最低价态,少部分被还原为NO。
(1)①“氧化”阶段的温度需控制在65℃,其适宜的加热方式为____;
②该步骤中FeO被NH4NO3氧化,其主要反应的离子方程式:____。
(2)在实验室进行实验时,“氧化”阶段反应可在如图所示装置中进行:

①实验开始时,温度计显示反应液温度低于室温,主要原因是____。
②通入氧气的目的是____。
③为便于观察和控制产生O2的速率,制备氧气的装置最好选用_______(填字母)。

(3)已知常温下CuCl在水溶液中Ksp=1.2×10-6,工艺流程最后一步析出CuCl晶体后的溶液中,如果c(Cl-)=4.0mol·L-1,则c(Cu+)=____。
(4)已知pH对CuCl沉淀率的影响如图所示,请设计从“过滤II”所得的滤液中获取CuCl的实验方案:____。(实验中必须使用的试剂有:NaCl溶液、Na2SO3溶液、NaOH溶液、95%乙醇)。

A. 组成为C6H14的烷烃中仅能由1种单炔烃加氢而制得的结构有2种
B. 立方烷(
C.
D. 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
A. 用过氧化氢溶液制取氧气时,加少量MnO2以加快反应速率
B. 用标准HCl溶液滴定 NaHCO3溶液来测定其浓度,选择甲基橙为指示剂
C. 用铂丝蘸取某碱金属的化合物溶液灼烧,火焰呈黄色,证明该化合物是钠盐
D. 给试管里的液体加热,液体体积一般不超过试管容积的三分之一
(1)用CH4催化还原氮氧化物,已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1= a kJ/mol,欲计算反应CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(1)的焓变△H2,则还需要查找某化合反应的焓变△H3,该化合反应中各物质化学计量数之比为最简整数比时△H3=bkJ/mol,则该化合反应的热化学方程式为____________________。据此计算出△H2=__________kJ/mol(用含a和b的式子表示)。
(2)汽车尾气转化的反应之一:2NO(g)+2CO(g)
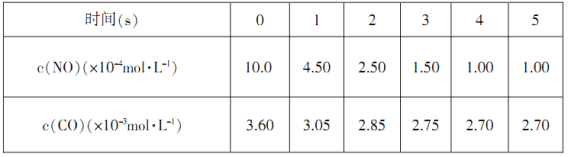
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率υ(N2)=______________________________。
②在该温度下,反应的平衡常数K=___________(只写出计算结果)。
③对于该可逆反应,通过综合分析以上信息,至少可以说明___________(填字母)。
A.该反应的反应物混合后很不稳定
B.在催化剂的作用下,该反应一旦发生将在较短的时间内完成
C.该反应体系达到平衡时至少有一种反应物的百分含量较小
D.该反应在一定条件下能自发进行
E.该反应使用催化剂意义不大
(3)通过调节溶液pH,在弱碱性条件下,用漂白粉溶液可将废水中的CN-转化为碳酸盐和N2而除去。写出该反应的离子方程式为______________________。
(4)废水中的重金属离子通常用沉淀法除去。已知Ksp(NiS)=1.1×10-21,Ksp(CuS)=1.3×10-36,国家规定的排放标淮:镍低于1.1×10-5mol·L-1,铜低于7.8×10-5mol·L-l。则需要控制溶液中S2-的浓度不低于__mol·L-1。
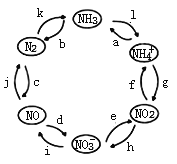
(1)氮分子的电子式为______________________。
(2)图中属于“氮的固定”的是___________(填字母)。
(3)已知NH4Cl溶液呈酸性,用离子方程式解释原因___________________________________________ 。
(4)用离子方程式举一例表示循环中发生非氧化还原反应的过程__________________。
(5)若反应h是在NO2与H2O的作用下实现,则该反应中氧化剂与还原剂物质的量之比为____________。
(6)若反应i是在酸性条件下由NO3—与Fe2+的作用实现,则该反应的离子方程式为_______________。
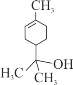
A. 该有机物催化加氢后的产物分子式为C10H18O
B. 该有机物发生消去反应可得到3种产物
C. 1 mol该有机物能与1 mol NaOH反应
D. 该有机物中碳原子上的氢原子的一氯代物的同分异构体有7种 (不考虑立体异构)
A. 酸性:HI>HF B. 碱性:NaOH>Mg(OH)2
C. 稳定性:CH4>H2S D. 氧化性:FeCl3> CuCl2
A. 0.6mol过氧化钠晶体中所含阴离子的数目为1.2NA
B. 46g NO2和N2O4的混合物中含有氧原子的数目为2NA
C. 11.2LCl2与足量NaOH溶液反应时转移的电子数为0.5NA
D. 电解法精炼铜时,阳极溶解32g,转移电子数一定为NA
(1)已知:2NO2(g)= N2O4(g) △H=-55.3kJ/mol
N2O5(g)=2NO2(g)+
则:N2O5(g)=N2O4(g)+
(2)以乙烯(C2H4)作为还原剂脱硝(NO),脱硝机理如图1。若反应中n(NO)︰n(O2)=2︰1,则总反应的化学方程式为___________;脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2,为达到最佳脱硝效果,应采用的条件是___________。

(3)T1温度时在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g)
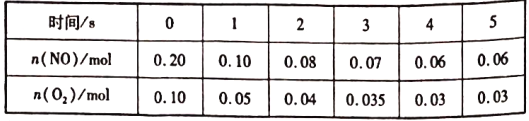
①从0~2s内该反应的平均速率υ(NO)=___________mol/(L·s)。
②T1温度时化学平衡常数K=___________ L/mol。 (结果保留3位有效数字)。
③化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T2___________T1(填“>”、“<”或“=")。
④已知2NO(g)+O2(g)
第一步NO+NO
下列叙述正确的是___________(填标号)。
A. υ(第一步的正反应)< υ(第二步的反应) B.总反应快慢由第二步决定
C.第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
- 两年前的9月15日,雷曼倒闭,金融危机风暴席卷全球。如多米诺骨牌,一张倒下,满盘崩溃。危机仅限于美国吗?绝非如此美国经济
- 常温下,在下列溶液中发生如下反应: ①16H++10Z-+2XO===2X2++5Z2+8H2O ②2A2++B2===
- ________one scientist has pointed out, children’s skulls are
- 某校高二年级共有六个班,现从外地转入4名学生,要安排到该年级的两个班级且每班安排2名,则不同的安排方案种数为
- 如图,导热性能极好的气缸,高为L = 1 m,开口向上固定在水平面上,气缸中有横截面积为S = 100 cm2、质量为m
- 碳化硅(SiC)陶瓷基复合材料是一种新型热结构材料.在空气中,碳化硅能与熔融的氢氧化钠发生反应:SiC+2NaOH+2O
- 下列句子中有错别字的一句是( ) A.唐代诗人王维有意将自己一生的悔恼痛苦,消除泯灭于佛教这个精神王国和幽寂净静的山林自
- 已知cos(+)=-,且是第四象限角,计算: (1)sin(2-); (2) (n∈Z).
- 请为下面的新闻拟写标题,并对“给力”登上《人民日报》头版头条这一事件作简要点评。(5分) 11月10日,《人民日报》头版
- 分解因式:=
- ——We need to ____the time to have a meeting now. ——What a
- 对绿色植物在生物圈中的作用的叙述,不合理的是( ) A.能够增加大气湿度,促进降雨 B.
- (07天津卷)(32分)君与民的关系曾在中外政治发展中不断探索,阅读下列图文材料,回答问题。材料一: 孟子认为君权的获得
- 如图所示,内壁光滑的空心细管弯成的轨道ABCD固定在竖直平面内,其中BCD段是半径R=0.25m的圆弧,C为轨道的最低点
- —I _______ to your birthday party last Sunday.—Unfortunately
- 使中国出现了第一批近代企业,为中国的近代化开辟了道路的运动是() A.洋务运动 B.戊戌变法
- 2014年9月30日,经中国人民银行授权,中国外汇交易中心宣布在银行间外汇市场开展人民币对欧元直接交易。在遵循市场原则的
- .The Gate of Fortune, from ____top visitors can enjoy a wond
- 关于能源和能源的利用,下列说法正确的是( ) A.因为能量是守恒的,所以不存在能源危机 B.太阳能无法被人类直接利用
- 工业上如何以铝土矿(主要成分为Al2O3,还含有少量的Fe2O3)为原料制取铝,请写出有关反应的化学方程式。



