高考化学试题
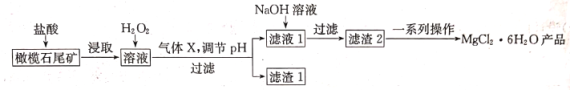
已知几种金属阳离子形成氢氧化物沉淀时的pH如下表
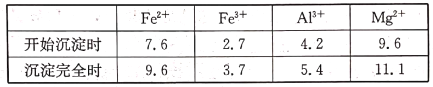
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有______________________(任写两种)。
(2)气体X的电子式为___________,滤渣1经过处理可以制得一种高效的无机高分子混凝剂、净水剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________。
(3)加入H2O2的目的是___________;若将上述过程中的“H2O2”用“ NaClO”代替也能达到同样目的,则发生反应的离子方程式为_________________________________。
(4)“一系列操作”主要包括加入足量盐酸,然后经过______________________、过滤、洗涤,即得到氯化镁晶体。
(5)准确称取2.000g氯化镁晶体产品于250mL锥形瓶中,加水50mL使其完全溶解,加入100mL氨性缓冲液和少量铬黑T指示剂,溶液显酒红色,在不断震荡下,用0.5000mol·L-1的EDTA标准溶液进行滴定,其反应原理为Mg2++Y4-=MgY2-,滴定终点时消耗EDTA标准溶液的体积19.00mL。
①则产品中MgCl2·6H2O的质量分数为___________(结果保留3位有效数字)。
②下列滴定操作会导致测量结果偏高的是___________(填宇母)。
a.锥形瓶洗涤后没有干燥 b.滴定时锥形瓶中有液体溅出
c滴定终点时俯视读数 d滴定管滴定前有气泡,滴定后气泡消失
选项 | 实验操作和现象 | 实验结论 |
A | 将SO2通入紫色石蕊试液中,溶液变红 | SO2与水反应生成H2SO3造成溶液显酸性 |
B | 向久置的Na2SO3溶液中加入足量Ba(NO3)2溶液,出现白色沉淀,再加入足量稀盐酸,部分沉淀溶解 | 部分Na2SO3被氧化 |
C | 向20%蔗糖溶液中加入少量稀H2SO4,加热,再加入银氨溶液,未出现银镜 | 蔗糖未水解 |
D | 向某黄色溶液中加入淀粉 KI 溶液,溶液呈蓝色 | 溶液中含 Br2 |
A. A B. B C. C D. D
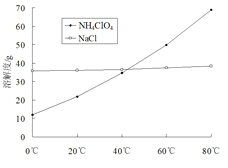
A. NH4ClO4分解后产生的气体通入紫色石蕊溶液中,溶液变红色
B. NH4ClO4分解后产生的气体通过足量NaOH溶液,再通过足量灼烧的铜网,可得到纯净的单质气体
C. NH4ClO4与NaCl的混合溶液分离时,应采取蒸发浓缩,冷却结晶,过滤,得到NH4ClO4固体粗产品
D. 在NH4ClO4固体粗产品中加入NaOH浓溶液,加热,收集所得NH3体积,可计算粗产品纯度
A.
C.
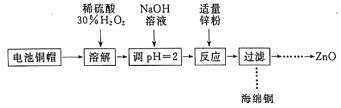
A. “溶解”操作中溶液温度不宜过高
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的氧气或H2O2
C. 与锌粉反应的离子可能为Cu2+、H+
D. “过滤”操作后,将滤液蒸发结晶、过滤、洗涤、干燥后,高温灼烧即可得纯净的ZnO
已知:①二茂铁熔点是173℃,在100℃时开始升华;沸点是249℃。
②制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O
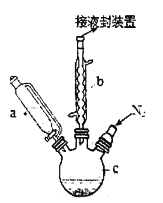
实验步骤为:
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到 烧瓶中,充分搅拌,同时通氮气约l0min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(C5H6质量为5.225g),搅拌;
③将足量的无水FeCl2(CH3)2SO(二甲亚砜,作溶剂〕配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是______________。
(2)步骤①中通入氮气的目的是______________。
(3)步骤⑤用盐酸洗涤的目的是______________。
(4)步骤⑦是二茂铁粗产品的提纯,该过程在下图中进行,其操作名称为_____________;该操作中棉花的作用是______________。
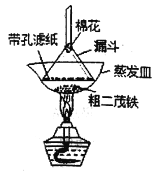
(5)为了确认得到的是二茂铁,还需要进行的一项简单实验是_____________________;若最终制得纯净的二茂铁4.3g,则该实验的产率为_____________(保留三位有效数字)。
以A、B、C为原料制取药物AspirinSustained-ReleaseTablets(缓释阿司匹林)的合成路线如图:

已知:ⅰ.A、B为烃,其中A的产量可作为石油化工水平的标志;
ⅱ. 。
。
回答下列问题:
(1)Z所含官能团名称为___。
(2)B和Y的结构简式为__、__。
(3)完成方程式:
①X→CH2OHCH2OH__。
②C→ __。
__。
(4)满足以下条件的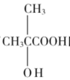 的同分异构体共有__种(不含立体异构),其中核磁共振氢谱峰面积比为6:1:1的同分异构体的结构简式为__。
的同分异构体共有__种(不含立体异构),其中核磁共振氢谱峰面积比为6:1:1的同分异构体的结构简式为__。
a.能发生水解反应 b.能与钠反应放出氢气 c.能发生银镜反应
(5)以乳酸(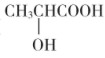 )和甲醇为原料,其他无机试剂任选,设计合成
)和甲醇为原料,其他无机试剂任选,设计合成 的路线:__。
的路线:__。
有科学研究提出 : 锂电池负极材料 (Li) 由于生成 LH 而不利于电池容量的保持。一定温度下,利用足量重水 (D 2 O )与含 LiH 的 Li 负极材料反应,通过测定 n(D 2 )/n(HD) 可以获知 n(Li)/n(LiH) 。
已知: ①LiH+H 2 O=LiOH+H 2 ↑
②2Li(s)+H 2 ⇌2LiH △H < 0
下列说法不正确的是
A . 可用质谱区分 D 2 和 HD
B . Li 与 D 2 O 的反应: 2Li+2D 2 O=2LiOD+D 2 ↑
C . 若 n(Li)/n(LiH) 越大,则 n(D 2 )/n(HD) 越小
D . 80℃ 反应所得 n(D 2 )/n(HD) 比 25℃ 反应所得 n(D 2 )/n(HD) 大
A. 中子数 B. 质量数 C. 核外电子数 D. 质子数

A.容器内压强不变,表明反应达到平衡
B.
C.平衡时A的体积分数
D.平衡常数K:
A | B | C | D |
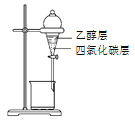
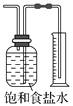
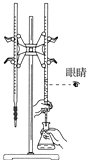
用CCl4提取溶在乙醇中的I2 | 测量Cl2的体积 | 过滤 | 用NaOH标准溶液滴定锥形瓶中的盐酸 |
|
|
|
|
A. A B. B C. C D. D

回答下列问题:
(1)I中含氧官能团的名称为___________________。
(2)由B生成C的化学方程式为_______________________________。
(3)由E和F反应生成D的反应类型为_______,由G和H反应生成I的反应类型为______。
(4)仅以D为单体合成高分子化合物的化学方程式为_________________ 。
(5)X是I的同分异构体,能发生银镜反应,能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1。写出两种符合要求的X的结构简式_________________ 。
(6)参照本题信息,试写出以1-丁烯为原料制取
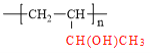 的合成路线流程图(无机原料任选)__________ 。
的合成路线流程图(无机原料任选)__________ 。合成路线流程图示例如下:

已知:H3AsO3为弱酸,热稳定性差。
(1)写出一条“碱浸”时提高浸取率的方法____;“碱浸”中H3AsO3转化成Na3AsO3的离子方程式为____。
(2)“氧化”时常在向混合液中通入O2时对体系加压,目的是____。
(3)“沉砷”过程中有如下反应:
①
②
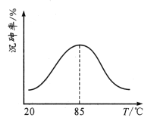
沉砷率与温度关系如图。沉砷最佳温度为____,高于85℃时,沉砷率下降的原因是____。
(4)“还原”过程中获得H3 AsO3的化学反应方程式为____;“操作A”为:____、过滤;滤液Ⅱ的主要成分是____。
(5)若每步均完全反应,“氧化’’和“还原”时消耗相同条件下O2和SO2体积分别为xL、yL,则废水中n(H3AsO3):n(H3AsO4)=____(写出含x、y的计算式)。
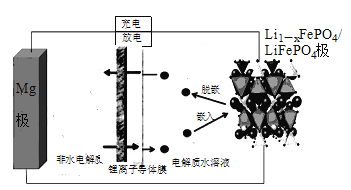
下列说法正确的是
A. 放电时,Li+被还原
B. 充电时,电能转变为化学能
C. 放电时,电路中每流过2mol电子,有1molMg2+迁移至正极区
D. 充电时,阳极上发生的电极反应为LiFePO4-xe-= Li1-xFePO4 + xLi+
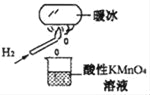
A. 20℃时,水凝固形成的“暖冰”所发生的变化是化学变化
B. “暖冰”是水置于足够强的电场中形成的混合物
C. 烧杯中液体为FeCl3溶液时,产生的气体为Cl2
D. 该条件下H2燃烧的产物中可能含有一定量的H2O2
A. 钛被称为继铁、铝之后的第三金属,但目前主要用于尖端领域,是因为其制备或冶炼的成本远高于铁或铝
B. 配制一定物质的量浓度的溶液时,固体溶解后未冷却就立即转移到容量瓶中定容,会使所配溶液浓度偏大
C. 用酒精灯加热铝箔可使铝箔熔化,但熔化的铝并不滴落,是因为构成铝表面薄膜的氧化铝的熔点高于铝的熔点
D. 胶体粒子的直径大于可见光的波长,能使光波发生散射
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1mol氢氧根离子中含有的电子数为9NA
B.将1molN2与足量H2充分反应,生成NH3的分子数为2NA
C.标准状况下,2.24L乙烯中含有C-H键的数目为0.4NA
D.常温下,1L 0.2mol/LAlCl3溶液中含Al3+数为0.2NA
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 提高CO2充气压力,饮料中c(A–)不变
C. 当pH为5.0时,饮料中
D. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(
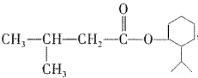 ,下列有关X的说法错误的是
,下列有关X的说法错误的是A. X可能有香味,是乙酸乙酯的同系物
B. X不溶于水,密度可能比水的小
C. 遇碱溶液或酸溶液均易变质
D.
A. 3A(g)+B(s)
B. A(g)+B(s)
C. A(g)+B(s)
D. A(g)+2B(s)
- 第二部分:知识运用(共两节, 共45分) 第一节:单项填空(共15小题,每小题1分,满分15分) 从每题所给的A、B、C
- 填入下面横线上最恰当的句子是( ) 真理是朴实无华的。真理就在我们日常生活里,但是看惯了,就发觉不出来了,可是有一天
- .按要求完成下面的对联题。(任选一题3分) (1)上联: 潜心复习战中考; 下联:
- 在下列变化中,属于分解反应的是() A.硫在氧气中燃烧 B.石蜡在空气中燃烧 C.给高锰酸钾加热 D.红磷在空气
- 某校园文学社为了解本校学生对本社一种报纸四个版面的喜欢情况,随机抽查部分学生做了一次问卷调查,要求学生选出自己最喜欢的一
- “三五步走遍天下,七八人百万雄兵”“咫尺地五湖四海,几更时万古千秋”。这些诗句是对下列中国哪种传统艺术特点的描述(
- 如图为小明同学连接的测量小灯泡额定功率的电路图,图中使用了三节干电池作电源,已知小灯泡的额定电压为3.8V,额定功率大约
- 2011年9月29日,国家发改委总结称,“十一五”期间,全国单位GDP能耗下降19.1%,全国二氧化硫排放量减少14.2
- 足量块状铁与100 mL 0.01 mol/L的稀硫酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用
- 若人体唾液淀粉酶反应体系的温度从15 ℃上升至25 ℃,唾液淀粉酶的活性将() A.增大
- 对下列事实解释不正确的是( )选项 事 实 解 释 A 体温计中的水银(汞)热胀冷缩 原子的体积热胀冷缩
- 国民革命时期,孙中山新三民主义与中国的民主革命纲领中最基本的相同点是 A.驱除鞑虏,恢复中华 B.
- “从自然数中任取两数,其中一个是偶数”,这是事件___________________;“从自然数中任取连续两数乘积是偶
- 求适合下列条件的直线方程: (1)经过点,且在两坐标轴上截距相等; (2)经过点,且倾斜角等于直线的倾斜角的倍.
- 一对色盲的夫妇,生育了一个XXY的色盲男孩,下列哪项不可能是致病来源 A.精子形成过程中,减数第一次分裂同源染色体
- 2010年伊始,面对雪灾、旱灾、地震、水灾等一系列灾难,武警官兵、各地人们抗击灾难,保家卫国的精神、气势、壮举令世人提气
- 在氢原子中,可以认为核外电子绕原子核(质子)做匀速圆周运动,轨道半径为 。求电子沿轨道运动的动能。
- 提取下列材料的要点,整合成一个单句来概括材料的主要内容和说明材料的主旨。 ①从19世纪中叶到新中国成立的100多年间,中
- 科学的研究方法是取得成功的关键。下列关于人类探索遗传奥秘历程中的科学实验方法及技术的叙述,不正确的是 A.孟德尔在研究豌
- (有意义吗) to let children watch such TV plays? (要