高考化学试题
A.A
B.B
C.C
D.D
I.(1)用甲醇制取甲胺的反应为
已知该反应中相关化学键的键能数据如下:
共价键 | C―O | H―O | N―H | C―N |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 |
则该反应的△H=__________kJ·mol-1
Ⅱ.一定条件下,将2mol CO和6mol H2通入2L密闭容器中发生如下反应
主反应:![]() △H<0 Ⅰ
△H<0 Ⅰ
副反应:![]() △H<0 Ⅱ
△H<0 Ⅱ
反应到t min时,达到平衡状态。平衡时CH3OH的体积分数φ(CH3OH)如图所示:
(2)图中a___b(填“大于”或“小于”)。图中Y轴表示温度,其理由是__________
(3)若反应II的平衡常数K值变小.则下列说法中正确的是___________(填序号)。
A.平衡均向正反应方向移动
B.平衡移动的原因是升高了温度
C.达到新平衡后,φ(CH3OH)减小
D.容器中φ(CH3OCH3)增大
(4)平衡时,M点CH3OH的体积分数为12.5%,c(CH3OCH3)=0.1mol·L-1,则此时CO的转化率为________;用H2表示I的反应速率为______mol·L-1·min-1。反应Ⅱ的平衡常数K=___________(用分数表示)
A.
B. CH3COOCH2CH3与CHI3CH2COOCH3中均含有甲基、乙基和酯基,为同一种物质
C. C60与14C互为同素异形体
D. 乙酸与硬脂酸互为同系物

已知:
①Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化
②有关Ksp数据如下表所示
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-13 | 10-17 | 10-38 |
回答下列问题:
(1)还原焙烧过程中, MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为___________。传统的工艺是使用浓盐酸在加热条件下直接处理废料,缺点是___________。
(2)酸漫时一般会适当加热并不断搅拌,其作用是___________,滤渣1和滤渣2主要成分的化学式依次是___________。
(3)净化时,先通入O2再加入MnCO3,其目的是___________;已知净化时溶液中Mn2+、Zn2+的浓度约为0.1mol·L-1,调节pH的合理范围是___________。
(4)电解制取MnO2时,MnO2在___________极产生。
(5)中科院研究人员将MnO2和生物质置于一个由滤纸制成的折纸通道内形成电池,该电池可将软饮料中的葡萄糖作为燃料获得能量,装置如图所示。此装置中b极的电极反应式为______________________。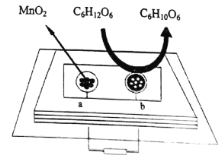
| 目的 | 操作 |
A | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B | 配制浓度为0.010 mol/L的KMnO4溶液 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
C | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
D | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
A. A B. B C. C D. D
某小组实验验证 “Ag + +Fe 2+ 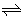
( 1 ) 实验验证
实验 I :将 0.0100 mol/L Ag 2 SO 4 溶液与 0.0400 mo/L FeSO 4 溶液 (pH=1) 等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验 II :向少量 Ag 粉中加入 0.0100 mol/L Fe 2 (SO 4 ) 3 溶液 (pH=1) ,固体完全溶解。
①取 I 中沉淀,加入浓硝酸,证实沉淀为 Ag 。现象是 _______ 。
② II 中溶液选用 Fe 2 (SO 4 ) 3 ,不选用 Fe(NO 3 ) 3 的原因是 _______ 。
综合上述实验,证实 “Ag + +Fe 2+ 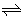
③小组同学采用电化学装置从平衡移动角度进行验证。补全电化学装置示意图 , 写出操作及现象 _______ 。

( 2 ) 测定平衡常数
实验 Ⅲ :一定温度下,待实验 Ⅰ 中反应达到平衡状态时,取 v mL 上层清液,用 c 1 mol/L KSCN 标准溶液滴定 Ag + ,至出现稳定的浅红色时消耗 KSCN 标准溶液 v 1 mL 。
资料: Ag + +SCN - 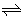
Fe 3+ +SCN - 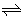
①滴定过程中 Fe 3+ 的作用是 _______ 。
②测得平衡常数 K = _______ 。
( 3 ) 思考问题
①取实验 I 的浊液测定 c (Ag + ) ,会使所测 K 值 _______ ( 填 “ 偏高 ”“ 偏低 ” 或 “ 不受影响 ”) 。
②不用实验 II 中清液测定 K 的原因是 _______ 。
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法 I :氨热分解法制氢气
相关化学键的键能数据
| 化学键 | | | |
| 键能 | 946 | 436.0 | 390.8 |
一定温度下,利用催化剂将 分解为

。回答下列问题:
(1) 反应 
_______
;
(2) 已知该反应的 
A.25 ℃ B.125 ℃ C.225 ℃ D.325 ℃
(3) 某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 
①若保持容器体积不变, 时反应达到平衡,用
的浓度变化表示
时间内的反应速率
_______

的代数式表示 )
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后

③在该温度下,反应的标准平衡常数 _______ 。 ( 已知:分压 = 总压 × 该组分物质的量分数,对于反应





、

方法 Ⅱ:氨电解法制氢气
利用电解原理,将氮转化为高纯氢气,其装置如图所示。
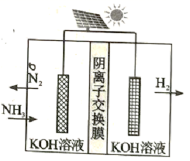
(4) 电解过程中 
(5) 阳极的电极反应式为 _______ 。
KOH 溶液 KOH 溶液

A. 若a=-8,则Kb(XOH)≈10-5
B. M点表示盐酸和XOH恰好完全反应
C. R点溶液中可能存在c(X+)+c(XOH)=c(Cl-)
D. M点到N点,水的电离程度先增大后减小
A. 78g苯中含有的碳碳双键数为3.0NA
B. 4.6g金属钠完全燃烧,转移的电子数为0.4NA
C. 等质量的N2和CO中,原子数均为2.0NA
D. 5.6L(标准状况)O2中含有的质子数为4.0NA
(1)向饱和NaCl溶液中滴入少量浓盐酸,会有白色晶体析出,该晶体的化学式是_____。
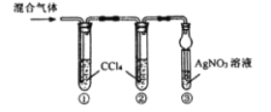
(2)按如图装置,将所得气体通入后,试管内白色晶体析出,能否证明氯气中含有HCl,说明理由_____。b装置的作用是_____。
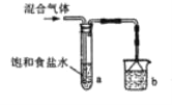
(3)已知氯气易溶于CCl4,按图中装置实验试管③中有白色沉淀,能够证明含HCl,说明理由_____。用浓盐酸与二氧化锰加热经干燥得到1.12L(标况下)气体,除去Cl2后,用水全部吸收并定容至100mL,再通过滴定测HCl气体含量。
(4)定容所需要仪器有烧杯、玻璃棒、________和_____。
(5)取定容后溶液20.00mL,加入2滴酚酞试液,用0.0250mol/L标准NaOH溶液滴定,当______即为滴定终点,消耗NaOH溶液19.20mL,则得到的气体中氯化氢的体积含量是______。
利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。

(2)若将该催化剂置于Na2SO3溶液中,产物之一为![]() ,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):![]()
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。

①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5) ![]() 的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,
的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,![]() =1:_______:__________。
=1:_______:__________。
下列叙述错误的是
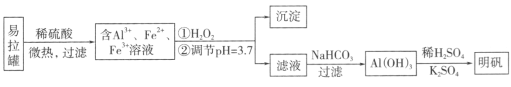
A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
(I)2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
(II)Ba(H2PO2)2+H2SO4=BaSO4↓+ 2H3PO2
下列推断不正确的是
A. 反应I是氧化还原反应,反应II是非氧化还原反应
B. H3PO2具有强还原性,在空气中可能被氧化成磷酸
C. 在反应I中氧化剂与还原剂的质量之比为1: 1
D. 在标准状况下生成2.24LPH3,上述反应转移0.3mol 电子
A. 蒸馏时可通过加碎瓷片防暴沸
B. 可用精密pH试纸区分pH=5.1和pH=5.6的两种NH4Cl溶液
C. 用加水后再分液的方法可将苯和四氯化碳分离
D. 根据燃烧产生的气味,可区分棉纤绵和蛋白质纤维
A. 原子半径:r(W)>r(Y)>r(X)
B. X与Y组成的化合物中均不含共价键
C. Z的简单气态氢化物的热稳定性比W的强
D. WX2是一种高效安全灭菌消毒剂
A.
 过滤
过滤B.
 稀释
稀释C.
 尾气处理
尾气处理D.
 蒸发结晶
蒸发结晶
近年来,我国航空航天事业成果显著。下列成果所涉及的材料为金属材料的是
A.“天宫二号“航天器使用的质量轻强度高的材料——钛合金
B.“北斗三号”导航卫星使用的太阳能电池材料——砷化镓
C.“长征五号”运载火箭使用的高效燃料——液氢
D.“C919”飞机身使用的复合材料——碳纤维和环氧树脂
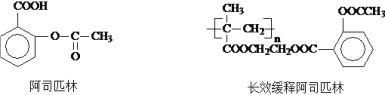
(1)阿司匹林通常在餐后服用,是因为它含有_______(填写官能团符号),易刺激肠胃,给胃部带来不适。
(2)分析说明长效缓释阿司匹林在人体内产生阿司匹林的过程以及长效缓释药品的优点______________
II.以丙酮为主要原料合成长效缓释阿司匹林的流程如下图所示:
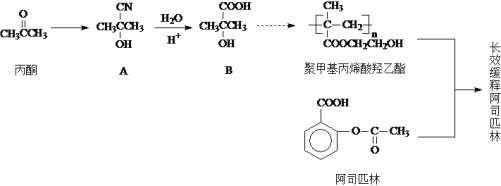
(3)由丙酮得到A的反应类型是_________,还需要的反应物是__________(填化学式)。
(4)写出一种满足下列条件的阿司匹林的同分异构体的结构简式____________。
①能发生银镜反应
②能与NaHCO3溶液反应生成CO2气体 ③能在铜作催化剂的条件下发生催化氧化反应
(5)由B和乙二醇(HOCH2CH2OH)为原料可以制得聚甲基丙烯酸羟乙酯,写出其合成路线(无机试剂任选)___________________。(合成路线常用的表示方式为:A
A. 赤色固体可能是Fe2O3
B. 青矾宜密闭保存,防止氧化变质
C. 青矾燃烧过程中发生了电子转移
D. “青矾厂气”可能是CO和CO2
A. 室温下用稀NaOH溶液吸收Cl2:Cl2+2OH−
B. 用铝粉和NaOH溶液反应制取少量H2:Al+2OH−
C. 室温下用稀HNO3溶解铜:Cu+2
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+
- 下列各组物质,能在pH=1的环境中形成无色溶液的是A.Na2SO4 Ba(OH)2 KClB.CuSO4 NaCl KN
- 如图,AB是⊙O的直径,C是⊙O上一点,且∠A=45°,则下列结论中正确的是 A.BC=AB B. BC
- 国务院决定自2009年1月1日起,实施开征燃油税改革方案:将价内征收的汽油消费税单位税额每升提高0.8元,柴油消费税单位
- 下列各组物质气化或熔化时,所克服的微粒间的作用力属同种类型的是( ) A.碘和干冰的升华
- 配平下列反应: (1)Pt+HNO3+HCl——H2PtCl6+NO↑+________ (2)HClOx+
- 康德为人们打开了一扇更为智慧的大门,是因为他( ) A、提出了“主权在民”的原则 B、提出三权分立的演说
- In our deepmind, we all talk to ourselves—an inner monolo
- 根据材料回答问题,要求语言符合每个人特定的身份,每人不能超过20字。(6分)三个朋友郊游,迎面遇到一株苍劲的巨松,大家都
- 下列植物激素或植物生长调节剂的应用,正确的是 A.可利用适宜浓度的赤霉素处理
- —— I’m sorry the traffic is so heavy. —— Does that _____
- - Which of her parents is a doctor? -- _______ are.
- 某学生的实验报告中有如下数据:①用托盘天平称取11.7 g食盐;②用量筒量取21.48mL盐酸;③用容量瓶配制210 m
- 求tan70°+tan50°-tan50°tan70°的值.
- 求证:
- 常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5
- 命题“方程x2-4=0的解是x=±2”,在这个命题中,使用逻辑联结词的情况是()A. 没有使用逻辑联结词B. 使用了联
- 下列说法中正确的是( ) A. PM 2.5、二氧化碳都属于空气质量日报的内容 B.向煤中加入适量CaSO4,可大大减
- 己知点A(4,0), B(0,4),点P(x, y)的坐标x,y满足, 则的最小值为 A. B.0 C.
- The flowers his friend gave him will die unless ______ every
- Cars are very popular in America.When the kids are fourteen




