高考化学试题
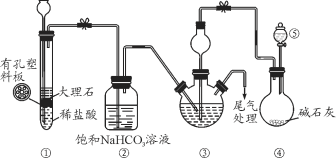
A. 装置①也可用于制取H2
B. ③、⑤中可分别盛放饱和食盐水和浓氨水
C. 应先向③中通入足量NH3,再通入足量CO2
D. ③中反应的离子方程式为NH3+CO2+H2O=NH4++HCO3-
A. 1 mol H2和1 mol I2在加热条件下充分反应,生成HI的分子数为2NA
B. 10g质量分数为46%的乙醇溶液含有的氢原子数目为0.6NA
C. 20 mL 0.1 mol/L AlCl3溶液中,水解形成Al(OH)3胶体粒子数为0.002NA
D. 0.1molNa2O2和Na2O的混合物中含有的离子总数等于0.3NA
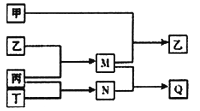
A. 原子半径的大小m>q>n>p
B. 元素非金属性q>n>p
C. Q的溶液可以保存在细口玻璃试剂瓶
D. n的氧化物的水化物一定为强酸
实验室配制碘水时,通常将 
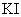
。关于该溶液,下列说法正确的是
A . 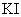
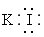
C . 加水稀释,平衡逆向移动 D . 加少量 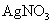
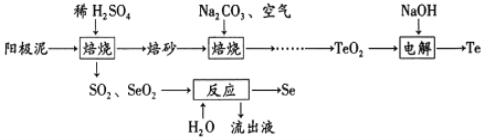
下列叙述错误的是( )
A. 合理处理阳极泥有利于保护环境和资源再利用
B. 流出液是H2SO4溶液
C. 电解过程中阴极上析出单质Te
D. “焙砂”与碳酸钠充分混合后,可在瓷坩锅中焙烧
I.实验室通过如图所示装置制备Na2S2O3

(1)实验中要控制SO2生成速率,可采取的措施有_____________(写出一条)。
(2)b装置的作用是_____________ 。
(3)反应开始后,c 中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为__________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH 溶液”、“水”、“CCl4”中的一种) 的注射器,接下来的操作为______________,最后拆除装置。
II.氰化钠废水处理
(5)已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-==[Ag(CN)2]-,Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
①滴定时1.00×10-4mol/L的标准AgNO3溶液应用________(填仪器名称) 盛装; 滴定终点时的现象是______________。
②处理后的废水是否达到排放标准_______(填“是”或“否”)。
I.(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的化学方程式是____________________。
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应
副反应:
某化学小组利用上述原理在实验室制备过硫酸钠,并用过硫酸钠溶液处理含氰化钠的废水。
实验一:实验室通过如下图所示装置制备Na2S2O8。

(2)装置中盛放双氧水的仪器名称是_________。
(3)装置a中反应产生的气体需要持续通入装置c的原因是______________________。
(4)上述装置中还需补充的实验仪器或装置有__________(填字母)。
A.温度计 B.洗气瓶 C.水浴加热装置 D.环形玻璃搅拌棒
实验二:测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L。
②
(5)滴定终点的现象是__________________________________。
(6)处理后的废水中氰化钠的浓度为_________mg/L;处理后的废水是否达到排放标准?___________(填“是”或“否”)。
Ⅲ.(7)常温下,含硫微粒主要存在形式,受pH影响。利用电化学原理,用惰性电极电解饱和
A. 1L0.1mol·L-1Na2S溶液中含有的S2-的数目小于0.1NA
B. 同温同压下,体积均为22.4L的卤素单质中所含的原子数均为2NA
C. 1mol苯中含有的碳碳双键数为3NA
D. 78g过氧化钠固体中所含的阴、阳离子总数为4NA
A. 常用危险化学品标签中的阿拉伯数字主要表示的是危险级别
B. 石油裂化和裂解制取乙烯、丙烯等化工原料不涉及化学变化
C. 误食重金属盐引起的人体中毒,可以喝大量的食盐水解毒
D. 少量的生石灰能作为鸡舍和猪栏的消毒剂

已知流程中“冶炼”的主要反应的化学方程式为Cu2S+O2
(l)工业炼铁的主要设备是炼铁高炉,该设备中生成铁的主要反应的化学方程式为________
(2)“冶炼”产生烟气中的废气主要是 ___,从提高资源利用率和减排考虑,可将该烟气回收制备____。
(3)电解法炼铜时,阳极是 ___(填“纯铜板”或“粗铜板”);粗铜中含有的金、银以单的形式沉积在电解槽____(填“阳极”或“阴极”)的槽底,阴极的电极反应式是_____
(4)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解。
已知几种物质的溶度积常数(Ksp)如下表:

调节电解液的pH是除去杂质离子的常用方法。根据上表中溶度积数据判断,含有等物质的量浓度的Fe2+、Zn2+、Fe3+、Cu2+的溶液,随着pH的升高,最先沉淀下来的离子是____。一种方案是先加入过量的H2O2,再调节pH到4左右。加入H2O2后发生反应的离子方程式为____。

A. 电极c与a相连,d与b相连
B. 左侧电解槽中:Si 优先于Cu被还原,Cu优先于Si被氧化
C. 三层液熔盐的作用是增大电解反应面积,提高硅沉积效率
D. 相同时间下,通入CH4、O2的体积不同,会影响硅提纯速率

已知:乙酸酐的结构简式为
请回答下列问题:
(1)A的名称是______;B中所含官能团的名称是______。
(2)反应⑤的化学方程式为______,该反应的反应类型是______。
(3)G的分子式为______。
(4)写出满足下列条件的E的同分异构体的结构简式:______、______。
Ⅰ.苯环上只有三个取代基
Ⅱ核磁共振氢谱图中只有4组吸收峰
Ⅲ.1mol该物质与足量NaHCO3溶液反应生成2molCO2
(5)根据已有知识并结合相关信息,写出以
 的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br
的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2BrA. 绚丽缤纷的烟花中添加了含钾、钠、铁、铜等金属元素的化合物
B. 明矾和漂白粉常用于自来水的净化,且原理相同
C. 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质
D. 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
(1)Ni2+电子排布中,电子填充的能量最高的能级符号为______。
(2)金属Ni能与CO形成配合物Ni(CO)4.与CO互为等电子体的一种分子为______(写化学式,下同),与CO互为等电子体的一种离子为______。
(3)丁二酮肟(
(4)丁二酮肟常与NI2+形成图A所示的配合物,图B是硫代氧的结果:
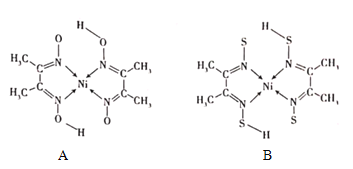
①A的熔、沸点高于B的原因为______。
②B晶体含有化学键的类型为______(填选项字母)。
A.σ键 B.金属键 C.配位键 D.π键
(5)人工合成的氧化镍往往存在缺陷,某缺陷氧化银的组成为Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为______。
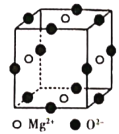
(6)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为______。
下列除去杂质(括号内的物质为杂质)的方法中错误的是( )
A.FeSO4(CuSO4):加足量铁粉后,过滤
B.Fe粉(Al粉):用NaOH溶液溶解后,过滤
C.NH3(H2O):用浓H2SO4洗气
D.MnO2(KCl):加水溶解后,过滤、洗涤、烘干

(1)滤渣I的主要成分是_____(填化学式),写出一种能提高酸浸速率的措施_______。
(2)操作①用到的玻璃仪器有_______________。
(3)H2O2是一种绿色氧化剂,写出加入H2O2后发生反应的离子方程式:_______________。
(4)加入氧化钴的目的是调节溶液的pH.若要将浸出液中Fe3+和Al3+全部沉淀,则应将浸出液的PH控制在_______。(已知:溶液中离子浓度小于1×10-5mol/L,则认为离子完全沉淀;Ni(OH)2、Fe(OH)3、Al(OH)3的Ksp分别为1×10-15, 1×10-38,1×10-32)
(5)加入(NH4)2C2O4反应的离子方程式为________,过滤得到的草酸钴晶体需要用蒸馏水洗涤,检验是否洗涤干净的方法是____________。
(6)加入有机萃取剂的目的是__________。实验室可以用酸性KMnO4标准液滴定草酸根离子(C2O42-)来测定溶液中C2O42-的浓度,KMnO4标准溶液常用硫酸酸化,若用盐酸酸化,会使测定结果______(填“偏高”、“偏低”或“无影响”).
A.
 分离CH3COOH和CH3COOC2H5混合液
分离CH3COOH和CH3COOC2H5混合液B.
 验证NH4NO3晶体溶于水的热效应
验证NH4NO3晶体溶于水的热效应C.
 蒸发FeCl3溶液得到FeCl3固体
蒸发FeCl3溶液得到FeCl3固体D.
 验证C、Cl、Si的非金属性强弱
验证C、Cl、Si的非金属性强弱
下列离子方程式书写正确的是
A.在100 mL 1 mol⸱L−1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++![]() +4H+
+4H+
B.在100 mL 2 mol⸱L−1的FeI2的溶液中通入标况下5.6 L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl-
C.向NaHCO3溶液中加入过量的澄清石灰水:2![]() +Ca2++2OH-═CaCO3↓+2H2O+
+Ca2++2OH-═CaCO3↓+2H2O+![]()
D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2![]() +2Ba2++4OH-═2BaSO4↓+
+2Ba2++4OH-═2BaSO4↓+![]() +2H2O
+2H2O
A. 10 gD2O中含有的质子数与中子数均为5NA
B. 标准状况下,22.4LCHC13中含C-Cl键的数目为3NA
C. 密闭容器中,1mol NH3和1molHCl反应后气体分子总数为NA
D. l00mL1.0 mol/L FeC13溶液与足量Cu反应,电子转移数为0.2NA
A. 2NaBr+Cl2=2NaCl+Br2 B. Br2+2NaI=2NaBr+I2
C. 3Br2+6NaOH
- . The teacher tells his students to _______the dictionary fo
- 四个旅行团选择四个景点游览,其中恰有一个景点没有旅行团游览的情况有( )种 A.36 B.7
- (山东卷)5. 下列各句,没有语病、句意明确的一句是A.这次招聘,一半以上的应聘者曾多年担任外资企业的中高层管理岗位,
- 如图所示,质量为M的木板,上表面水平,放在水平桌面上,木板上面有一质量为m的物块,物块与木板及木板与桌面间的动摩擦因数均
- 函数y=log(x++1)(x>1)的最大值为_____________.
- 下列加横线的字注音完全正确的一项是: A、团箕(jī) 悄(qiǎo)然 发酵(jiào) 长篙(hāo)
- 关于“学习”有两种观点:其一,“人之岁月精神有限,诵说中度一日,习行中错一日;纸墨上多一分,身世上少一分。”其二,“教人
- 2010年1月27日,第40届世界经济论坛年会开幕大会在瑞土达沃斯举行。本届年会的主题是“改善世界状况:反思、重设、重建
- 如果一氨基酸分子中有两个羧基,其中一个羧基连接在R基上,那么另一个羧基部位() A.与氨基端相连 B. 与羧
- 依次填入下列各句横线处的词语,最恰当的一句是( ) ①毫无疑问,入世后凡是违反世贸组织规则的外资限制政策都必须
- 我们用碎冰和碎蜡研究物质熔化过程,为让碎冰和碎蜡均匀缓慢地熔化,我们把碎冰放到盛有温水烧杯中,把碎蜡放到盛有热水的烧杯中
- 据气象专家的调查结果表明。大多数商品的销售量都受气温的影响。各种商品最畅销的气温是:10℃时是防寒衣料,20℃时是空调机
- 在日前召开的全国财政工作会议上,财政部负责人表示,今后一个时期.财政投入将优先向社会主义新农村建设倾斜,向社会事业发展的
- (共10分) W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外
- 20.阅读下面的材料,根据要求作文。 有人发现这样一个现象:在飞机上,同样是30岁到40岁年纪的旅客,头等舱的旅客往往是
- Frank邀请Alice参加他这周日的生日宴会,但Alice的父母不在家要到下个月回来,奶奶又卧病在床,需要人照顾。因此
- 现有一定量的铁粉和铜粉的混合物,将其平均分成四等份,分别加入同浓度不同体积的稀硝酸,充分反应后,在标准状况下生成NO的体
- _________surprised me most was that she didn’t even know __
- 针对日本无理扣押中国渔船船长,温家宝总理表示:这对中方船长及家人造成严重伤害,并激起海内外全体中国人民的愤怒。中方多次严
- (8分)甲、乙两地同时生产某种蔬菜若干吨,现甲地可外销这种蔬菜10吨,乙地可外销这种蔬菜4吨,经调查A、B两城各需这种蔬



