高考化学试题
钴、铁、镓、砷的单质及其化合物在生产生活中有重要的应用。回答下列问题:
(1) 写出As的基态原子的电子排布式_________________。
(2)N、P、As为同一主族元素,其电负性由大到小的顺序为____________________,它们的氢化物沸点最高的是____________。将NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,则该阴离子的化学式是_____________。
(3) Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为______________。
②[Co(N3)(NH3)5]SO4中Co的配位数为____________,其配离子中含有的化学键类型为_______(填离子键、共价键、配位键),C、N、O 的第一电离能最大的为_______,其原因是_____________________。
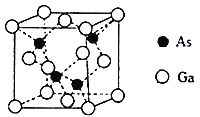
(4) 砷化镓晶胞结构如下图。晶胞中Ga与周围等距且最近的As形成的空间构型为________。已知砷化镓晶胞边长为apm,其密度为pg·cm-3,则阿伏加德罗常数的数值为__________________(列出计算式即可)。
A. 原子半径:W>Z>Y>X>M
B. 常见气态氢化物的稳定性:X<Y<Z
C. 1 mol WM溶于足量水中完全反应,共转移2 mol电子
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
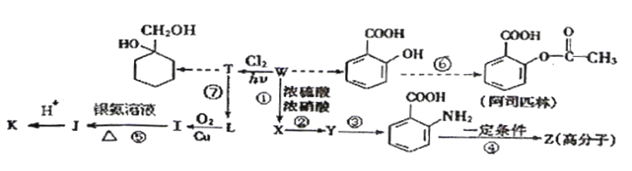
己知部分信息如下:
①1mol 芳香烃W含50mol 电子;
②
③
④K 的分子式为C7H6O2,其核磁共振氢谱上有4 个峰。
请回答下列问题:
(1) X 的名称为_________,Y 中所含官能团的名称为_________ 。
(2)反应⑦的条件为_________,②的反应类型________。
(3)反应⑤的化学方程式为_________。
(4)Z 的结构简式为_________ 。
(5)K 的同分异构体M既能发生水解反应,又能发生银镜反应,M在氢氧化钠溶液中发生水解反应的化学方程式为__________。
(6)
 有多种同分异构体,写出符合以下3个条件的同分异构体的结构简式_________。
有多种同分异构体,写出符合以下3个条件的同分异构体的结构简式_________。①能发生银镜反应但不能水解。
②每摩尔同分异构体最多消耗2mol NaOH。
③苯环上一氯代物只有两种。
(7)请以流程图的形式写出由T制备
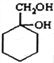 的过程(无机试剂任选) :(仿照
的过程(无机试剂任选) :(仿照 )_____________________
)_____________________
A. 0.1 mol·L-1的氨水:Cu2+、Na+、SO42-、NO3-
B. 0.1 mol·L-1的CaCl2溶液:Na+、K+、Cl-、NO3-
C. 0.1 mol·L-1的Na2SO3溶液:K+、H+、SO42-、NO3-
D. 0.1 mol·L-1的NaHCO3溶液:K+、Na+、NO3-、OH-
A. 碱性:NaOH>LiOH B. 热稳定性:Na2CO3>NaHCO3
C. 酸性:HClO4> H2SO4 D. 气态氢化物的稳定性:HBr > HI
(1)NaClO溶液的物质的量浓度_________mol·L-1。
(2)化学式Na2Sx中的X=____________。
A. 等质量的金刚石和石墨所含的原子数相同
B. 常温常压下,46 g NO2与92 g N2O4,所含的分子数相同
C. 标准状况下,2.24L HF与2.24L HCl所含共价键数目相同
D. 相同体积、相同物质的量浓度的CH3COONa溶液和NaCl溶液所含离子数目相同
A. 牺牲阳极阴极保护法利用的是原电池原理
B. 外加电流阴极保护法利用的是电解原理
C. 牺牲阳极阴极保护法中钢铁为负极
D. 外加电流阴极保护法中钢铁为阴极
A. 我国出土的青铜礼器司母戊鼎是铜和铁的合金
B. 高纯硅具有良好的半导体性能,可用于制光电池
C. 港珠澳大桥钢筋表面的环氧树脂涂层属于合成高分子材料
D. 火箭推进剂使用煤油-液氧比偏二甲肼-四氧化二氮的环境污染小
(1)已知:2CO(g)+O2(g)
H2O(g)+CO(g)
CO(g)+2H2(g)
则CH3OH(g)+
(2)T℃时,向容积均为2L的A、B两个密闭容器中均通入4.0 mol CO2和6.8molH2,发生反应:CO2(g)+3H2(g)
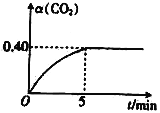
①在0~5min内A容器中v(CH3OH)=_______;该温度下上述反应的平衡常数K=_______(保留两位有效数字)。
②反应开始至平衡的过程中,A、B两容器中CO2的消耗速率的大小关系为v(A) ________(填“>”“<”或“=”)v(B)。
③下列各项指标能表明A容器中反应的v正>v逆的是___(填标号)
a.体系内的压强增大
b.气体的平均相对分子质量增大
c.断裂H-H键的数目是形成C-O键数目的2倍
d.v逆(CO2)=v正(H2)
| 实验操作和现象 | 结 论 |
A | 向浓度均为0.1mol/L的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
B | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,溶液变为红色 | 样品已部分或全部变质 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置润湿的红色石蕊试纸,石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中含Br2 |
A. A B. B C. C D. D
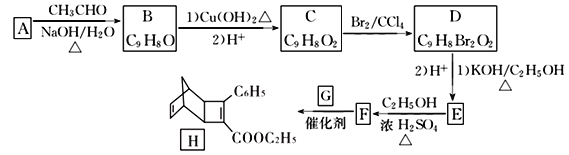
已知:①RCHO+CH3CHO
②
回答下列问题:
(1)A的化学名称是____________,D中含有的官能团名称为_______________________。
(2)由F生成H的反应类型是_______________。
(3)G为甲苯的同分异构体,G的结构简式为_________________。
(4)由D生成E第(1)步的化学方程式为:____________________________________________。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液放出CO2, 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1。符合要求的X有____种。
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C.从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
Ⅰ. KSCN溶液与CuSO4溶液反应,实验如下。
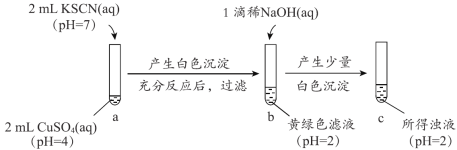
资料:ⅰ.Cu2+可与SCN-反应生成CuSCN白色沉淀和(SCN)2。
ⅱ.(SCN)2称为“拟卤素”,在水溶液中呈黄色;(SCN)2的化学性质与Cl2相似,可与水、碱等发生反应。
(1)a中CuSO4溶液显酸性的原因是______(用离子方程式表示)。
(2)a→b中试管内溶液pH减小,可能的原因是______。
(3)b→c产生沉淀的原因是______。
Ⅱ. 同学们根据相同条件下氧化性:Fe3+>Cu2+,预测Fe3+与SCN-也可发生类似a中的氧化还原反应,进行如下实验。
(4)向Fe2(SO4)3溶液中滴入少量KSCN溶液,观察到______,表明发生了反应:Fe3+ + 3SCN-
(5)基于(4)继续实验:用Fe2(SO4)3溶液、KSCN溶液与石墨电极、电压表、盐桥等组装成原电池,电压表指针几乎不偏转。该实验的目的是______。
(6)查阅资料并讨论后得出:溶液中离子在反应时所表现的氧化性强弱与相应还原产物的价态和状态有关。由此分析a中反应发生的原因:生成CuSCN沉淀使Cu2+的氧化性增强,并补充实验进一步证明。补充的实验是______。
(7)取(4)中反应后溶液,逐滴加入K3[Fe(CN)6]溶液,产生蓝色沉淀,并且沉淀量逐渐增多。该实验结果与(5)中实验结果不一致,解释原因:______。
(8)为进一步证实(7)中的解释,在以上实验的基础上补充实验,其操作及现象是___。

A. 制取NaHCO3的反应是利用其溶解度比较小
B. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
C. 在第③、④、⑤步骤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
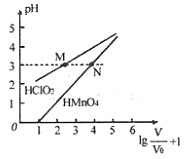
A.
B. 在0≤pH≤5时,
C. 分别往M、N两点对应溶液中滴加1 mo/L NaOH溶液至恰好完全反应,消耗NaOH溶液的体积相等
D. 常温下,浓度均为0.1 mo/L的

已知:Cr2O72-+H2O
回答下列问题:
(1)“粗制盐水”中加入NaOH和Na2CO3的目的是___________________。
(2)过滤时,使用的玻璃仪器有烧杯、玻璃棒和____________。
(3)在pH:6.4~6.8,温度:40~50℃的条件下电解,理论上最终产物只有NaC1O3。电解时阳极的产物为C12,溶液中发生的反应有C12+H2O====HC1O+H++C1-,HC1O
(4)电解槽中温度不宜过高,其原因是_________________________。加入的Na2Cr2O7可以调节电解液酸度,若酸度过大,则电解液中主要存在__________(填“Cr2O72-”或“CrO42-”)。
(5)为检测电解后盐水中NaC1O3的物质的量浓度进行下列实验:
I.准确吸取10.00mL电解后的盐水,加入适量的3%H2O2溶液充分搅拌并煮沸。
Ⅱ.准确吸取0.10mol·L-1的(NH4)2Fe(SO4)2标准溶液25.00 mL于300mL锥形瓶中,加入足量稀硫酸。
III.将I的溶液加入Ⅱ的锥形瓶中,隔绝空气煮沸10min,加热充分反应。冷却至室温后,加入10mL0.4mol·L-1MnSO4溶液、5mL 85%磷酸溶液,用c mol·L-1的KMnO4标准溶液滴定剩余的Fe2+至溶液变为微红色,即滴定终点,此时消耗高锰酸钾V mL。
①步骤I中加入H2O2溶液的作用是______________________。
②步骤Ⅱ中C1O3-被Fe2+还原为C1-的离子方程式为________________________。
③该盐水中NaC1O3的物质的量浓度为________mol·L-1。
元素符号 | X | Y | Z | W |
原子半径/nm | 0.160 | 0.143 | 0.070 | 0.066 |
主要化合价 | +2 | +3 | +3,+5,-3 | -2 |
下列有关叙述正确的是( )
A. 四种元素位于元素周期表的同一周期
B. 电解X的氯化物的水溶液可以得到单质X
C. Y的最高价氧化物对应的水化物既能溶解在盐酸中,又能溶解在氨水中
D. W、Z的氢化物均多于1种
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ·mol-1
CO(g)+0.5O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
H2(g)+0.5O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH4=-41.0kJ·mol-1
则甲烷水蒸气重整反应的ΔH=_____kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
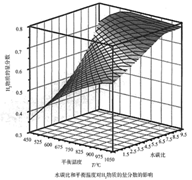
①温度一定时,H2的物质的量分数与水碳比(1~10)的关系是_____,产生该结论的原因是_____。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为_____,其压强平衡常数为_____;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率v=_____。
(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为_____。

A. 标准状况下,WZ为液态 B. 原子半径大小为W<X<Y
C. YQ2和YW4均只含极性共价键 D. 氢化物的稳定性为Q>Y>Z
- 为了庆祝元素周期表建立150周年,联合国宣布将2019年定为国际化学元素周期表年。请从H、C、O、N、Na、Al中选择合
- I got the first prize in last year's competition.A.s
- 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为,下列叙述不正确的
- 中外历史人物评说 材料 唐寅,字伯虎,明中叶杰出的画家、文学家。唐寅曾遭科考案牵连,痛感社会黑暗。为了排遣胸中烦
- 已知函数f(x)=2sin xcos x+2sin2 x-1,x∈R. (1)求函数f(x)的最小正周期和单调递增区间;
- 18.函数f(x)是定义在[0,1]上的增函数,满足f(x)=2f()且f(1)=1,在每个区间(,)(i=1,2,…)
- 设a,b为不重合的两条直线,α,β为不重合的两个平面,给出下列命题: ①若a⊂α,bα,a,b是异面直线,那么b∥α;
- 读美国阿拉斯加州及其附近地区示意图(下图),回答4~5题。 4.阿拉斯加州面积约171万km2,但人口仅60多万。影响其
- Jane Austen, a famous English writer, was born at Steventon,
- (09天津海滨新区五校联考)下列哪一项不是细胞间信息交流的方式
- 背诵、默写(每题1分,共7分) (1)、《望岳》中,诗人化用孔子名言“登泰山而小天下”,表达不但要攀登泰山极顶,更要攀登
- 99式坦克是我军最新型主战坦克,具备优异的防弹外型,其炮塔和车体均采用复合装甲,抗弹能力成倍提高,是我军装甲师和机步师的
- 测滑轮组的机械效率。(4分) (1)利用图13所示的滑轮组成滑轮组,要求弹簧测力计向上拉,在图13中画出滑轮组的绕法。
- — Was it not until last week ______ he decided to give up sm
- 图2-5是改革开放以来全国及国内三大经济地带城市化水平变化情况。改革开放以来我国城市化进程的特点是( ) ①城市化
- 向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中不可能出现的是……( ) ①溶液中有Fe2+、Cu2+
- 小明同学利用电压表和电流表测量小灯泡的电阻值(已知小灯泡的额定电压为2.5V),实验电路图如图左所示。(1)按左图所示的
- Books for ChildrenFleabag and the Ring's End Beth Webb More
- 下列物质的分类组合全部正确的是编组 强电解质 弱电解质 非电解质 A NaCl HF Cl2 B H2SO4 BaSO4
- 下列有关互联网的表述,不正确的是 A.互联网改变了单调的政治生活B.2003年我国互联网用户数居世界第一位 C.中国第一



