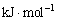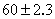高考化学试题
锂-空气电池是一种可充放电池,电池反应为2Li+O2=Li2O2,某锂-空气电池的构造原理图如图。下列说法正确的是
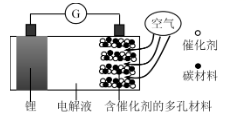
A.可选用有机电解液或水性电解液
B.含催化剂的多孔电极为电池的负极
C.放电时负极的电极反应式为Li-e-=Li+
D.充电时锂电极应连接外接电源的正极
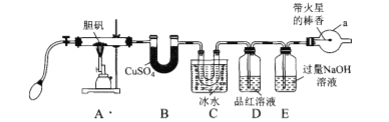
已知:
请回答下列问题:
(1)仪器a的名称是____,a中的棒香能复燃,说明热分解产物含有_____(填化学式)。
(2)A中固体由蓝色变为黑色,B中的现象是____。
(3)C中冰水的作用是_____。
(4)D中品红溶液褪色,E中有
(5)若生成
(6)小组同学用滴定法测定某胆矾样品中
①样品中
②下列操作会导致
a.未润洗锥形瓶
b.滴定终点时仰视读数
c.滴定终点时滴定管尖嘴中有气泡
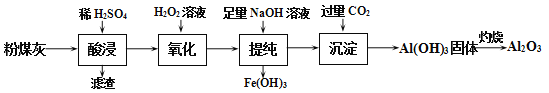
(1)“酸浸”时需加入过量的稀硫酸,目的是提高浸取率和________;滤渣的主要成分是__________。
(2)“氧化”过程中,加入H2O2发生反应的离子方程式为____________。
(3)“提纯”过程中,当加入NaOH溶液达到沉淀量最大时,溶液中c(SO42-)∶c(Na+)=_________。
(4)已知Ksp[Fe(OH)3]=1×10-39。“提纯”过程中,当c(Fe3+)<10-6 mol ·L-1时,溶液中c(OH-)>________mol ·L-1。
(5)“沉淀”过程中,通入过量CO2时发生反应的化学方程式为_____________。
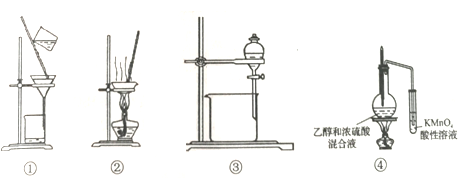
A. 图①所示装置用于粗盐提纯中除掉泥沙
B. 图②所示装置用于蒸干氯化镁溶液制无水MgCl2
C. 图③所示装置用于以己烯为萃取剂萃取溴水中的溴单质
D. 图④所示装置用于验证乙烯的生成
聚合硫酸铁(PFS)是谁处理中重要的絮凝剂,下图是以回收废铁屑为原料制备PFS的一种工艺流程。
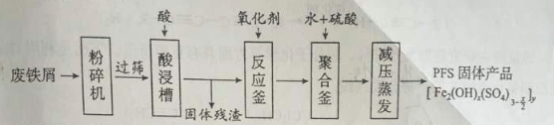
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_________。粉碎过筛的目的是_______
(2)酸浸时最合适的酸是_____,写出铁锈与酸反应的离子方程式_____________________。
(3)反应釜中加入氧化剂的作用是_________,下列氧化剂中最合适的是____________(填标号)。
A.KMnO4 | B. | C. | D. |
(4)聚合釜中溶液的pH必须控制在一定的范围内,pH偏小时Fe3+水解程度弱,pH偏大时则_______。
(5)相对于常压蒸发,减压蒸发的优点是______。
(6)盐基度B是衡量絮凝剂絮凝效果的重要指标,定义式为![]() (n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c
(n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c![]() 的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液
的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液![]() ,已知该样品中Fe的质量分数w,则B的表达式为__________
,已知该样品中Fe的质量分数w,则B的表达式为__________
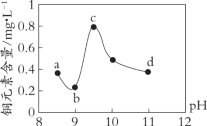
查阅资料,平衡I:Cu(OH)2 + 4NH3
平衡II:Cu(OH)2 + 2OH-
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/ mg·L-1 | 72 | ≤0.5 |
NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法不正确的是
A. 废水中Cu2+处理的最佳pH约为9
B. b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升
C. c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降
D. d点以后,随c(OH-)增加,铜元素含量可能上升
A. 陶瓷坩埚和石英坩埚都是硅酸盐产品
B. 乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
C. 新型材料聚酯纤维、光导纤维都属于有机高分子材料
D. 高分子吸水性树脂聚丙烯酸钠,不溶于水,可吸收其自身重量几百倍的水
A. 元素M的氧化物对应的水化物酸性比G的弱
B. 化合物Z2M、MY2中化学键的类型相同
C. ZX与水的反应属于氧化还原反应
D. 简单离子半径的大小顺序:X<Y<Z<M<G
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_______。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
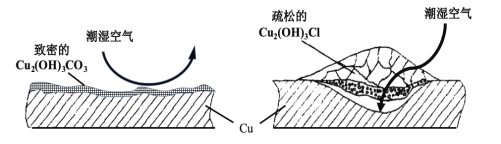
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因_____________。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
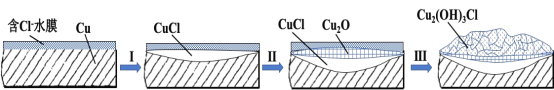
① 过程Ⅰ的正极反应物是___________。
② 过程Ⅰ负极的电极反应式是_____________。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
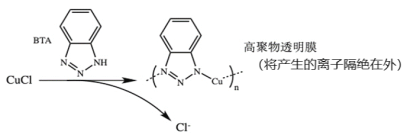
请回答下列问题:
①写出碳酸钠法的离子方程式___________________。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
化学链燃烧 ( 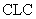
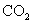
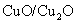
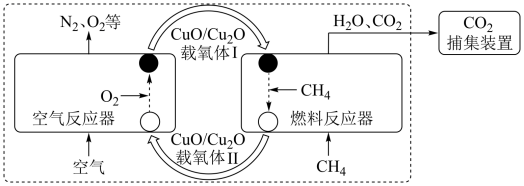
空气反应器与燃料反应器中发生的反应分别为:
①
② 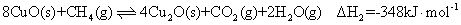
( 1 ) 反应 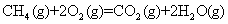
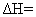
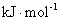
( 2 ) 反应 ②的平衡常数表达式 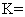
( 3 ) 氧的质量分数:载氧体 Ⅰ _______ ( 填 “>”“=” 或 “<”) 载氧体 Ⅱ 。
( 4 ) 往盛有 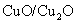
为 21% ),发生反应 ①。平衡时
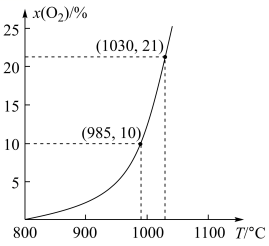
随反应温度 T 变化的曲线如图所示。
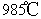
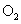
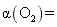
( 5 ) 根据下图, 随温度升高而增大的原因是 _______ 。反应温度必须控制在
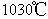
( 6 ) 载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 
| 载氧体掺杂物质 | 氧化铝 | 膨润土 |
| 活化能 / | | |
由表中数据判断:使用 _______ ( 填 “ 氧化铝 ” 或 “ 膨润土 ”) 掺杂的载氧体反应较快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为 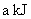
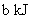
①写出并配平湿法制高铁酸钾反应的离子方程式:______________________________
②每生成l mol FeO42-转移__________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为____mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4)原因是__。
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为____。
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为__。
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为____。
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的0.9倍
D. K3>K2>K1
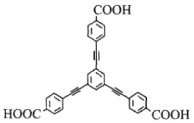
A. 1molM可与足量Na2CO3溶液反应生成1.5molCO2
B. 苯环上的一氯化物有3种
C. 所有碳原子均处同一平面
D. 1molM可与15mol H2发生加成反应
编号 | 实验目的 | 实验方案 |
A | 验证Fe2+还原性弱于I- | 将KI溶液与FeCl3溶液混合后加入CCl4 |
B | 比较氯和碳的非金属性强弱 | 将稀盐酸滴入碳酸氢钠溶液中 |
C | 配制100mL 1mol/LCuSO4溶液 | 将25gCuSO4 5H2O 溶于91mL蒸馏水中 |
D | Mn2+能加快H2C2O4溶液与KMnO4酸性溶液的反应 | 将4mL 0.01mol/L酸性溶液和2mL 0.1mol/LH2C2O4溶液混合 |
A. A B. B C. C D. D
A. Pb位于周期表ⅣA族
B. Pb3O4可以写成2PbO·PbO2
C. PbO2分解生成Pb2O3同时生成O2
D. PbO2可作为铅蓄电池的正极,放电时发生氧化反应
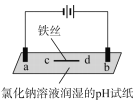
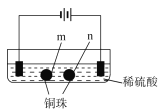
| 实验一 | 实验二 |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
A. 以此类推分子式为C12H12的立体烷烃的结构应为正六棱柱
B. 上述一系列物质互为同系物,它们的通式为C2nH2n(n≥2)
C. 棱晶烷与立方烷中碳原子均为饱和碳原子,其二氯代物都有三种
D. 苯乙烯(
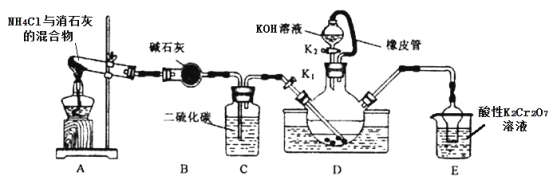
已知:①CS2不溶于水,比水重;NH3 不溶于CS2;②三颈烧瓶内盛放有CS2、水和催化剂。
实验步骤如下:
(1)制备NH4SCN溶液:CS2+3NH3
①实验前,经检验装置的气密性良好。三颈烧瓶的下层CS2液体必须浸没导气管口,目的是_____。
②实验开始时打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,至CS2消失。
则:装置A中反应的化学方程式是_____;装置C的作用是______。
(2)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃,当NH4HS完全分解后(NH4HS= H2S↑ + 3NH3↑),打开K2,再缓缓滴加入适量的KOH溶液,发生反应:NH4SCN + KOH= KSCN + NH3↑ +H2O。
小组讨论后认为:实验中滴加入相同浓度的K2CO3溶液比KOH溶液更好,理由是_____。
(3)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶______,干燥,得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取10.0g样品配成1000mL溶液量取20.00mL于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液做指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液20.00mL。
①滴定时发生的反应:SCN- + Ag+= AgSCN↓(白色)。则判断达到终点时的方法是____。
②晶体中KSCN的质量分数为____。
A. 有无色气体放出
B. 先产生白色沉淀,最后沉淀溶解
C. 先产生白色沉淀,最后沉淀不溶解
D. 既有无色气体放出,又有白色沉淀生成
物质 | HCl(g) | O2(g) | H2O(g) | Cl2(g) |
0min | 4 | 1 | 0 | 0 |
2min | 1.2 | 0.3 | 1.4 |
|
3min | 1.2 | 0.3 | 1.4 |
|
4min | 1.0 | 0.35 | 1.5 |
|
(1)计算0~2min内Cl2的平均生成速率___________________。 该反应合适的温度范围是380~440℃,选择该温度范围可能的原因是:①加快反应速率;②_______________________________。
(2)工业上用传感器检测反应容器中的气体压强,当压强保持不变时,表面反应已达平衡。能通过检测压强判断反应是否达到平衡状态的理由是__________________________。
(3)实验时,在3~4min之间改变了某一条件造成平衡移动。表中数据说明平衡向____移动(填“左”或“右”);达到新平衡后,与原来相比平衡常数_______(填“变大”、“变小”、“不变”)。
(4)Cl2也可用于制备新型净水剂高铁酸钠(Na2FeO4)。配平制备反应的化学方程式___Fe(NO3)3+___NaOH+___Cl2→___Na2FeO4+___NaNO3+___NaCl+___H2O若反应消耗3.36L Cl2(标准状况),则转移电子的数目是________。
(5)用Na2FeO4杀菌消毒的优点是还原产物具有净水作用,缺点是还原产物会对铁制水管造成腐蚀,造成腐蚀的原理有________________________________________。
- 美国1787年宪法的主要起草人汉密尔顿曾引用孟德斯鸠的话“假如人类没有创造出一种政体,它既具有共和政体的内在优点,又具有
- 若方程表示焦点在轴上的椭圆,则的取值范围是 ▲ .
- -- are the blue hats on sale? -- They are on sale for
- 下列说法正确的是( ) A.影响太阳辐射强度的最主要因素是地面状况B.引起大气运动的根本原因是水平气压梯度
- 实验课上,小柯在低倍镜下看清某种细胞结构后,将显微镜轻移到小妍面前给她看,而小妍看到的却是较暗的视野,她首先应操作的是(
- Our sports meeting has been ____ till next Monday because of
- ________ I heard someonecalling for help,Irushed out. A.Imme
- 下列说法:①若a、b互为相反数,则a+b=0;②若a+b=0,则a、b互为相反数;③若a、b互为相反数,则;④若则a、b
- .“三角贸易”是15到19世纪西方殖民掠夺的一个重要方式。读右图《三角贸易示意图》,其中航程B贩运的主要是
- 根据下列表格的对应值,判断方程ax2+bx+c=0(a≠0,a,b,c为常数)一个解的范围是() x 3.23 3.24
- 苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如下图: 关于苏丹红说法错误的是( ) A.分子中含一个苯环和一个
- It was Monday. Mrs Smith's dog was hungry, but there was not
- 早年,梅兰芳在《断桥》中扮演白娘子。白娘子的一个动作是面对负心丈夫许仙追赶、跪求时,她爱恨交加,就用手指去戳许仙的脑门,
- 通过海水晾晒可得粗盐。粗盐除含有NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操
- 如图所示,取稍长的细杆,其一端固定一枚铁钉,另一端用羽毛做一个尾翼,做成A、B两只“飞镖”,将一软木板挂在竖直墙壁上,作
- 写出蜡烛燃烧的文字表达式.
- 在玉米种子的纵剖面上滴加碘液变蓝色的部分是( ) A.胚根 B.子叶
- 设NA代表阿伏加德罗常数的数值,下列说法中正确的是
- 一个人的皮肤干燥、夜盲症等,可能是缺乏 ,佝偻病、骨质疏松症等可能缺乏 ,大脖子病的患者应补
- 用逻辑联结词“且”改写下列命题,并判断它们的真假.(1)0是自然数,0是偶数;(2)26被2和13整除.