高考化学试题
A. 1 mol SO2溶于足量水,溶液中 H2SO3、HSO3-与 SO32-粒子的物质的量之和为 NA
B. 34g H2O2中含有的化学键数目为3NA
C. 常温常压下,17 g 甲基(—14CH3)所含的中子数为 11NA
D. 22.4L Cl2在一定条件下与铁粉完全反应,转移电子数为2NA
《天工开物》中记载: “ 凡乌金纸由苏、杭造成,其纸用东海巨竹膜为质。用豆油点灯,闭塞周围,只留针孔通气,熏染烟光而成此纸,每纸一张打金箔五十度 ……” 下列说法错误的是
A . “ 乌金纸 ” 的 “ 乌 ” 与豆油不完全燃烧有关
B . “ 巨竹膜 ” 为造纸的原料,主要成分是纤维素
C . 豆油的主要成分油脂属于天然高分子化合物
D . 打金成箔,说明金具有良好的延展性

回答下列问题:
(1)A中官能团的名称是_______________。B→C的反应类型是__________________。
(2)B的分子式为________________________。
(3)C→D的化学方程式为__________________________。
(4)F的结构简式为___________________________。
(5)符合下列条件的C的同分异构体共有____________种(不考虑立体异构);
①能发生水解反应;②能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为4组峰的结构简式为_______________(任写一种)。
(6)请以
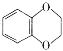 的合成路线(无机试剂任选)_______________。
的合成路线(无机试剂任选)_______________。
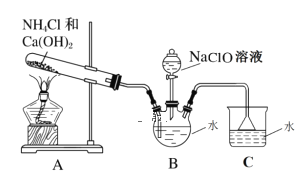
(1)写出肼的电子式__________,写出肼与硫酸反应可能生成的盐的化学式_______;
(2)装置A中反应的化学方程式_____;
(3)实验时,先点燃A处的酒精灯,一段时间后再向B的三口烧瓶中滴加NaClO溶液。滴加NaClO溶液时不能过快、过多的原因___________;
(4)从实验安全性角度指出该实验装置中存在的缺陷_______。
(5)准确量取20.00mL含肼溶液,加入硫酸和碳酸氢钠,用0.1000mol/L的标准碘液进行滴定,滴定终点时,消耗V0mL(在此过程中N2H4→N2)。该实验可选择______做指示剂;该溶液中肼的浓度为______mol/L(用含V0的代数式表达,并化简)。
A. 铝离子的结构示意图:
C. 硫化氢的电子式:
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NO2可消除氮氧化物的污染。已知:
①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.8 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则CH4催化还原NO的热化学方程式为__________________________________。
(2)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)
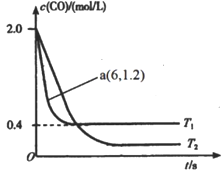
①据此判断该反应的正反应为____(填“放热”或“吸热”)反应。
②温度T1时,该反应的平衡常数K=_____;反应速率v=v正-v逆=k正c2(NO)c2(CO)-k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,计算a处
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素作还原剂,其基本流程如图:
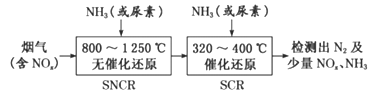
①SNCR-SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0,则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为____________。
②体系温度直接影响SNCR技术的脱硝效率,如图所示:
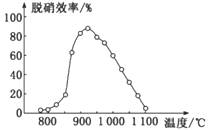
SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是__________;当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是______________。
| A | B | C | D |
实验 | 新制氯水滴入Na2S 溶液中 | 乙醇滴入K2Cr2O7酸性溶液中 | 饱和FeCl3溶液滴入沸水中 | 草酸滴入KMnO4 酸性溶液中 |
现象 | 产生黄色浑浊 | 溶液由橙色变为绿色 | 液体变为红褐色且澄清透明 | 产生无色气体,溶液紫红色褪去 |
A. A B. B C. C D. D

A. 常温对伞花烃呈液态且难溶于水
B. 图Ⅱ物质的一氯代物有5种结构
C. 对伞花烃最多有9个碳原子共平面
D. 图中氢化反应既是加成反应又是还原反应

下列说法不正确的是()
A. 图所示过程①是放热反应
B. 反应Ⅱ的能量过程示意图如图所示
C. 断开3 mol N2H4(g)的化学键吸收的能量大于形成1 molN2(g)和4 mol NH3(g)的化学键释放的能量
D. 200℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2(g)ΔH=+50.7 kJ·mol-1
(1)基态铝原子的核外电子排布式为___________,占据最高能级的电子的电子云轮廓图形状为___________,基态铝原子比基态镁原子的第一电离能(I1)小,其原因是___________。
(2)通常情况下,AlF3可由六氟铝酸铵[(NH4)3AlF6]受热分解制得,请写出该反应的化学方程式______________________。
(3)AlF3具有较高的熔点(1040℃),属于___________晶体(填晶体类型);AlCl3在178℃时升华,写出导致AlF3、AlCl3具有不同晶体类型的原因(从原子结构与元素性质的角度作答)___________。
(4)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出Al原子的杂化形式___________,该阴离子中存在的化学键有___________(填字母代号)
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位健 F.氢键
(5)萤石CaF2晶体的晶胞如图所示,其中Ca2+的堆积方式称为___________。立方体边长为acm,阿伏加德罗常数的值为NA,则CaF2晶体的密度为___________g·cm-3(列出计算式)
A. 实验室用乙醇在140℃可制得乙烯
B. 工业上用煤干馏可得到乙烯
C. 乙烯和Br2发生加成反应,使溴水褪色
D. 乙烯属于饱和烃,能发生聚合反应
(1)基态硼原子的价电子轨道表达式是_______________。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为___________。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的________。
(3)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为________。

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______,写出一种与氨硼烷互为等电子体的分子_____(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH
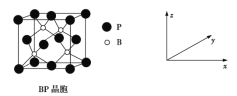
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是_______;已知晶胞边长为458 pm,则磷化硼晶体的密度是____g·cm-3(列式并计算,结果保留两位有效数字,已知4.583=96.07)。
A. 足量SO2通入NaClO溶液中:SO2+H2O+ClO-===SO42-+Cl-+2H+
B. 在稀氨水中通入过量CO2:NH3·H2O+CO2===NH4++HCO3-
C. 用浓H2SO4溶解FeS固体:FeS+2H+===Fe2++H2S↑
D. 氢氧化钡溶液与等物质的量的稀H2SO4混合:Ba2++2OH-+2H++SO42- ===BaSO4↓+2H2O
A. 等质量的N2O和CO2中,分子数均为NA
B. 3.1g 31P与3.2g 32S中,中子数均为1.6NA
C. 0.4 mol BaCl2与0.4 mol Na2O2中,阴离子数均为0.8NA
D. 1mol正丁烷与1mol异丁烷中,化学键数均为14NA
(1)写出Fe的原子结构示意图_____________________,O原子核外电子轨道表示式为______。
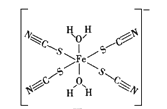
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为__________。如图是SCN−与Fe3+形成的一种配离子,画出该配离子中的配位键(以箭头表示)_______。
(3)K3[Fe(CN)6]晶体中Fe3+与CN−之间的键型为__________,该化学键能够形成的原因是_______。
(4)K3[Fe(CN)5NO]的组成元素中,属于第二周期的元素的第一电离能由小到大的顺序是_____,配合物中原子序数最小的元素与氢元素形成的相对分子质量为92的芳香化合物中,中心原子的杂化轨道类型是_________。
(5)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写出该变化的化学方程式______。
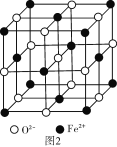
(6)FeO晶胞结构如图2所示,FeO晶体中Fe2+配位数为____,若该晶胞边长为acm,则该晶体密度为___g/cm3(阿伏伽德罗常数的值为NA)。
广东有众多国家级非物质文化遗产,如广东剪纸、粤绣、潮汕工夫茶艺和香云纱染整技艺等。下列说法不正确的是
A . 广东剪纸的裁剪过程不涉及化学变化
B . 冲泡工夫茶时茶香四溢,体现了分子是运动的
C . 制作粤绣所用的植物纤维布含有天然高分子化合物
D . 染整技艺中去除丝胶所用的纯碱水溶液属于纯净物
A. 化合反应 B. 分解反应 C. 氧化还原反应 D. 置换反应
氢化可的松乙酸酯是一种糖皮质激素,具有抗炎、抗病毒作用,其结构简式如图所示。有关该化合物叙述正确的是

A . 分子式为 C 23 H 33 O 6 B . 能使溴水褪色
C . 不能发生水解反应 D . 不能发生消去反应

A. 若a点pH=4,且c(Cl-)=m·c(ClO-),则Ka(HClO)=
B. 若x=100,b点对应溶液中:c(OH-)>c(H+),可用pH试纸测定其pH
C. b~c段,随NaOH溶液的滴入,
D. 若y=200,c点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO)
高分子材料在生产生活中应用广泛。下列说法错误的是
A . 芦苇可用于制造黏胶纤维,其主要成分为纤维素
B . 聚氯乙烯通过加聚反应制得,可用于制作不粘锅的耐热涂层
C . 淀粉是相对分子质量可达几十万的天然高分子物质
D . 大豆蛋白纤维是一种可降解材料
- Very few people have to finish the work before going home, _
- 某大学地理系科考队暑假期间对图示地区进行了地质、地貌等野外考察。据此完成下列问题。(8分)(1)出发前老师提示:“此次
- 民主监督是一种“自下而上”的非权力性监督。回答1~2题。 1.我国宪法和法律赋予公民监督权。公民民主监督的对象是(
- 、两个定值电阻,甲标有“16Ω,1.5A”,乙标有“22Ω,0.5A”,现把它们串联起来,则该串联电路两端允许加的最高电
- 某校研究性学习小组到实验室进行探究实验。他们准备用加热高锰酸钾的方法取氧气并验证氧气的性质。 (1)写出用该方法制取氧气
- 如图所示,甲、乙是摆长相同的两个单摆,它们中间用一根细线相连,两摆线均与竖直方向成θ角。已知甲的质量大于乙的质量,当细
- “在天之变,日月薄蚀。四十二月日一食。五(十)六月月亦一食。食有常数,不在政治。百变千灾,皆同一状,未必人君政教所致。
- I can’t thank you ______ much because without your help I __
- 2、纤维素这种多糖在下列哪种生物体内可以找到( )A.水螅 B.大熊猫 C.柳
- 发现电磁感应现象的科学家是 A.法拉 B.法拉利 C.法拉哥 D.法拉第
- 下面句子中对“济”解释错误的一项是( ) ①无济于事 (有益) ②直挂云帆济沧海
- —How did she find the trip to Beijing last month? —She enjo
- 动物细胞与植物细胞相比,分裂过程基本相同的时期是( )。A. 间期 B. 前期
- You’d sound a lot more polite if you make a request ______ a
- 孟子主张民贵君轻,董仲舒主张君权神授,明末清初的进步思想家黄宗羲提出君主专制是天下之大害。对以上三种观念的理解,其共性是
- 已知ABCD中,=(3,7),=(-2,3),对角线AC、BD交于O,则坐标为( )A.(,5)
- 已知直线和平面,下列推理错误的是( ) A、且B、∥且 C、∥且∥ D、且∥或
- (4分)加速度:是 量。物理意义:描述速度 。方向:与方向相同。当a与v方向
- 41.Heis so (固执的)that no one can persua
- 如图所示,平行板电容器板面水平放置于空气中,两板与电源连接,A板接静电计小球,B板接静电计外壳,这时有一个带电微粒在电容



