高考化学试题

A. 该温度下,Ksp(Ag2CrO4)=4×10-12
B. al、b、c三点所示溶液中c(Ag+):al>b>c
C. 若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点
D. 用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂
(1)湿法空气氧化法回收铈的部分流程如下:
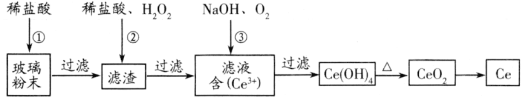
已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。
滤渣的成分是________,反应②的离子方程式是________。
(2)干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为________。两种制备Ge(OH)4的数据如下表:
干法空气氧化法 | 氧化温度/℃ | 氧化率/% | 氧化时间/h |
暴露空气中 | 110〜120 | 90 | 18 |
在对流空气氧化炉中 | 110〜120 | 99 | 8 |
在对流空气氧化炉中大大缩短氧化时间的原因是________。
(3)利用电解方法也可以实现铈的回收。
①在酸性条件下电解Ce2O3 (如图):阳极电极反应式为______,离子交换膜为______ (填“阴”或“阳”)离子交换膜。
②电解产物Ce(SO4)2是重要的氧化剂,将其配成标准溶液,在酸性条件下能测定工业盐中NaNO2的含量,写出发生反应的离子方程式_______。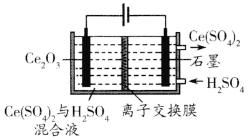
化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 NaHCO 3 ,进一步处理得到产品 Na 2 CO 3 和 NH 4 Cl ,实验流程如图:

回答下列问题:
(1) 从 A ~ E 中选择合适的仪器制备 NaHCO 3 ,正确的连接顺序是 ___ ( 按气流方向,用小写字母表示 ) 。为使 A 中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或 ___ 。
A.  B.
B.  C.
C.  D.
D.  E.
E. 
(2)B 中使用雾化装置的优点是 __ 。
(3) 生成 NaHCO 3 的总反应的化学方程式为 ___ 。
(4) 反应完成后,将 B 中 U 形管内的混合物处理得到固体 NaHCO 3 和滤液:
①对固体 NaHCO 3 充分加热,产生的气体先通过足量浓硫酸,再通过足量 Na 2 O 2 , Na 2 O 2 增重 0.14g ,则固体 NaHCO 3 的质量为 ___ g 。
②向滤液中加入 NaCl 粉末,存在 NaCl(s)+NH 4 Cl(aq)→NaCl(aq)+NH 4 Cl(s) 过程。为使 NH 4 Cl 沉淀充分析出并分离,根据 NaCl 和 NH 4 Cl 溶解度曲线,需采用的操作为 ___ 、 ___ 、洗涤、干燥。

(5) 无水 NaHCO 3 可作为基准物质标定盐酸浓度 . 称量前,若无水 NaHCO 3 保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果 ___ ( 填标号 ) 。
A. 偏高 B. 偏低 不变
合成气(CO+H2)广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气。
(1)已知,5.6LCH4(标况下数据)与水蒸气完全反应时吸收51.5kJ的热量,请写出该反应的热化学方程式___;
(2)在150℃时2L的密闭容器中,将2molCH4和2molH2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的物质的量浓度变化表示该反应速率v(H2)=___。
②该反应的平衡常数表达式K=___。
③下列选项中能表示该反应已达到平衡状态的是___
A.v(H2)逆=3v(CO)正
B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变
D.c(CH4)=c(CO)
④平衡时容器中CH4的体积分数___。
| A | B | C | D |
实验 | 实验室 | 分离苯和溴苯的混合物(沸点:苯为80.1℃,溴苯为156.2℃) | 分离KCl和NH4Cl固体混合物 | 实验室用纯碱和稀硫酸制备二氧化碳 |
实验 |
|
|
|
|
A. A B. B C. C D. D

下列说法正确的是
A.曲线①代表
B.该温度下
C.加适量
D.
A. SO2
B. Fe
C. HCl(aq)
D. Cu2(OH)2CO3
(1)基态锌(Zn)原子的电子排布式为[Ar]_____。
(2)“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是______(填标号)
a 构造原理 b 泡利原理 c 洪特规则 d 能量最低原理
(3)在周期表中,Se与As、Br同周期相邻,与S、Te同主族相邻。Te、As、Se、Br的第一电离能由大到小排序为_______。
(4)H2O2和H2S的相对分子质量相等,常温下,H2O2呈液态,而H2S呈气态,其主要原因是______;
(5)ZnO具有独特的电学及光学特性,是一种应用广泛的功能材料。
①已知锌元素、氧元素的电负性分别为1.65、3.5,ZnO中化学键的类型为______。ZnO可以被NaOH溶液溶解生成[Zn(OH)4]2—,请从化学键角度解释能够形成该离子的原因。_______。

②一种ZnO晶体的晶胞如图所示。晶胞边长为a nm、阿伏加德罗常数的值为NA,其晶体密度为________g·cm−3。
A. 柴油汽车中尿素溶液进入尾气系统,是为了处理尾气
B. “可燃冰”中的甲烷对温室效应的影响几乎为零
C. 古代用明矾除去铜器表面的铜绿,利用了明矾溶液显碱性的特性
D. 铌酸锂( LiNbO3)材料将用于量子通信,41Nb位于第VA族

A. 键的断裂过程是吸热过程,键的形成过程是放热过程
B. “假想的中间物质”的总能量高于起始态H2和Cl2的总能量
C. 反应的△H=[(a+b)-2c]kJ/mol
D. 点燃条件和光照条件下,反应的△H不同
A.定期清淤,疏通河道
B.化工企业“三废”处理后,达标排放
C.利用微生物降解水域中的有毒有害物质
D.河道中的垃圾回收分类后,进行无害化处理
(1)NaCN广泛用于电镀工业上,实验测得浓度相同的NaCN溶液和NaHCO3溶液,前者的pH大,则酸性:HCN___________H2CO3(填“强于”或“弱于”)。
(2)亚硝酰氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由C12和NO在通常条件下反应制得,反应方程式为:2NO(g)+Cl2(g)

当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上热量变化为___________kJ。
(3)在一个恒容密闭容器中充入2 mol NO(g)和1molCl2(g)发生(2)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示:

①T1___________T2(填“>”“≤”或“=”),理由是___________。
②若容器容积为1L,温度为T1℃时,反应开始到5min时,C12的平均反应速率为_______。
③温度为T2℃时,在相同容器中,充入1 molNO(g)和0.5mo1Cl2(g),则NO的平衡转化率___________50%(填“大于”、“等于”或“小于”)
④温度为T2℃时,起始时容器内的压强为p0,则该反应的平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示:

①Ir表面发生反应的方程式为___________。
②若导电基体上的Pt颗粒增多,造成的结果是___________。
二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4)∶n(H2O)=__________。当反应达到平衡时,若增大压强,则n(C2H4)___________(填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示C2H4、CO2变化的曲线分别是______、______。CO2催化加氢合成C2H4反应的ΔH______0(填“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数Kp=_________(MPa)−3(列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。

回答下列问题:
(1)已知:
4Fe(s)+3O2(g)=2Fe2O3(s) △H=akJ/mol
SO2 (g)=S(s)+O2(g)△H=bkJ/mol
Fe(s)+2S(s)=Fe2S(s)△H=ckJ/mol
沸腾炉中主要反应的热化学方程式为____。
(2)如果生产过程中H2的总转化率为90%,FeS2的总转化率为95%,氨与硫酸生成硫酸铵的转化率为100%,则最初FeS2和H2的物质的量之比为 ___。
(3)在一定条件下,分别向体积相同的恒容密闭容器甲,乙、丙中通入一定量的N2、H2或 NH3,发生反应:N2 (g)+3H2=2NH3 (g),相关数据如下:

①乙中NH3的转化率为 ___,丙中x的取值范围为 ___。
②在t1时升高甲容器的温度,至t2时再次达到平衡,测得t2时 混合气体的平均摩尔质量比tl时小。请在图中画出tl~t2 时间段正反应速率的变化示意图______________。

(4)尾气中含有SO2,直接排放会造成环境污染,可用Fe2(SO4)3 溶液吸收。某科研团队对pH、c(Fe3+)、温度等因素对SO2最 高吸收率的影响进行研究,结果如图:

40℃时SO2的最高吸收率随pH、c(Fe3+)的增大而 __,其原因是 ___;温度高于 40℃后,SO2的最高吸收率随温度的升高而减小,其原因是____。

A. M的分子式为C11H12O3
B. 能使溴的四氯化碳溶液褪色
C. 一定条件下,M能生成高分子化合物
D. 能发生加成反应不能发生取代反应
【答案】D
【解析】
试题A.根据物质的结构简式可知M的分子式是C11H12O3,正确; B.该物质的分子中含有碳碳双键,因此能使溴的四氯化碳溶液褪色,正确;C. 该物质的分子中含有碳碳双键,在一定条件下发生加聚反应形成高聚物,正确;D. 化合物M含有碳碳双键,因此能发生加成反应,含有醇羟基、羧基,因此可以发生取代反应,错误。
考点:考查有机物的结构与性质的关系的知识。
【题型】单选题
【结束】
22
【题目】下列有关金属腐蚀与防护的说法不正确的是( )
A. 钢铁发生电化学腐蚀时,若表面水膜呈中性,则正极发生的反应为:2H2O+O2+4e一= 4OH一
B. 在潮湿的空气中,黄铜(铜锌合金)制品比纯铜制品更易产生铜绿
C. 金属制品在海水中比淡水中更容易发生腐蚀
D. 从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程
【答案】B
【解析】A、钢铁发生电化学腐蚀时,若表面水膜呈中性发生吸氧腐蚀,则正极发生的反应为:2H2O+O2+4e一=4OH一,A正确;B、在潮湿的空气中易发生电化学腐蚀,锌的金属性强于铜,因此黄铜(铜锌合金)制品比纯铜制品更不易产生铜绿,B错误;C、海水中含电解质浓度大,淡水中含电解质浓度小,故金属制品在海水中比淡水中更容易发生腐蚀,C正确;D、从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程,D正确;答案选B。
【题型】单选题
【结束】
23
【题目】下列说法不正确的是
A. 麦芽糖及其水解产物均能发生银镜反应
B. 用溴水即可鉴别苯酚溶液,2,4-已二烯和甲苯
C. 在酸性条件下,
D. 用甘氨酸
A. 碳九是多种芳香烃的混合物,可通过石油催化重整得到
B. 进入碳九的泄露区应佩戴含活性炭的口罩,避免吸入有害气体
C. 碳九含上述四种分子的分子式均为C9H12,它们互为同分异构体
D. 碳九含有的有机物均易溶于水,会造成泄露处海域严重污染

A. 表中数字代表元素的原子序数
B. 表中元素的排列依据是元素的原子结构
C. 推测表中“?=70”指代的元素的最高化合价为+4
D. 每一纵行(列)都对应现在常用的元素周期表中的一族
A. 标准状况下,22.4LCO和CO2的混合物中,含碳原子的数目为NA
B. 14g分子式为C5H10的烃中,含有的碳碳双键的数目为0.2NA
C. 0.1mol/L的CH3COONH4溶液中,含铵根离子数目小于0.1NA
D. 标准状况下2.24LCl2通入足量水中或NaOH溶液中,转移电子数目为0.1NA
Ⅰ.碳酸钙的制备

1.步骤①加入试剂A的目的是__________。
2.操作②所需要的玻璃仪器_____________。
Ⅱ.过氧化钙制备
制备步骤
(1)将以上制得的碳酸钙置于烧杯中,逐滴加入6mol·L-1的盐酸,直至烧杯中剩余极少量的碳酸钙固体未溶,将溶液加热煮沸,趁热过滤除去未溶的碳酸钙。
(2)另外量取30mL6%的过氧化氢,加入到15ml浓氨水中,将制得的氯化钙溶液和过氧化氢-氨水混合液置于冰水中冷却,观察白色的过氧化钙晶体的生成。
(3)抽滤,用5mL无水乙醇洗涤2~3次,将晶体抽干。
(4)将抽干后的过氧化钙晶体放在表面皿上,于烘箱内在105℃下烘1h,最后取出冷却,称重。
问题讨论
3.步骤(1)中将溶液煮沸的作用是_________。
4.步骤(2)中反应的化学方程式为__________。
5.步骤(3)中将过滤得到的白色晶体,使用乙醇洗涤的目的是_______。
过氧化钙含量的测定
(1)实验步骤
按下面装置图将量气管与水准管用橡皮管连接,量气管上方的三通活塞,使量气管与大气相通,向水准管内注入水,并将水准管上下移动,以除去橡皮管内的空气。

①精确称取0.40g(精确到0.01g)无水过氧化钙加入试管中,转动试管使过氧化钙在试管内均匀铺成薄层。把试管连接到量气管上,塞紧橡皮塞。悬转活塞使量气管通向试管,调整水准管,记下量气管内液面的初读数。
②用小火缓缓加热试管,过氧化钙逐渐分解放出氧气,调整水准管,记下量气管内液面的终读数,并记录实验时的温度和大气压力。计算出产品中过氧化钙的百分含量。
(2)问题讨论
6.写出上述实验中 “调整水准管”的操作__________。
7.若测得氧气的体积为44.8mL(已经折算成标准状况下),则该研究小组制备的过氧化钙的纯度为____。

A. Li极有机电解质可以换成Cu极的水溶液电解质
B. 放电时,正极的电极反应式为:Cu2O+2H++2e-=2Cu+H2O
C. 放电时,Cu极的水溶液电解质的PH值减小
D. 通空气时,整个反应过程中,铜相当于催化剂
- 核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR
- 如图8中图①,两个等边△ABD,△CBD的边长均为1,将△ABD沿AC方向向右平移到△A′B′D′的位置得到图②,则阴影
- --- Do you want to go out tonight ? ---- _______ ; it’s up
- 下列液体均处于25℃,有关叙述正确的是 A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐B.pH = 4
- 长期营养不良,血浆蛋白降低,会引起水肿,这是因为 ( ) A.血浆
- 阅读下面一段文字,完成5-7题。载人航天最动人的情节是航天员在太空中的精彩表现,完成一系列太空工作之后,总要返回地面,有
- 随着国际石油价格的飙升,电石法制乙炔越来越受重视。工业生产电石是以焦炭和生石灰为原料,在高温下生成CaC2(电石)和CO
- 设在可导,则等于A. B. C. D.0
- 如图所示,闭合开关,两灯都亮不起来,电流表的指针几乎不动,而电压表指针有明显偏转,该电路的故障可能是 A.电流表
- “尽道隋亡为此河,至今千里赖通波。若无水殿龙舟事,共禹论功不较多。”诗中的“河”指的是 A.黄河 B.长江
- 排球场总长为18 m,网高2.25 m,女排比赛时,某运动员进行了一次跳发球,若击球点恰在发球处底线上方3.05 m高处
- 某同学利用电压表和电阻箱测定一种特殊电池的电动势 (电动势E大约在9V左右,内阻r约为50Ω),已知该电池 允许输出的最
- 下列命题中,正确的是( ) A. 若|a|=|b|,则a=b B. 若a=b, 则a与b是平行向量 C. 若|a|
- 某发电站的输出功率为104kW,输出电压为4kV,通过理想变压器升压后向80km远处供电.已知输电导线的电阻率为ρ=2.
- Youmother is waiting for you at home .You'd better ______ r
- 在△ABC中,分别为内角的对边,且 (Ⅰ)求A的大小;(Ⅱ)求的最大值.
- 下列符号中,既能表示氢元素,又能表示氢原子的是()A. 2H B. 2H+ C. 2H2 D. H
- 如图,在⊙O中,O为圆心,点A,B,C在圆上,若OA=AB,则∠ACB=()A.15° B.30° C.45°
- 困扰我国北方农业生产的主要问题是 A.水土流失
- 假如你叫李华, 你的笔友Mike给你写信说他因体重问题被同学嘲笑,想节食减肥,征求你的意见。请根据下面表格内容给他回信,







