高考化学试题
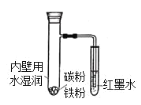
A.具支试管底部发热
B.负极电极反应式:Fe-2e-=Fe2+
C.反应结束后,最终导管内液面下降
D.正极电极反应式:2H2O+O2+4e-=4OH-
温度为T时,在两个起始容积都为1 L的恒温密闭容器发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH<0。实验测得:v正=2v(H2)消耗=2v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2(HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
2HI(g) ΔH<0。实验测得:v正=2v(H2)消耗=2v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2(HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
| 容器 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度 | ||
| c(H2) | c(I2) | c(HI) | ||
| Ⅰ(恒容) | 0.1 | 0.1 | 0 | c(I2)=0.07 mol·L-1 |
| Ⅱ(恒压) | 0 | 0 | 0.6 | |
A.反应过程中,容器Ⅰ与容器Ⅱ中的物质的量比为1∶3
B.两容器达平衡时:c(HI,容器Ⅱ)>3c(HI,容器Ⅰ)
C.温度一定,容器Ⅱ中反应达到平衡时(平衡常数为K),有K=k正/k逆成立
D.达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时v正>v逆
回答下列问题
I.制备富马酸(实验装置如图所示,夹持装置已略去)

(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量水,滴加糠醛并加热至90~100℃,维持此温度3~4h。实验中冷凝管的作用是_________,冷却液宜从___________ (填a”或“b”)处进入。
(2)冰水冷却使其结晶,并通过___________操作可以得到富马酸粗品。
(3)再用1mol·L-1HCl溶液重结晶,得到纯富马酸。该操作中用1mol·L-1HCl溶液的原因是_____________。
Ⅱ.合成富马酸亚铁
(4)取富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH6.5~6.7,产生大量气泡。写出该反应的化学方程式:___________。
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度100℃并充分搅拌3~4h。
①该操作过程中加入适量的Na2SO3溶液,其目的是___________。
②写出生成富马酸亚铁的离子方程式:_____________。
(6)过滤、干燥得到产品。
过滤时滤纸要紧贴漏斗内壁,原因是________。
Ⅲ.产品纯度测定
(7)取0.300g样品置于250mL锥形瓶中,加入15.00mL硫酸,加热溶解后冷却,再加入50.00mL新沸过的冷水和2滴邻二氮菲指示液,此时溶液呈红色;立即用0.1000mol·L-1硫酸铈(Ⅳ)铵[(NH4)2Ce(SO4)3]标准液滴定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗17.30mL标准液,则样品的纯度为___________。
A. 质子数和中子数相等的钠原子:2211Na
B. 氯原子的结构示意图:

C. NaCN的电子式:
D. 丙烯酸的结构简式:CH3CH=CHCOOH
①氨的测定:精确称取wgX,加适量水溶解,注入下图所示的蒸馏烧瓶中(夹持和加热仪器略去),然后逐滴加入足量10%NaOH溶液,加热烧瓶将氨蒸出,用V1mLc1mol·L-1的盐酸吸收蒸出的氨,然后取下锥形瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl。.终点时消耗V2 mLNaOH溶液。

②氯的测定:准确称取样品X配成溶液,用K2CrO4溶液为指示剂,用AgNO3标准溶液滴定,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)
回答下列问题:
(1)X的制备过程中,温度不能过高,其原因是____________________________
(2)仪器a的名称是________________;测定氨前应该对装置进行气密性检验,若气密性不好则测定结果将________(填“偏高”或“偏低”).该滴定过程中选择________做指示剂。
(3)样品中氨的质量分数表达式为_____________________________。
(4)测定氯的过程中,AgNO3标准溶液置于_________(填“无色”或“棕色”)滴定管中;滴定终点时,溶液中已检测不到Cl-[c(Cl-)≤1.0×10-5 mol·L-1],则出现砖红色沉淀时,溶液中c(CrO42-)的最小值为_____________mol·L-1。[已.知:Ksp(AgCl)=1.0×10-10,Ksp( Ag2CrO4)=1.12×10-12]
(5)经测定分析,样品X中钴、氨和氯的物质的量之比为1:6:3,则制备X的化学方程式为________________________________________。
(6)某同学向CoCl2溶液中加入足量(NH4)2C2O4得到CoC2O4沉淀,在空气中煅烧CoC2O4生成钻氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则所得钴氧化物的化学式为________________。
| 异丁醇 | 叔丁醇 |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用蒸馏的方法可将叔丁醇从二者的混合物中分离出来
D. 两种醇发生消去反应后得到同一种烯烃
鸟嘌呤 ( ) 是一种有机弱碱,可与盐酸反应生成盐酸盐 ( 用
表示 ) 。已知
水溶液呈酸性,下列叙述正确的是
A . 
B . 

C . 在水中的电离方程式为:
D . 水溶液中:

Na 2 Cr 2 O 7 的酸性水溶液随着 H + 浓度的增大会转化为 CrO 3 。电解法制备 CrO 3 的原理如图所示。下列说法错误的是

A . 电解时只允许 H + 通过离子交换膜
B . 生成 O 2 和 H 2 的质量比为 8 ∶ 1
C . 电解一段时间后阴极区溶液 OH - 的浓度增大
D . CrO 3 的生成反应为: Cr 2 O +2H + =2CrO 3 +H 2 O
正溴丁烷是稀有元素萃取的溶剂及有机合成的中间体,其制备如图(夹持装置略):

已知:i.NaBr+H2SO4(浓)=HBr↑+NaHSO4
ii.CH3CH2CH2CH2OH十HBr→CH3CH2CH2CH2Br+H2O
iii.2HBr+H2SO4![]() Br2+SO2+2H2O
Br2+SO2+2H2O
iv.正溴丁烷密度:1.27g·mL-1;浓硫酸密度:1.84g·mL-1
请回答下列问题:
(1)正溴丁烷粗产品的制备:
①仪器a的名称是__,向圆底烧瓶中添加药品顺序正确的是__(填正确选项字母)。
A.浓H2SO4→适量水→正丁醇→溴化钠粉末
B.适量水→浓H2SO4→正丁醇→溴化钠粉末
C.适量水→正丁醇→浓H2SO4→溴化钠粉末
D.适量水→正丁醇→溴化钠粉末→浓H2SO4
②装置b中装入NaOH溶液,目的是__。
③加热回流,在此期间要不断地摇动反应装置,其原因为__;冷却后改为蒸馏装置,蒸出其正溴丁烷的粗品。
(2)正溴丁烷的提纯:
①把正溴丁烷粗品倒入分液漏斗中,加入适量水洗涤,分出有机层;
②在另一干燥的分液漏斗中,加入浓硫酸洗去有机层中少量的未反应的正丁醇及副产物,从__(选填“上口”或“下口”)分出有机层;
③有机层依次用适量的水、浓硫酸、水、饱和NaHCO3溶液、水洗涤,用无水CaCl2干燥。以上三次用水洗涤简化为一次用水洗涤是否合理,并说明理由__。
(3)①若洗涤后产物有红色,说明含有溴单质,应加入适量的饱和NaHSO3溶液洗涤,将溴单质全部除去,其反应的离子方程式为__。
②若投入正丁醇11.84g,得到产物12.50g。则正丁醇的转化率为__(保留两位小数)。

下列说法不正确的是
A. 工业上可将ClO2制成NaClO2固体,便于贮存和运输
B. 通入空气的目的是驱赶出ClO2,使其被吸收器充分吸收
C. 吸收器中生成 NaClO2的离子方程式:2ClO2+H2O2=2ClO2-+O2↑+2H+
D. 步骤a的操作包括过滤、洗涤和干燥
下列性质的比较,不能用元素周期律解释的是
A . 酸性: HClO 4 > H 2 SO 3 > H 2 SiO 3 B . 碱性: KOH>NaOH>LiOH
C . 热稳定性: H 2 O>H 2 S>PH 3 D . 非金属性: F > O > N
A. S
B. NH3
C. Cu2(OH)2CO3
D. 饱和NaCl溶液
下列曲线表示卤素元素某种性质随核电荷数的变化趋势,正确的是
A. B.
B.
C. D.
D.

(R1、R2、R3、R4均表示烃基或H原子。)
下列说法不正确的是
A. 过程①中,H2O2作氧化剂 B. 过程②中,有碳碳键、碳氢键断裂
C. 过程③中反应的原子利用率为100% D. 在反应历程中,有水参与反应
Ⅰ.用如图装置来推测乙醇的结构式。
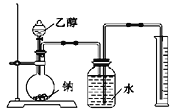
(1)实验中钠需要粉碎成很小的颗粒,其原因是__________。
(2)两次实验平均用乙醇1.15克,收集到气体体积平均为0.28升(换算成标准状态)。由实验数据可以推测乙醇分子的结构,依据是________。
(3)若使用的乙醇中含有少量的水,则收集到氢气的体积________。(偏大、偏小、无影响)
Ⅱ.利用下列装置进行乙醇的催化氧化实验,并检验其产物,其中C装置的试管中盛有无水乙醇。(固定和夹持装置已略去)

(4)装置A圆底烧瓶内的固体物质是________,C中热水的作用是__________。
(5)实验过程中D装置可以观察到的实验现象为_______。写出D处发生反应的化学方程式__________。实验进行一段时间后,如果撤去D处酒精灯,反应能否继续进行?_____。原因是_______。
(6)检验E中的生成物__________。
A. 甘氨酸溶于过量盐酸中生成的离子在电场作用下向阴极移动
B. 植物油和动物油都能发生皂化反应
C. 可以用酸性高锰酸钾溶液鉴别苯和直馏汽油
D. 向鸡蛋清溶液中滴加CuSO4溶液变浑浊,再加蒸馏水,振荡无明显变化
A. 我国在南海成功开采的可燃冰(CH4∙nH2O)可能会带来酸雨等环境污染
B. 大量使用含丙烷、二甲醚等辅助成分的“空气清新剂”,会对环境造成新的污染
C. 某些筒装水使用的劣质塑料桶常含有乙二醇(HOCH2-CH2OH),乙二醇不溶于水
D. 我国全面启动的北斗导航系统的信号传输与硅有关
绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了 Cr—Fe—Al—Mg 的深度利用和 Na + 内循环。工艺流程如图:
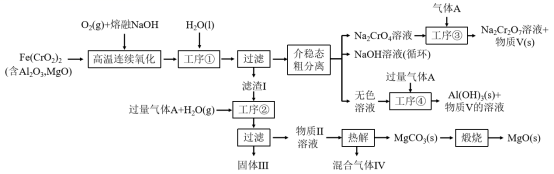
回答下列问题:
(1) 高温连续氧化工序中被氧化的元素是 ___ ( 填元素符号 ) 。
(2) 工序 ①的名称为 __ 。
(3) 滤渣的主要成分是 __ ( 填化学式 ) 。
(4) 工序 ③中发生反应的离子方程式为 ___ 。
(5) 物质 V 可代替高温连续氧化工序中的 NaOH ,此时发生的主要反应的化学方程式为 __ ,可代替 NaOH 的化学试剂还有 ___ ( 填化学式 ) 。
(6) 热解工序产生的混合气体最适宜返回工序 ___ ( 填 “ ① ” 或 “ ② ” 或 “ ③ ” 或 “ ④ ”) 参与内循环。
(7) 工序 ④溶液中的铝元素恰好完全转化为沉淀的 pH 为 __ 。 ( 通常认为溶液中离子浓度小于 10 -5 mol•L -1 为沉淀完全; A1(OH) 3 +OH - 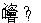
: K =10 0.63 , K w =10 -14 ,
![]()
A. 胶体:分散质颗粒直径1﹣100mm的分散系
B. 弱电解质:HClO、NH3•H2O、AgCl、NH4NO3
C. 混合物:空气、盐酸、王水、氯水、水玻璃
D. 有机物:丙醇、丙酸、1,2﹣二溴戊烷、碳酸钠

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中的平衡浓度与pH的关系如图所示(25℃):
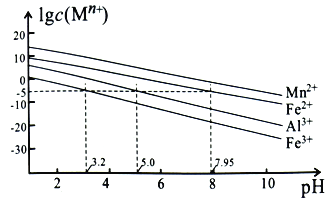
③此实验条件下Mn2+开始沉淀的pH为7.54;离子浓度≤10-5mol·L-1时,离子沉淀完全。
请回答:
(1)传统工艺处理高硫锰矿时,不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为___________。
(2)“氧化”时,发生反应的离子方程式为_________________________________。若省略“氧化”步骤,造成的后果是_________________________________。
(3)“中和除杂”时,生成沉淀的主要成分为______________________(填化学式)。
(4)“氟化除杂”时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于___________。(已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12)
(5)“碳化结晶”时,发生反应的离子方程式为______________________。
(6)“系列操作”指___________、过滤、洗涤、干燥
(7)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为___________。
- 在锐角△ABC中,内角A,B,C的对边分别为,且. (Ⅰ)求角A的大小; (Ⅱ)若,求△ABC的面积.
- 新中国60华诞喜逢团圆中秋,沉浸在喜悦中的海内外网民通过各种方式在网上欢度佳节,感受节日的温馨和亲情,表达对中国明天的美
- 下图反映四个城市某年人口资料。四个地区中,经济发展较快、就业水平最高的是 A.甲 B.乙
- 已知一玉米植株的基因型为AABB,周围虽生长有其他基因型的玉米植株,但其子代不可能出现的基因型是() A.AABB
- 歌曲是流动的历史,记录着时代的变迁。下列歌词出现在社会主义道路探索时期的是 A.“没有就没有新中国” B.“雄赳
- 高温下硫酸亚铁发生如下反应:2FeSO4Fe2O3+SO2↑+SO3↑若将生成的气体通入氯化钡溶液中,得到的沉淀是
- Read the following text and choose the most suitable headin
- 写出求(共7个3)的值的一个算法,并画出流程图.
- 能直接鉴别氯化钠和葡萄糖两种未知浓度溶液的方法是( ) A.观察颜色 B.测量比重
- 下列物质投入盐酸溶液中,没有CuCl2生成的是( ) A. Cu
- 的倒数是___________.
- 若A=(x+3)(x+7),B=(x+4)(x+6),则A、B的大小关系为________.
- I want to be liked and loved for _______ I am inside. A. who
- 函数的定义域是
- 某校为了了解学生的课外阅读情况,随机调查了50名学生,得到他们在某一天各自课外阅读所用时间的数据,结果用右侧的条形图表示
- 下列动物的行为中,哪些属于学习行为: ( ) A.繁殖行为 B.迁徙行为
- 有5列火车停在某车站并行的5条轨道上,若快车A不能停在第3道上,货车B不能停在第1道上,则5列火车的停车方法种数共有(
- 我国古代中央机构不断变革,曾出现三公九卿、三省六部、内阁、军机处等制度。这些变革反映的趋势是不断强化
- 假设某中心血防站调查了1788个MN血型血样本,其中397人是M型(LM LM),861人是MN型(LMLN),530人
- 短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外




