高中 化学
-
(1) Mg、Al的物质的量各为多少?
-
(2) 若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积。


-
(1) 与氩原子电子层结构相同的﹣2价阴离子的结构示意图.
-
(2) 写出含有6个质子,8个中子的原子的化学符号是.
-
(3) 用“<”或“>”填空:A.酸性:H2SO4HClO4 , B.碱性:Ca(OH)2Ba(OH)2
-
(4) 用电子式表示氯化镁的形成过程.
2CO(g)+4H2(g)⇌CH3CH2OH(g)+H2O(g)△H=﹣256.1kJ•mol﹣1
已知:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1
-
(1) 以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g)△H=.
-
(2) 汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.
①某研究小组在实验室以Ag﹣ZSM﹣5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1.若不使用CO,温度超过800℃,发现NO的转化率降低,其可能的原因为;在n(NO)/n(C O)=1的条件下,应控制的最佳温度在左右.

②用活性炭还原法处理氮氧化物.有关反应为:C (s)+2NO2(g)⇌N2 (g)+CO2 (g).某研究小组向某密闭容器中加入足量的活性炭和NO,恒温( T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol∙L﹣1
时间/min
NO
N2
CO2
0
1.00
0
0
20
0.40
0.30
0.30
30
0.40
0.30
0.30
40
0.32
0.34
0.17
50
0.32
0.34
0.17
I.根据表中数据,求反应开始至20min以v(NO)表示的反应速率为(保留两位有效数字),T1℃时该反应的平衡常数为(保留两位有效数字).
II.30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是.图2表示CO2的逆反应速率[v逆(CO2)]随反应时间的变化关系图.请在图中画出在30min改变上述条件时,在40min时刻再次达到平衡的变化曲线.
 CO2+2H2O
B . CH2=CH2 +H2
CO2+2H2O
B . CH2=CH2 +H2 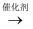 CH3CH3
C .
CH3CH3
C .  2CH3CHO+2H2O
2CH3CHO+2H2O
①根据氧化物的组成将氧化物分成酸性氧化物、碱性氧化物
②根据反应中是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔现象分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据物质在水中的溶解度,将物质分为可溶性物质、微溶性物质和难溶性物质

下列说法正确的是( )
 并调节
并调节 , 离子方程式为
, 离子方程式为 D . 取洗脱后的溶液检验
D . 取洗脱后的溶液检验 的方法是直接加入少量稀硝酸和淀粉溶液,观察溶液是否变蓝
的方法是直接加入少量稀硝酸和淀粉溶液,观察溶液是否变蓝
25℃时,CH3COOH的电离常数Ka=1.8×10-5。常温下,往25ml氢氧化钠标准溶液中逐滴加入0.2 mol·L-1的CH3COOH溶液,pH变化曲线如下图所示:

(1)该氢氧化钠溶液的物质的量浓度为________mol·L-1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH-)=____ mol·L-1。
(3)B点所示溶液中,c(CH3COO-)-c(Na+)=_______________ mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=_______。
(4)C点所示溶液中,c(CH3COOH) c(CH3COO-)。(填“>”、“<”或“=”)
(5)向300 mL上述NaOH溶液中通入448 mL CO2(标准状况)气体,充分反应后,溶液中粒子浓度关系正确的是________.
A.c(Na+)+ c(H+)= c(OH-)+ c(HCO3-)+ c(CO32-)
B.2/3c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.c(Na+)> c(CO32-)> c(HCO3-)> c(OH-)> c(H+)
D.c(Na+)> c(HCO3-)> c(CO32-)> c(OH-)> c(H+)
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填
入下面对应的横线上,组成一个未配平的化学方程式。
+ ![]()
![]() + + +H2O
+ + +H2O
(2)反应物中发生氧化反应的物质 ,被还原的元素是 。
(3)反应中1 mol氧化剂得到 mol电子。
(4)请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
□ +□ 。
3个装有CH4和Cl2混合气体的集气瓶,用玻璃片盖好瓶口后,分别作如下处理,各有怎样的现象发生?
(1)①置于黑暗中:________________;
②将点燃的镁条靠近集气瓶外壁:________________;
③放在有光线的房子里:________________________。
(2)CH4和Cl2发生的一系列反应都是________(填反应类型)反应,请写出CH4和Cl2反应生成一氯甲烷的化学方程式:__________。
(3)若要使0.5 mol CH4完全和Cl2发生取代反应,并生成相同物质的量的四种取代产物,则生成HCl的物质的量为________。
A.2.5 mol B.2 mol
C.1.25 mol D.0.5 mol
有机物与生产、生活息息相关。现有下列有机物:①乙烯 ②油脂 ③乙二醇 ④纤维素。请将相应的序号填入空格内。
(1)能加强肠胃蠕动的是_________; (2)能用于制造肥皂的是________;
(3)能用于汽车防冻液的是________; (4)能用于植物生长调节剂的是________。
反应A(g)+3B(g) ![]() 2C(g);ΔH<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是 ( )
2C(g);ΔH<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是 ( )
A.正反应速率加大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率变小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率和逆反应速率减小,平衡向正反应方向移动
D.正反应速率和逆反应速率减小,平衡向逆反应方向移动
下列反应的离子方程式书写正确的是( )
A. 氯化铁溶液与碘化钾溶液反应:Fe3++2I-===Fe2++I2
B. 硫酸溶液与氢氧化钡溶液反应:Ba2++SO![]() ===BaSO4↓
===BaSO4↓
C. 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+===Ca2++H2O+CO2↑
D. 氯化铝溶液与过量氨水反应:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
“神舟”飞船成功发射,标志着我国航天科技达到了较高水平。为了降低宇航员所在轨道舱和返回舱内二氧化碳的浓度,同时释放氧气,舱内放入下列哪种物质能满足上述要求( )
A.H2O B.Na2O2 C.KClO3 D.KMnO4

已知:
(1)A中含氧官能团的名称是______。
(2)反应①的试剂和条件为_______,B的结构简式为______。
(3)D为酯类,以乙醛为原料,写出合成D所涉及的化学方程式______。
(4)2 D → E + C2H5OH,F中含有醇羟基,写出下列物质的结构简式:E________ F________G___
(5)反应①~⑥中属于取代反应的有______。
- 阅读图文资料,回答下列各题。(10分) 材料一 2011年1月26日,日本九州南部的雾岛山新燃岳火山喷发,激起的火山灰
- 在“测定电池的电动势和内阻”的实验中 (1) 第一组同学利用如图a所示的实验装置测量,电压表应选择量程 (填“
- 在观察如图17所示小球摆动时动能和势能转化的实验中,小涛发现小球每摆一个来回的时间似乎都相同。于是他产生了猜想,小球来回
- 2011年11月01日5时58分07秒,我国成功发射神州八号飞船,它将与天宫一号实现空中对接,从而建立我国第一个空间实验
- 下列词语中没有错别字的一组是( ) A.提纲 融洽 拭目以待 通货膨涨 B.赋
- 2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑
- 阅读理解 This is a beautiful park near my home. People like togo
- 33. Although I’ve never worked for a bank before, I feel qui
- .能鉴别MgI2、AgNO3、Na2CO3 、NaAlO2四种溶液的试剂是() A.HNO3 B.KOH C.B
- 下列各句中,加点的成语使用最恰当的一句是 A.范仲淹的《岳阳楼记》言从楼起,但意在楼外,写景抒情曲尽其妙,炼词造句独具匠
- 如图①已知△ABC中,AB=BC=1,∠ABC=90°,把一块含30°角的三角板DEF的直角顶点D放在AC的中点上(直角
- 在等比数列{an}中,若a2+a3=4,a4+a5=16,则a8+a9= (A) 128 (B)
- 定义:对函数,若存在常数,对任意的,存在唯一的,使得,则称函数在上的“均值”为.已知,,则其反函数在[10 ,100]上
- “火车教会人们守时,准时准点成了现代生活的准则,人们开始要随身带上一块表,时间概念是一个全新的概念。”这种情况最早应始
- 有一个直流电动机,把它接入0.2V电压的电路时,电动机不转,测得流过电动机的电流是0.4A,若把它接入2V电压的电路中,
- 读“1984年到1996年我国流动人口数量的变动图”,回答下列问题(共13分):(1)从1984年到1996年,我国人口
- 科学家在对人和猪的胰岛素进行对比研究后发现,二者仅相差一个氨基酸,于是便对猪的胰岛素基因作了适当的改造和修饰,然后将其导
- 补写出下列名句名篇中的空缺部分。 (1)子曰:“不愤不启,不悱不发,___________________,则不复也。”
- 近代割占中国领土最多的国家是 A英 B法 C俄 D美
- 1.下列词语中,加横线字的读音全都正确的一项是( ) A.饿莩(fú) 饯别(jiàn) 凝



