高中 化学

 C . 若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D . 反应至15min时,改变的反应条件是降低温度
C . 若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D . 反应至15min时,改变的反应条件是降低温度
 +6H2O。则下列有关说法错误的是( )
+6H2O。则下列有关说法错误的是( )
 +6H2O
D . 每转移0.6 mol电子,则消耗氧气的体积为3.36L
+6H2O
D . 每转移0.6 mol电子,则消耗氧气的体积为3.36L
A.A(g)+B(g)=C(g)△H1<0 A(g)+B(g)=C(l)△H2<0 则△H1△H2
B.S(g)+O2(g)=SO2(g)△H1<0 S (s)+O2(g)=SO2(g)△H2<0 则△H1△H2
C.C(s)+O2(g)=CO2(g)△H1<0 C(s)+ 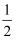 O2(g)=CO(g)△H2<0 则△H1△H2 .
O2(g)=CO(g)△H2<0 则△H1△H2 .
-
(1) NaCl溶液加热蒸干后最终产物是
-
(2) NaHCO3溶液加热蒸干灼烧后最终产物是
-
(3) AlCl3溶液加热蒸干灼烧后最终产物是
-
(4) Na2SO3溶液加热蒸干灼烧后最终产物是.
选项 | A | B | C | D |
生活中的物质 | 食盐 | 熟石灰 | 复方氢氧化铝片 | 酒精 |
有效成分的化学式 | NaCl | CaO | Al(OH)3 | C2H5OH |
用途 | 做调味品 | 干燥剂 | 做抗酸药 | 消毒 |
-
(1) 在稀盐酸中,NaNO2会与Fe2+反应生成一种无色气体M,气体M对该反应有催化作用,其催化原理如图所示。 M的化学式为; Fe2+在酸性条件下被O2氧化的离子方程式为。

-
(2) 盐基度[B=
 × 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响。(填“越大”、“越小”或“无影响”)
× 100%]是衡量净水剂优劣的一个重要指标。盐基度越小,净水剂对水pH变化的影响。(填“越大”、“越小”或“无影响”)
-
(3) PFC样品中盐基度(B)的测定:
已知:PFC样品的密度ρ = 1.40 g·mL−1 , 样品中铁的质量分数ω(Fe) = 16%
步骤1:准确量取1.00 mL PFC样品置于锥形瓶中。
步骤2:加入一定体积0.05000 mol·L−1的盐酸标准溶液,室温静置后,加入一定体积的氟化钾溶液(与Fe3+反应,消除Fe3+对实验的干扰),滴加数滴酚酞作指示剂,立即用0.05000 mol·L−1氢氧化钠标准溶液滴定至终点,消耗氢氧化钠标准溶液13.00 mL。
步骤3:准确量取1.00 mL蒸馏水样品置于锥形瓶中,重复步骤2操作,消耗氢氧化钠标准溶液49.00 mL。
根据以上实验数据计算PFC样品的盐基度(B)(写出计算过程)。
已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论正确的是
A.氯化铝硬度大,固体可导电
B.氯化铝易溶于有机溶剂,难溶于水
C.氯化铝中存在离子键
D.氯化铝属于分子晶体
下列变化中,不存在化学键断裂的是
A . 氯化氢气体溶于水 B . 干冰升华
C . 氯化钠固体溶于水 D . 氢气在氧气中燃烧
常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
① pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是: ;
② 0.2 mol·L-1 HA溶液与0.1mol·L-1 NaOH溶液等体积混合后所得溶液中:c(H+)+c(HA)-c(OH-)= mol·L-1。(溶液体积变化忽略不计)
A是一种重要的化工原料,A的产量通常用衡量一个国家石油化工发展水平标志。E是具有果香气味的烃的衍生物。A、B、C、D、E在一定条件下存在如下转化关系(部分反应条件、产物被省略)。

(1)工业上,由石油获得石蜡油的方法是 ;
(2)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式是: ;
(3)A→B的化学方程式是: 该反应的反应类型是 ;
(4)B→C的化学方程式为: 该反应的反应类型是 ;
(5)反应B+D→E的反应的速率比较缓慢,我们在实验中为了提高该反应的速率,通常采取的措施有: 。
某金属A及其化合物之间有如下的
 转化关系:
转化关系:
(1)写出下列物质的化学式:
A ;D
(2)向B溶液中加入KSCN溶液现象
再加入A振荡后现象
(3)写出E生成C的化学方程式
已知:还原性HSO3﹣>I﹣,氧化性IO3﹣>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )

A.0~b间反应:3HSO3﹣+IO3﹣=3SO42﹣+I﹣+3H+
B.a点时消耗NaHSO3的物质的量为1.2 mol
C.b~c间反应:I2仅是氧化产物
D.c点之后碘的物质的量不变是因为还原剂消耗完全
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 。
(5)科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。当收集的N2体积为 3.36L(已换算为标准状况)时,可制备纳米级Cu2O的质量为 ;
下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是
A. NaOH的碱性比Mg(OH)2的强
B. Cl2得到电子的能力比Br2的弱
C. 原子半径r: ![]()
D. 原子的最外层电子数n: ![]()
今有氧、镁、铝、硫、铬5种元素,试回答下列问题
(1)镁晶体堆积方式为 ▲ 堆积(选填:“简单立方”、“体心立方”、“面心立方”、“六方”);
(2)用“>”、“<”填写下表
| 第一电离能 | 电负性 | 晶格能 | 沸点 |
| Mg ▲ Al | O ▲ S | MgO ▲ MgS | H2O ▲ H2S |
(3)基态铬原子外围电子轨道表示式为 ▲ 。
反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥
C.②③⑤ D.③⑤⑥
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如右图。下列
 叙述正确的是( )
叙述正确的是( )
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
.物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl-的物质的量之比为( )
A.1∶1∶1 B.1∶2∶3
C.3∶2∶1 D.3∶4∶3
向某碳酸钠溶液中逐滴加1 mol·L-1的盐酸,测得溶液中Cl-、HCO![]() 的物质的量随加入盐酸体积的关系如图所示,其中n2∶n1=3∶2,则下列说法中正确的是
的物质的量随加入盐酸体积的关系如图所示,其中n2∶n1=3∶2,则下列说法中正确的是
A.b点的数值为0.6
B.该碳酸钠溶液中含有1 mol Na2CO3
C.b点时生成CO2的物质的量为0.3 mol
D.oa段反应的离子方程式与ab段反应的离子方程式相同
A. 浓硫酸具有脱水性,可用于干燥氯气
B. 晶体硅熔点高,可用于制作半导体材料
C. Na2CO3溶液显碱性,可用热的纯碱溶液洗油污
D. FeS固体呈黑色,可用于除去废水中Cu2+、Hg2+等重金属
- I’m a writer and ___________ language is the tool of _______
- 一个由中、美、俄等国科学家组成的研究小组给食盐施加 20 万大气压,生成了一些“不可能”的物质如氯化三钠和三氯化钠。按照
- 一电路图如图所示,从A到B共有 条不同的线路可通电.
- 固定光滑斜面与地面成一定倾角,一物体在平行斜面向上的拉力作用下向上运动,拉力F和物体速度随时间的变化规律如图所示,取重力
- 2010年2月20日凌晨开始,持续数小时的暴风雨猛烈袭击马德拉岛,这是马德拉岛自1993年以来遭受的最大的一次强暴风雨。
- 硫氰(SCN)2有如下系列化学反应: ①NaSCN+NaHSO4Na2SO4+HSCN↑②MnO2+4HSCNMn(SC
- 质量相等的物体A和B并排放在光滑水平面上,现用―水平推力F推物体A,同时在与力F相同方向给物体B一冲量I,两物体都开始运
- 依次填人下列各句横线处的词语,恰当的一组是 ①广大群众认为:綦江市彩虹桥倒塌案公开审理是 公平性、公正性的体
- 在一定条件下,氯气与碘单质以等物质的量进行反应,可得到一种红棕色液体ICl,ICl有很强的氧化性,ICl跟Zn、H2O反
- 如图,△ABC是边长为1的等边三角形.取BC边中点E,作ED∥AB,EF∥AC,得到四边形EDAF,它的面积记作S1;取
- 小明发现野营篝火的火焰很小,便将木柴架空火焰就大了,他这样做主要是为了 A.降低木柴的着火点
- 下列方程中有两个不相等实数根的方程是() A.x2﹣2x+2=0 B. =﹣1 C.x2﹣3x+
- 镓元素的单质是半导体材料。下列有关说法错误的是( ) A.镓的核电荷数是31 B. 镓原子核外电子数是31
- 《论语》十二章(节选) ①子曰:“学而时习之,不亦说乎?有朋自远方来,不亦乐乎?人不知而不愠,不亦君子乎?” ②曾子曰:
- 臭氧层保护是当今全球最重要的环保议题之一。图2反映了9月份30°S~80°S平流层臭氧总量多年变化状况。读图2回答第1-
- 图9是安装在列车车厢之间的摩擦缓冲器结构图,图中①和②为楔块,③和④为垫块,楔块与弹簧盒、垫块间均有摩擦,在车厢相互撞击
- 小明从眼镜上取下一块镜片,透过镜片观看邮票上的文字(如图所示).小明用的镜片是_______透镜,所成的是_______
- Thebig desk toomuch room. Please take it away.
- 下列加线字与“函封之”中的“函”用法不同的一项是 () A.君为我呼入,吾得兄事之 B.秦伯说,与郑人盟 C.项伯亦拔剑
- 已知实数x,y满足的图象与坐标轴所围成的封闭图形的内部的概率为 A.



