高中 化学
⑴X、Y、Z的单质在常温下均为气体;
⑵X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
⑶XZ极易溶于水,在水溶液中电离出X+和Z﹣ , 其水溶液能使蓝色石蕊试纸变红;
⑷每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
⑸Z单质溶于X2Y中,所得溶液具有漂白性.
试写出其元素符号:X,Y,Z,以及化合物的分子式:XZ,X2Y.
 的
的 溶液中加入
溶液中加入 的盐酸(混合后溶液的体积变化忽略不计)。已知25℃时,
的盐酸(混合后溶液的体积变化忽略不计)。已知25℃时, 。请回答下列问题:
。请回答下列问题:
-
(1) 混合后溶液的pH=。
-
(2) 混合后溶液中
 mol/L(写出计算过程)。
mol/L(写出计算过程)。
| 实验 | 结论 | |
| A | 某有机物完全燃烧,只生成CO2和H2O | 该有机物属于烃类物质 |
| B | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中羟基上的氢与水分子中的氢具有相同的活性 |
| C | 向苯酚溶液中滴加几滴浓溴水,无白色沉淀生成 | 苯酚与浓溴水不反应 |
| D | 将铜丝在酒精灯外焰上加热,变黑后再移至内焰,变黑的铜丝恢复红色 | 酒精灯内焰有挥发出的乙醇蒸气,将变黑的铜丝还原 |
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。 
请回答下列问题:
-
(1) 盛放浓盐酸的仪器名称是,a的作用为。
-
(2) b中采用的加热方式的优点为,b中反应的化学方程式为。
-
(3) c中采用冰水浴冷却的目的是。
-
(4) d中可选用试剂___________(填标号)。A .
 B . NaCl
C .
B . NaCl
C .  D .
D . 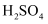
-
(5) 反应结束后,取出b中试管,经冷却结晶,,洗涤,干燥,得到
 晶体。
晶体。
-
(6) 取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入  振荡,静置后
振荡,静置后  层显色。可知该条件下NaClO的氧化能力
层显色。可知该条件下NaClO的氧化能力  (填“大于”或“小于”)。
(填“大于”或“小于”)。
-
(1) 合金在生活中的应用很普遍,其优点是,常见的合金有.
-
(2) 金属的腐蚀使我们生活中常看到的现象.家用铁锅洗后容易生锈,请举出一种避免生锈的办法.
-
(3) 服用药物时要对症下药.以碳酸氢钠为主要成分的药物适合治疗.
-
(4) 蛋白质是生命的基础,没有蛋白质就没有生命.蛋白质的基石是.常利用(填“盐析”“变性”或“颜色反应”)分离、提纯蛋白质.
①气体的质量为,气体中含氢原子的物质的量为 mol。
②气体中所含分子数为。
③气体在标准状况下的体积为。
④将气体甲完全溶解于水中形成500mL溶液,所得溶液溶质的物质的量浓度为 mol•L-1。
⑤将④中所得溶液取出100mL,加水稀释至1000ml,所得溶液溶质的物质的量浓度为 mol•L-1。

-
(1) 上述反应中生成二氧化硫的化学方程式为
-
(2) 乙同学认为还可能产生氢气的理由是
-
(3) 丙同学在安装好装置后,必须首先进行的一步操作是
-
(4) A中加入的试剂可能是,作用是;B中加入的试剂可能是,作用是;E中加入的试剂可能是,作用是.
-
(5) 可以证明气体X中含有氢气的实验现象是C中:,D中:.如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?(填“能”或“不能”),原因是.
(1)NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是________。
(2)实验室中不能用硫化钠溶液和氯化铝溶液混合来制取硫化铝,原因是______
(用化学方程式表示)。
(3)溶液中SO32-与H+不能大量共存,是因为发生了_________反应,酸性条件下NO3-与Fe2+不能大量共存,是因为发生了_________反应(填反应类型)。
(4)只选用一种试剂就能把浓度均为1 mol·L-1的Na2SO4、Na2SO3、Na2CO3、BaCl2溶液加以区别,这种试剂是。
A.CaCl2 B.AgNO3 C.H2SO4 D.NaOH
某化学兴趣小组在实验室中探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,现象如下:

下列有关三种金属的说法中正确的是( )
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和MgCl2溶液不发生化学反应
(1)氯水有漂白作用,是由于其中含具有漂白性的__________(填“![]() ”或“
”或“![]() ”)的缘故。奶粉中________(填“蛋白质”或“葡萄糖”)含量不足,将导致食用这种奶粉的婴幼儿营养不良。
”)的缘故。奶粉中________(填“蛋白质”或“葡萄糖”)含量不足,将导致食用这种奶粉的婴幼儿营养不良。
(2).属于人体生命活动必需的微量元素是__________(填“Fe”、“H” 或“Na” );钢铁暴露在潮湿空气中发生电化学腐蚀的实质是:钢铁表面的水膜与铁和碳组成了无数微小的________________。
(3).蛋白质是构成生命的基础物质,是日常膳食的重要组成部分。下列食物中富含蛋白质的是_______(填序号)。①苹果 ②葡萄糖 ③牛奶
下列离子方程式正确的是( )
A.向氢氧化钡溶液中加硫酸溶液 Ba2+ + SO42- ![]()
![]() BaSO4 ↓
BaSO4 ↓
B.用食醋与苏打溶液反应(主要成分是碳酸钠) 2CH3COOH + CO32- ![]()
![]() 2CH3COO- + CO2↑ +H2O
2CH3COO- + CO2↑ +H2O
C.石灰乳与碳酸钠溶液混合Ca2+ + CO32- ![]()
![]() CaCO3 ↓
CaCO3 ↓
D.氧化铁溶于稀硝酸 Fe2O3 + 6H+ ![]()
![]() 2Fe3+ + 3H2O
2Fe3+ + 3H2O
在下列过程中,需要加快化学反应速率的是( )
A. 钢铁腐蚀 B. 食物腐败 C. 炼钢 D. 塑料老化
下列仪器名称为“容量瓶”的是
![]() A.
A.![]() B.
B.![]() C.
C.![]() D.
D.
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.1mol二甲醚中含有的C—O键的数目为2NA
B.标准状况下,44.8L HF中含有分子的数目为2NA
C.200g质量分数为23%的HCOOH水溶液中含氧原子的总数目为2NA
D.在反应Cu2S+O2![]() 2Cu+SO2中,每生成1molCu,转移电子的数目为2NA
2Cu+SO2中,每生成1molCu,转移电子的数目为2NA
NA表示阿伏德罗常数的值,下列叙述正确的是
A. 标准状况下,33.6 L H2O含有的H2O分子数为1.5 NA
B. 常温常压下,32g O2和28 g N2所含分子个数比为1:1
C. 0.5 mol/L AlCl3溶液中含有的Cl 数为1.5 NA
D. 1 mol Na2O2与足量CO2完全反应转移的电子数目为2 NA
已知I-、Fe2+、SO2、Cl-、H2O2都有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2。则下列反应不能发生的是
A. 2Fe3++SO2+2H2O=2Fe2+ +SO42-+4H+
B. I2+SO2+2H2O=H2SO4+2HI
C. H2O2+H2SO4=SO2+O2+2H2O
D. 2Fe3++2I-=2Fe2++I2
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.加入苯酚显紫色的溶液:Cu2+、 NH4+、 Cl-、SCN-
B.无色透明的溶液:Na+、 Fe2+、![]() 、
、 ![]()
C.![]() =10-2 mol/L的溶液:K+、Na+、
=10-2 mol/L的溶液:K+、Na+、 ![]() 、CH3COO-
、CH3COO-
D.能使酚酞变红的溶液:Mg2+、 Ba2+、ClO-、 I-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使酚酞呈红色的溶液:Na+、NO3-、Ba2+、Br-
B.加水稀释pH减小的溶液:K+、Al3+、Cl-、CH3COO-
C.含有大量Fe(NO3)2的溶液:NH4+、H+、SO42-、I-
D.c(OH-)<![]() 的溶液:ClO-、NO3-、Na+、Ca2+
的溶液:ClO-、NO3-、Na+、Ca2+
- “谷撒地,薯叶枯,青壮炼铁去,收禾童与姑,来年日子怎么过”,诗中反映的20世纪50年代末的现象,主要由于: ( )
- (10分)阅读短文,回答问题:巨磁电阻效应1988年阿尔贝·费尔和彼得·格林贝格尔发现,在铁、铬相间的三层复合膜电阻中,
- 我国最东端、最北端所在省区是( )A、黑龙江 B、内蒙古、黑龙江 C、黑龙江、辽宁
- 下图是某区域某时刻近地面天气简图。读图,回答6~7题。6.图中M气压中心形成的主要因素是 A.洋流影响 B.海陆热
- a=(-2,1),b=(x,-3),a∥b,则x= .
- 中国坚持走和平发展道路,通过维护世界和平发展自己,又通过自身发展维护世界和平。这表明中国的发展() ①不走国强必霸的路子
- 已知:甲乙两组数据的平均数都是5,甲组数据的方差,乙组数据的方差,下列结论中正确的是()A. 甲组数据比乙组数据的波动大
- 己知在碱性溶液中可发生如下反应:2R(OH)3 +3C1O- +4OH- =2RO4n-+3Cl-+5H2O。则RO
- 首届中国国际文化创意产业博览会以“点亮创意智慧,融入科技力量,焕发文化魅力,创造财富价值”为宗旨,以“创意、科技、文化”
- 1947年收回汉口、九江英租界的是
- . Jim isn't _____, but he did badly in the final exams last
- 23592U常用于制造原子武器。关于23592U原子的说法正确的是 A.中子数为92
- 已知是两条不同直线,是三个不同平面,则下列正确的是( ) A. 若,,则 B. 若,,则 C. 若,,
- 明天数学课要学“勾股定理”,小敏在“百度”搜索引擎中输入“勾股定理”,能搜索到与之相关的结果个数约为12 500 000
- Was it because of the bad weather _____ the sports meeting h
- 如图11-1-10所示为电视机显像管偏转的示意图,圆环上的偏转线圈通以图示方向的电流时,圆心O处的磁场方向为______
- 阅读下面这首诗,然后回答问题。 清 溪 行 李 白 清溪清我心,水色异诸水。借问新安江,见底何如此? 人行明镜中,鸟度屏
- 一架飞机从海口起飞,如果途中不改变方向,一直朝正北飞行,最终可以 A.绕地球一周 B.到达南极点
- 常温下,下列各组离子一定能大量共存的是() A.3% H2O2溶液中:Fe2+、H+、SO、Cl- B.使甲基橙试液变红
- 阅读下面文字,完成下面小题。 全球化时代中国设计的发展趋向 王丽文 全球化是一个既让人欢迎又让人不安的现象。全球化对设



