高中 化学
 B .
B . 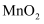 和
和  C .
C . 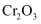 和
和  D .
D .  和FeO
和FeO

已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
-
(1) BaTiO3中Ti 元素的化合价为:。
-
(2) 用盐酸酸漫时发生反应的离子方程式为:。
-
(3) 流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有。
②如何证明晶体已洗净?。
-
(4) TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,共目的是:。
-
(5) 某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3 , 得产品13.98g,BaTiO3的产率为:。
-
(6) 流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c([Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为mol/L。
 )的说法,正确的是( )
)的说法,正确的是( )
 2Sn+aM↑+CO2↑,则下列说法中错误的是( )
2Sn+aM↑+CO2↑,则下列说法中错误的是( )
 X一个该原子的基本微粒(质子、中子、电子)的总数是( )
X一个该原子的基本微粒(质子、中子、电子)的总数是( )
①1L0.1 mol·L-1 FeCl3溶液中含Fe3+数目为0.1NA
②5.6g铁粉与3.2g硫粉混合隔绝空气加热,充分反应后,转移电子数为0.2NA
③0.1mol乙醇与0.1mol乙酸在浓硫酸催化并加热下,生成乙酸乙酯分子数为0.1NA
④60gSiO2中含有的Si-O键和12g金刚石中含有的C-C键的数目均为NA
⑤体积为11.2L的氯气中含有氯原子数约为6.02×1025个
⑥92g的NO2和N2O4混合气体含有的原子数为6NA
⑦10g46%甲酸( HCOOH)水溶液中所含的氧原子数为0.5NA
⑧7.8gNa2O2与足量的水(H218O)反应生成的氧气中所含的中子数为0.5NA
 含Fe2+电镀液
B .
含Fe2+电镀液
B .  含Fe2+电镀液
C .
含Fe2+电镀液
C .  含Zn2+电镀液
D .
含Zn2+电镀液
D .  含Zn2+电镀液
含Zn2+电镀液

| 实验组别 | | 温度/℃ | 形状 |
| Ⅰ | 2.0 | 30 | 块状 |
| Ⅱ | 2.5 | 30 | 块状 |
| Ⅲ | 2.5 | 50 | 粉末状 |
| Ⅳ | 2.5 | 50 | 块状 |
某烧杯中含有0.2mol NH4Al(SO4)2,向其中缓缓加入4mol/L的NaOH溶液180mL,使其充分反应,此时烧杯中铝元素的存在形式( )
A.Al3+和Al(OH)3 B. ![]() C.
C. ![]() 和Al(OH)3 D.Al(OH)3
和Al(OH)3 D.Al(OH)3
氢氧化钡是一种使用广泛的化学试剂。某课外小组通过下列实验测定某试样中Ba(OH)2・nH2O的含量。
(1)称取3.50g试样溶于蒸馏水配成100mL溶液,从中取出10.0mL溶液于锥形瓶中,加2滴指示剂,用0.100mol/LHCl标准溶液滴定至终点,共消耗标准液20.0mL(杂质不与酸反应),求试样中氢氧化钡的物质的量。
(2)另取5.25g试样加热至失去全部结晶水(杂质不分解),称得质量为3.09g,求Ba(OH)2・nH2O中的n值。
(3)试样中Ba(OH)2・nH2O的质量分数为 。
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、与铝反应产生大量氢气![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
B、能使硫氰化钾溶液显红色的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
C![]() 、常温下
、常温下![]() 值为13的溶液中:
值为13的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
D、在使石蕊试液变红的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()

A. 电子流动方向为a→导线→b
B. H+经质子交换膜由右向左移动
C. 放电一段时间b极附近pH不变
D. a电极发生反应:H2N(CH2)2NH2+16e-+4H2O==2CO2↑+N2↑+16H+

A. 原子半径的大小W <X<Y B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态 D. X的最高价氧化物的水化物为强酸
- 在同一平面内,下列说法正确的是 ( ).A.两直线的
- 按下列要求书写化学方程式: ⑴天然气的主要成分甲烷在空气中燃烧 ; ⑵在通电条件下只有两种气体生成的分解
- It is really a bad news that after his father died last year
- 阅读下面的文字,完成小题。(25分) 齐白石与知己徐悲鸿 齐白石出生于湖南湘潭一个农民家庭,他从一个木匠而成为一个在世界
- 下图是分泌细胞分泌的某种物质与靶细胞结合的示意图,据图回答:(1)分泌细胞的分泌物与靶细胞相互结合的原因是靶细胞膜上有_
- 正确量取8.5mL的液体,应选用的合适仪器有() ①5mL量筒②10 mL量筒③50
- You’d better TV too often. It’s bad for your eyes.
- 在1~18号元素中(稀有气体元素除外),元素所形成的最稳定的气态氢化物是____________(填化学式,下同);与水
- 依次填入下列各句横线上的词语,最恰当的一组是 () ①野生动物是人类的朋友,然而却有不少人在利益
- (12分)在△ABC中,已知,.
- 一质子以1.0×107 m/s的速度与一个静止的未知核碰撞.已知质子的质量是1.67×10-27 kg,碰撞后质子以6.
- 需求价格弹性表示某商品的需求量变动对于该商品的价格变动的反应程度,其系数为需求量的变动百分率与价格的变动百分率之比。假定
- I don't think difficult for a Chinese student to master a fo
- 熊猫是我国的国宝,假如一对熊猫所生4个熊猫宝宝的基因型测定为RRLL、Rrll、RRll和rrLL。则该对熊猫的基因型是
- 动物的行为多种多样,属于学习行为的是A.蜘蛛结网 B.鹦鹉学舌 C.鸟类孵卵
- 如图所示,可视为质点的小球A、B用不可伸长的细软轻线连接,跨过固定在地面上半径为R的光滑圆柱,A的质量为B的三倍。当B位
- 的算术平方根是 .
- 选出标点符号使用无误的一项 A.我一进门的时候本来就有点疑惑,现在更加疑惑了;虽然猜不出是谁,但自己断定,一定是一个不平
- 某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动. (1)该反应的化学方程式为. (2)反应后
- Wembley Stadium(温布利大球场)is one of the _____ soccerfields in





