高中 化学
X | ||
Y | ||
Z |
-
(1) I.NaNO2和食盐外观很像,曾出现误把NaNO2当食盐而造成人员中毒的事情,在酸性溶液中它也是一种氧化剂,如NaNO2能把Fe2+氧化成Fe3+。已知NaNO2水溶液呈碱性,AgNO2是一种难溶于水白色固体。NaCl溶液呈中性。试回答下列问题:
人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐,如NaNO2 , 则导致血红蛋白中的Fe2+转化为Fe3+而中毒(FeCl2溶液为浅绿色,FeCl3溶液为棕黄色),可以服用维生素C解毒,维生素C在解毒的过程中表现出(填“氧化”或“还原”)性。
-
(2) 下列方法中,不能用来区分NaNO2和NaCl的是__________。A . 测溶液的酸碱性 B . 加入AgNO3溶液观察是否有沉淀生成 C . 分别在它们的酸性溶液中加入FeCl2溶液,观察溶液颜色变化
-
(3) II. H3PO2是精细磷化工产品。工业制备原理如下:
a.2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑
b.Ba(H2PO2)2+H2SO4=BaSO4↓+2H3PO2
下列推断正确的是__________
A . 反应a是氧化还原反应,反应b是复分解反应 B . H3PO2中P化合价是+1 C . 在反应a中发生氧化反应与还原反应的原子个数之比为1:1 -
(4) 某离子反应涉及到H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程,ClO-表现出性。
、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,请写出反应的离子方程,ClO-表现出性。 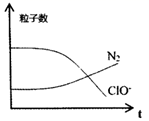
-
(5) 用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴入物质M的饱和水溶液,继续煮沸至液体呈红褐色,停止加热。写出该过程反应的化学方程式。
 ﹣NMR(核磁共振)可用于含碳化合物的结构分析,
﹣NMR(核磁共振)可用于含碳化合物的结构分析,  表示的是( )
表示的是( )
-
(1) I.
 ,反应过程的能量变化如图所示:
,反应过程的能量变化如图所示: 
已知2mol
 和
和  反应生成为1mol
反应生成为1mol  的
的  ,请回答下列问题.
,请回答下列问题.该反应通常用
 作催化剂,加
作催化剂,加  会使图中B点(填“升高”或“降低”).
会使图中B点(填“升高”或“降低”). -
(2) 图中
 .
.
-
(3) 如果反应速率
 为
为  ,则
,则  .
.
-
(4) II.已知下列热化学方程式:
①


②


③


④


回答下列问题:
上述反应中属于熵减反应的是;(写序号)
-
(5) 燃烧20 g
 生成液态水,放出的热量为;
生成液态水,放出的热量为;
-
(6) 写出CO燃烧的热化学方程式;
-
(7) 写出制水煤气的热化学方程式.
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
-
(1) 该烃分子的摩尔质量.
-
(2) 确定该烃的分子式.
-
(3) 已知该烃的一氯代物只有一种,写出该烃的结构简式.

已知:①A的核磁共振氢谱有两组峰,且峰面积之比为3∶1;
②G的结构简式为: ![]() ;
;
③ ![]() 。
。
回答下列问题:
-
(1) A的名称是;B→C的反应类型是。
-
(2) G的分子式为;G中官能团名称是;1 mol G与NaOH溶液反应最多消耗 mol NaOH。
-
(3) H的结构简式为。
-
(4) D在浓硫酸加热的条件下会生成一种含六元环的化合物,写出该反应的化学方程式。
-
(5) I与F互为同分异构体,则满足下列条件的I的结构有种(不包括F)。
①苯环上有两个取代基;②遇FeCl3溶液显紫色;③能与NaOH反应。
-
(6) 根据题中所给信息,写出由苯酚,甲苯为原料制备苯甲酸苯酚酯的合成路线(其它无机试剂任选):。
-
(1) 工业废水中含有重金属离子Cu2+ , 需要将其转化沉淀除去,请选择合适沉淀剂.已知常温下:
Cu(OH)2 KSP=2.2×10﹣23
CuS KSP=6.3×10﹣36
-
(2) ①完成表格办1mol/L下列离子,沉淀完全阳离子浓度为10﹣5 mol/L
Fe2+
Fe3+
Cu2+
开始沉淀时pH
完全沉淀时pH
8
3.2
6.7
②能否控制pH将三种离子逐一分离出溶液.
浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况)。试计算:
(1)反应后生成硫酸铜的物质的量。
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫![]() 酸铜的物质的量浓度。
酸铜的物质的量浓度。
用下列装置进行的实验, 能达到相应实验目的的是

A. 用装置①配制一定浓度的硫酸溶液
B. 用装置②分离溶解在CCl4中的 I2
C. 用装置③制备和收集少量 NH3
D. 用装置④验证FeCl3 对 H2O2分解有催化作用
洗涤含SO2的烟气。以下物质可作洗涤剂的是________。
a.Ca(OH)2 b.Na2CO3
c.CaCl2 d.NaHSO3
在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是 ( )。

A.a反应:Fe2++2H++H2O2===Fe3++2H2O
B.b反应:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C.c反应:H++OH-===H2O
D.d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
为测定某有机物A的结构,进行如下实验:
(1)将一定量的有机物A置于氧气流中充分燃烧,实验测得:生成0.3molH2O和0.2 molCO2,消耗氧气6.72L(标准状况下),则该物质的实验式是 。
(2)用质谱仪测定该有机物的相对分子分子质量,得到如图所示的质谱图,则其相对分子质量为
,该物质的分子式是 。
 |
(3)根据价键理论,预测A的可能结构并写出结构简式: 、 。
(4)经测定,有机物A的核磁共振氢谱如下图所示,则A的结构简式为 。
 |
针对下列实验现象表述不正确的是
A.用同一针筒先后抽取80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色
B.在表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,固体由蓝色变白色
C.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀
D.将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成
已知一个SO2分子的质量是a克,一个SO3分子的质量是b克,若以硫1/100作为标准,则SO2的摩尔质量是( ) g/mol
A. 100a/(b—a) B.l00a/(3a-2b) C. l00b/(3a-2b) D.l00a/(3b-2a)
下列电子式中,书写正确的是( )

设阿伏加德罗常数的数值为NA,下列说法正确的是( )
A.0.2 molCH4分子所含质子数为2NA
B.24 g金属镁变为镁离子时失去的电子数为NA
C.含有NA 个氦原子的氦气在标准状况下的体积约为11.2L
D.标准状况下,11.2 L CCl4 所含分子数为NA
A. 30g冰醋酸和葡萄糖的混合物中含氢原子的数目为2NA
B. 在12. 0 gNaHSO4晶体中,所含离子数目为0.3NA
C. 足量的镁与浓硫酸充分反应,放出 2.24L混合气体时,转移电子数为0.2NA
D. 标准状况下,11.2L乙烯和丙烯混合物中含氢原子数目为2NA
- 眼球内有感光细胞的结构是( )A.角膜 B.巩膜 C.脉络膜 D.视网膜
- 已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4 = 2CuI↓+13I2+12K2SO4+12H2O;其
- 如图,焦点在x轴上的椭圆+=1的离心率e=,F,A分别是椭圆的一个焦点和顶点,P是椭圆上任意一点,则·的最大值为____
- 4.下列各句中,没有语病的一项是 ( ) A
- 根据短文内容和所给中文提示写单词,每空一词。 Full Moon, Full Feelings Chinese pe
- Will you _____ the clock? It’s slow. A. adjust B. f
- 居里夫人曾经说过:“我从来不曾有过幸运,将来也永远不指望幸运……我激励自己,用尽所有的力量应对一切……我的毅力终于占了上
- 煮鱼时加些酒,能使甲胺溶于乙醇并随加热后挥发逸去,经过这样烹饪的鱼就不再有腥味了。下列过程与上面所述原理不相似的是 (
- 生活中的一些问题常涉及化学知识,下列叙述正确的是() A.棉花的主要成分是纤维素 B.过多食用糖类物质如淀粉等不会致人发
- 某省有一位全国人大代表,为方便同选民的沟通,设立了自己的全国人大代表联系点,并且通过电视广告向选民征集议案,这种做法在国
- 动漫产业是我国的新兴产业,作为我国动漫产业的杰出作品《喜羊羊与灰太狼》正是通过导演的合理想象,博得千千万万小朋友的喜爱。
- 下列有关①②处共同点的描述正确的是( )A.都可以无限量地吸收 B.都需要供给AT
- 2005年黔东南州实施“粮食增产工程”,引进适宜本地种植的高产优质稻种,实施旱育浅植等增产技术,亩产比往年增收粮食近20
- 反应 A+B → C的反应速率方程式为:v = k c(A) c (B), v为反应速率, k为速率常数。当c (A)
- 已知An+、B(n+1)+、Cn-、D(n+1)-都有相同的电子层结构 ,则A、B、C、D的原子半径由大到小的顺序是A.
- 关于转运RNA和氨基酸之间相互关系的说法,正确的是() A.每种氨基酸都可由几种转运RNA携带 B.每种氨基酸都有它特定
- 一位一辈子从事文艺工作的前辈用“四有”概括自己对工作、对人生的态度和坚守,即胸有大业,腹有诗书,肩有担当,术有专攻。这对
- 如图所示,小明分别用甲、乙两滑轮把同一桶沙从一楼地面提到二楼地面,通常情况下用甲滑轮人拉绳的力为F1,所做的总功为W1,
- 在英国君主立宪制的建立过程中,1701年颁布的嗣位法发挥了重要作用。该法规定,国王所作的任何决定必须由同意该决定的大臣签
- 对人体完成某一动作(如屈肘)的叙述中,错误的是() A.必须有肌肉收缩 B.必须有肌肉舒张 C.必须有神经支配 D



