高中 化学
-
(1) 已知分子式为C6H6的烃结构有多种,其中的两种为

①下列反应中Ⅰ能(填字母)而Ⅱ不能。
a.被酸性高锰酸钾溶液氧化 b.与溴水发生加成反应
c.与液溴发生取代反应 d.在空气中可以燃烧
②1 mol 物质与H2加成时, Ⅰ 需H2mol,而 Ⅱ 需H2mol。
③Ⅰ的一氯取代产物有种,Ⅱ的二氯取代产物有种

-
(2) 今发现C6H6还可能有另一种立体结构(如图所示),该结构的二氯代物有种。
-
(3) 下列四种芳香烃中,属于苯的同系物的是


-
(4) 现代化学认为苯分子中碳碳之间的键是。

工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。试回答下列问题:
-
(1) 装置B的作用是;B中发生反应的化学方程式是。
-
(2) 装置C中的物质是;C的作用是。
-
(3) 点燃氢气前将E(带导管胶塞)接在D出口处,目的是。
-
(4) 装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是。
 CH2═CH2↑+H2O
C . 丙烯聚合成聚丙烯的化学方程式:nCH2=CHCH3
CH2═CH2↑+H2O
C . 丙烯聚合成聚丙烯的化学方程式:nCH2=CHCH3 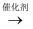
 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
-
(1) 该反应的逆反应为热反应,且m+np(填“>”“=”“<”).
-
(2) 减压时,A的质量分数.(填“增大”“减小”或“不变”,下同)
-
(3) 若加入B(体积不变),则A的转化率.
-
(4) 若升高温度,则平衡时B、C的浓度之比将.
-
(5) 若加入催化剂,平衡时气体混合物的总物质的量.


请回答下列问题:
-
(1) 将A点燃后伸入到装有E的集气瓶中,可观察到的现象是.
-
(2) C的浓溶液与黑色粉末反应生成E的化学方程式为.
-
(3) 若将溶液Ⅱ滴入到碘化钾溶液中,发生反应的离子方程式为,向反应后的溶液中加入适量CCl4 , 充分振荡后静置,可以观察到的现象是.
-
(4) 与溶液Ⅰ比较,溶液Ⅱ中多出的物质是(填化学式).

 该物质与
该物质与  溶液反应,最多消耗
溶液反应,最多消耗 
核糖是合成核酸的重要原料,其结构简式为CH2OH—CHOH—CHOH—CHOH—CHO,下列关于核糖的叙述中,正确的是( )
A.与葡萄糖互为同分异构体
B.可以与银氨溶液作用形成银镜
C.与葡萄糖互为同系物
D.可以使石蕊试液变红
已知下列两个反应:
① 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ + 4H2O
②3Cu2S + 22HNO3 = 6Cu(NO3)2 + 3H2SO4 + 10NO↑ + 8H2O
试回答下列问题:
(1)反应①中_________________(填化学式)作氧化剂;Cu发生________________(填“氧化”或“还原”)反应;用双线桥表示出反应①的电子转移方向和数目____________。
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ + 4H2O
(2)将反应②改写为离子方程式___________________________(提示:Cu2S不溶于水)
(3)反应②中Cu2S中Cu的化合价为______;___________(填元素符号)元素被氧化,还原产物为_____________。
(4)当反应②中生成2.24L(标准状况下)NO气体,消耗HNO3的质量为__________g,其中有_________mol HNO3被还原,共转移电子_________mol。
已知在相同状况下,要使同一化学键断裂需要吸收的能量等于形成该化学键放出的能量。下列说法正确的是…………………..………………………………..…………..…( )
A、 电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应
B、 水分解产生氢气和氧气时放出能量
C、 相同状况下,反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应
D、氯化氢分解成氢气和氯气时需要吸收能量
对于![]()
![]() 溶液与铁片的反应,采取下列措施能使反应速率加快的是:
溶液与铁片的反应,采取下列措施能使反应速率加快的是:![]() 升高温度;
升高温度;![]() 改用
改用![]()
![]() 溶液;
溶液;![]() 改用
改用![]()
![]() 溶液;
溶液;![]() 用等量铁粉代替铁片;
用等量铁粉代替铁片;![]() 改用
改用![]()
![]()
![]() 溶液
溶液
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 = 2NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
A.431 kJ/mol B.946 kJ/mol C.649 kJ/mol D.869 kJ/mol
香叶醇是合成玫瑰香油的主要原料,其结构简式如下: 下列有关香叶醇的叙述正确的是( )

A. 香叶醇的分子式为C10H18O
B. 不能使溴的四氯化碳溶液褪色
C. 不能使酸性高锰酸钾溶液褪色
D. 能发生加成反应不能发生取代反应
- 写作(60分)请以“ 的我”为题,写一篇作文。要求:⑴先把题目补充完整,然后作文;⑵字数不少于600。
- 一位同学在测质量时,在天平右盘里无论怎样加减砝码都不能使横梁平衡,下列方法中正确的是:A.交换左右托盘B.旋动平衡螺母C
- I can never forget the day ________ we worked together and t
- What a wonder! They’ve finished _________half of the project
- (本小题满分15分)已知A(1,1)是椭圆上一点,F1,F2,是椭圆上的两焦点,且满足(I)求椭圆方程; (Ⅱ)设C,
- 我们的共和国已经走过了60年的风雨历程,回首来路,我们心潮起伏。请以“国庆60年”为话题写一段文字。要求所写句子包含比喻
- 右侧漫画的哲学寓意是 A.必须在改造主观世界的同时,改造客观世界 B.必须坚持适度原则 C.必须牺牲个人利益去维护人
- 已知⊙O1、⊙O2的半径分别是、,若两圆相交,则圆心距O1O2可能取的值是……………………………………………………………
- 历史是复杂的。有时吸取前人的历史教训会导致新问题的产生。下列史实能佐证这—看法的是( ) A.秦二世而亡,汉推行郡
- (湖北省钟祥六中2009年高三高考冲刺最后一卷) My son was badlyhurt in a fire. Af
- 当前珠江三角洲水资源状况主要面临干旱、洪涝、水环境恶化三大问题,关于珠江三角洲水资源的叙述正确的是 A.水资源总量少时造
- 已知全集U={l,2,3·4,5,6,7},A={2,4,5),则= A.{1,3,5,6,7} B.
- 我国面积最大的盆地是: A.四川盆地 B.柴达木盆地 C. 准噶尔盆地 D.
- 下列关于硅单质及其化合物的说法正确的是 ①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐
- MrsChen is paper-cuttingexpert, whom I interviewed f
- 某班同学在表演井冈山会师的情景剧时,下列人物中可能出现的有( ) ① ②朱德
- 在搭建DNA分子模型的实验中,若有4种碱基塑料片共20个,其中4个C,6个G,3个A, 7个T,脱氧核糖和磷酸之间的连接
- 小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧,于是设计了如图所示的装置进行实验探究,请你结合实验过程回答下
- (2011年厦门模拟)在实际生活中常常有这样的一种情况出现,即人们对某种事物的存在与否感到难以预料,心中无底时,往往就认
- 下列叙述正确的是( ) A.1 mol H2O的质量为18g/mol B.CH4的摩尔质量为16g



