高三化学试题
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO![]() 、Cl-
、Cl-
B.()![]() =1×10-13 mol·L-1的溶液中:NH
=1×10-13 mol·L-1的溶液中:NH![]() 、Ca2+、Cl-、NO
、Ca2+、Cl-、NO![]()
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO![]() 、SO
、SO![]()
D.水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、[Al(OH)4]-、CO![]()
利用下列实验装置能达到相应实验目的的是
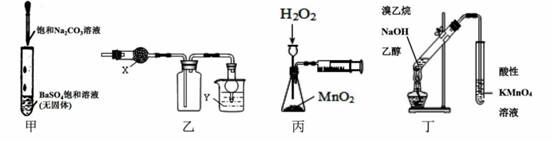
A.甲可用于研究沉淀的转化,可比较出Ksp(BaSO4)>Ksp (BaCO3)
B.乙中X为无水CaCI2,Y为NaOH溶液时,该装置可用于SO2的收集
C.丙装置可定量测定H2O2的分解速率
D.丁可用于证明实验中生成了乙烯
研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列判断中正确的是( )

A.用装置①模拟研究时未见a上有气泡产生,说明铁棒没有被腐蚀
B.②中桥墩与外加电源正极连接能确保桥墩不被![]() 腐蚀
腐蚀
C.③中采用了牺牲阳极的阴极保护法保护桥墩
D.①②③中海水均是实现化学能转化为电能的电解质
利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)甲烷与水蒸气反应,被氧化的元素是____________(元素符号作答),当生成标准状况下35.84 L合成气时转移电子的物质的量是________。
(2)将2 mol CH4和5 mol H2O(g)通入容积为10 L的反应室,CH4的平衡转化率与温度、压强的关系如图所示。
 ①若达到A点所需的时间为5 min,
①若达到A点所需的时间为5 min,
则v(H2)=____________________,
②图中的p1______p2(填“<”“>”或“=”),
A、B、C三点的平衡常数KA、KB、KC的大小关系是_______。
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0,下列措施中能使
CO2(g)+H2(g) ΔH<0,下列措施中能使![]() 增大的是________(选填编号)。
增大的是________(选填编号)。
A.降低温度 B.恒温恒容下充入He(g)
C.将H2从体系中分离 D.再通入一定量的水蒸气
已知氧化性:Br2>Fe3+>I2;还原性:I﹣>Fe2+>Br﹣,则下列反应能发生的是( )
|
| A. | I2+2Fe2+═2Fe3++2I﹣ | B. | 2Br﹣+I2═Br2+2I﹣ |
|
| C. | 2Fe3++2I﹣═2Fe2++I2 | D. | 2Fe3++2Br﹣═2Fe2++Br2 |
下列化学反应先后顺序判断正确的是( )
A.在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I—、Br—、Fe2+
B.在含有等物质的量的NaOH、Ca(OH)2 、NaAlO2 的溶液中通入CO2气体:NaOH、Ca(OH)2 、
NaAlO2
C.在含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH溶液:H+、A13+、Al![]() (OH)3
(OH)3
D.在含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉:Cu2+、Fe3+
化学与生产、生活密切相关。下列说法错误的是
A.二氧化氮能使织物褪色,对金属材料也有腐蚀作用
B.纯碱是制作面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂
C.“水滴石穿”是因为CaCO3与CO2、水发生了化学反应
D.因为氨易液化,在汽化时会吸收大量的热量,所以可作制冷剂
乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。
将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌
洛托品,则甲醛与氨的物质的量之比为
A.1∶1 B.2∶3 C.3∶2 D.2∶1
设NA为阿伏加德罗常数的数值,下列叙述中正确的是( )
A.2molSO3一定条件下充分分解得到的产物分子的数目为3NA
B.一定量的无水乙醇与足量钠反应生成5.6LH2,则乙醇分子中共价键总数为4NA
C.等物质的量的氯气分别与足量铁和铜完全反应,转移电子数均为2NA
D.标准状况下22.4L空气中含有的单质分子数目小于NA
钇(Y)元素是激光和超导的重要材料,常见化合价为+3价。我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。

已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
②在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。请回答下列问题:
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式表示为
(按YFeBeSi的氧化物顺序)
(2)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
①最好选用盐酸和两种试剂,再通过必要的操作即可实现。
a. NaOH溶液b. 氨水c. CO2d. HNO3
Na2SiO3的水溶液的俗称是。
②写出Na2BeO2与足量盐酸发生反应的离子方程式
(3)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在范围内,检验Fe3+是否沉淀完全的操作方法是
二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
 |
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是___________________。
(2)滤液1中加入H2O2溶液的目的是_________________________________________________。
(3)某同学设计实验证明滤液1中含有Fe2+,他所用的试剂为___________________。
(4)已知溶液中的Fe2+可以和难溶于水的FeO(OH)反应生成Fe3O4,请书写该反应的离子方程式_____________________________________________________________________________。
(5)由滤液2生成Ce(OH)4的离子方程式______________________________________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理。相对于去除中性废水,其在去除酸性废水中的悬浮物时效率 (填“增强”或“降低”)。
(7)取上述流程中得到的C![]() e(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。
e(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。
该产品中Ce(OH)4的纯度为 。(保留两位有效数字)
 如图所示装置中,a、b、c、d、e、f均为惰性电极电解质溶液均足量。接通电源后,d 极附近显红色。下外说法正确的是
如图所示装置中,a、b、c、d、e、f均为惰性电极电解质溶液均足量。接通电源后,d 极附近显红色。下外说法正确的是
A.电源B 端是正极
B.f 极附近红褐色变深,说明氢氧化
铁胶粒带正电
C.欲用丁装置给铜镀银,N 应为Ag,
电解质溶液为AgNO3溶液
D.a、c电极均有单质生成它们的物质的量之比为2∶1
下列说法不正确的是
A.任何化学反应都伴有能量变化
B.化学反应中的能量变化不一定都表现为热量变化
C.反应物的总能量高于生成物的总能量时,发生的是放热反应
D.任何放热反应在常温下一定能发生反应
(1)请在下图所示分子的结构简式中用“*”标记出手性碳原子。若用该有机物进行核磁共振实验,所得核磁共振氢谱有________个峰,强度比为________。

(2)已知某硼烷相对分子质量为28,核磁共振氢谱有两个峰且强度比为1∶2,则该硼烷的分子式是________,已知该硼烷气体在空气中能剧烈燃烧生成三氧化二硼和水,且生成1 mol液态水可放出722 kJ的热量,请写出燃烧的热化学方程式:____________________________。
短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:① R、Y原子的最外层电子数与电子层数相同;② Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;③ W与R同主族。下列说法正确的是
A.元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型
B.元素T、Q、W、Y的原子半径大小为:T<Q<Y<W
C.Q与Y组成的常见物质是一种两性物质,结构中含有共价键
D.由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成
下列实验表述正确的是

A.图l:用于制取纯净的NO2气体 B.图2:用于研究温度对化学平衡的影响
C.图3:用于实验室Cl2的收集 D.图4:用于除去CO2气体中的HCl杂质
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如下的转化关系(部分产物及反应条件已略去),下列判断正确的是( )

A.X元素可能为Al
B.X元素不一定为非金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
综合利用CO2、CO对构建低碳社会有重要意义。
(1) Li4SiO4可用于富集得到高浓度CO2。原理是:在500℃,低浓度CO2与Li4SiO4接触后生成两种锂盐;平衡后加热至700℃,反应逆向进行,放出高浓度CO2,Li4SiO4再生。700℃时反应的化学方程式为____。
(2) 固体氧化物电解池(SOEC)用于高温共电解CO2/H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如图。写出电极c发生的电极反应式:___________、_____________ 。

(3) 电解生成的合成气在催化剂作用下发生如下反应:CO(g)+2H2(g)⇌CH3OH(g)。对此反应进行如下研究:某温度下在一恒压容器中分别充入1.2 mol CO和1 mol H2,达到平衡时容器体积为2 L,且含有0.4 mol CH3OH(g)。此时向容器中再通入0.35 mol CO气体,则此平衡将_____(填“向正反应方向”“不”或“向逆反应方向”)移动。
(4) 已知:

若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)⇌CH3OH(l)的ΔH,则ΔH=_____。
(5) 利用太阳能和缺铁氧化物可将廉价CO2热解为碳和氧气,实现CO2再资源化,转化过程如图所示,若用1 mol缺铁氧化物与足量CO2完全反应可生成______mol C(碳)。

溶液X中只可能溶有K+、Mg2+、Al3+、AlO![]() 、SiO
、SiO![]() 、SO
、SO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种离子。某同学对该溶液进行了如下实验。则下列判断正确的是( )
中的若干种离子。某同学对该溶液进行了如下实验。则下列判断正确的是( )
 A.气体甲一定是纯净物 B.沉淀甲是硅酸和硅酸镁的混合物
A.气体甲一定是纯净物 B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO![]() 和SiO
和SiO![]() 一定存在于溶液X中 D.CO
一定存在于溶液X中 D.CO![]() 和SO
和SO![]() 一定不存在于溶液X中
一定不存在于溶液X中
草酸晶体(H2C2O4•2H2O)无色,易溶于水,熔点为101℃(失水后能升华),170℃以上分解。其钠、钾、铵盐均易溶于水,而钙盐难溶于水.某实验探究小组对草酸晶体进行加热,并验证其分解产物.
 (1)加热草酸晶体最适宜选用图1中的 (填装置编号),不选其它装置的原因是 _________
(1)加热草酸晶体最适宜选用图1中的 (填装置编号),不选其它装置的原因是 _________
(2)若将产生的气体直接通入澄清石灰水来检验分解产物中是否含CO2,请你评价正确与否并作简要的解释________________________________________________________。
(3)用图2装置检验草酸的分解产物H2O(g)、CO2和CO.将这种混合气体依次通过___________(填装置中接口的字母,可重复使用)。
(4)能否依据硬质玻璃管Fe2O3质量的减轻来计算分解产生CO的量?_____。假设硬质玻璃管中所装为铁氧化物的混合物,可能是FeO、Fe2O3、Fe3O4的任意组合,现取ag混合物充分反应后,质量减轻了8a/29克,通过计算确定该混合物中三种氧化物的物质的量的关系为____________。
(5)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。

(6)有同学设计图3装置来证明Fe2O3反应后的固体中含有单质铁,你认为可行吗?________;其原因是:_____________________;图3中安全漏斗的作用是____________________。
(7)设计一个简单的实验证明草酸是弱酸:_____________________________________。
- 下面是某同学根据收集到的资料绘制的图表。请仔细观察并比较两组数据,用简明的语言概括出图表所包含的信息。(4分)
- 如图所示,该小组发现8米高旗杆DE的影子EF落在了包含一圆弧型小桥在内的路上,于是他们开展了测算小桥所在圆的半径的活动.
- 在原子中含有 个质子, 个中子;它的原子结构示意图为 。铁在氯气中燃烧,生成
- 质量为M的物体放在倾角为α的斜面上时,其重力在沿斜面方向的分力大小为________,在垂直于斜面方向的分力大小为___
- 我国政府领导人在许多重要场合谈到我国的对外方针时,都强调我国坚持走和平发展道路。坚持走和平发展道路是我国唯一正确的选择。
- 质量相等的甲、乙两同学站在滑板上,在旱冰场上相对而立,如果甲用60N的力推乙,如图所示。以下分析正确的是【 】
- Where did you meet him while in Beijing?--It was in the hote
- 狼体内有A种蛋白质,20种氨基酸;兔体内有B种蛋白质,20种氨基酸。狼捕食兔后狼体内的一个细胞中含有的蛋白质种类和氨基酸
- 若a、b是两条异面直线,且分别在平面α、β内,若α∩β=l,则直线l必定( )A.分别与a、b相交
- 在奥运比赛项目中,高台跳水是我国运动员的强项。质量为m的跳水运动员进入水中后受到水的阻力而做减速运动,设水对他的阻力大小
- 9.下列句中加点词的词类活用都属于名词作动词的一组是( ) ①既东封郑 ②发尽上指冠 ③沛公欲王关中
- Last month, I (33)_______(return) to Australia to attend my
- CPI是用于衡量某一固定消费品集合价格水平的指数,CPI越大,表明物价越高。下表列出了某年份我国三个城市的人均工资与CP
- 将H2、CO、CO2、N2依次通过足量下列物质:澄清石灰水、灼热的氧化铜、浓H2SO4(注:有吸水性),最终剩余的气体为
- 下列各选项中加线字的解释有误的一项是( ) A.淇水汤汤,渐车帷裳 《诗经·氓。》 (shāng水大流急的样
- 当代环境问题,主要是由人类污染造成的,如巨大的人口压力、自然资源的不合理利用、片面追求经济增长速度等,都是产生环境问题的
- 法国艺术家贝纳尔创作的装置艺术作品,通过64张占卜牌随机抽取法文字母,不规则地布置电子元件的位置,以闪烁的字母重现“在世
- “在欧洲……的一种文艺思潮和艺木流派……反对学院派的保守,主张到大自然中去写生,直接获取光与色的无穷变化以作艺术表现…
- 小莉的妈妈一直注意给她加喂钙粉,可医生还是诊断小莉缺钙,原因是在服用钙粉时没有补充()A. 维生素A B. 维生素B C
- .晚清维新派代表人物梁启超等人在上海创办“不缠足会”,规定“凡入会人所生女子,不得缠足”“凡入会人所生男子,不得娶缠足之



