高三化学试题
设nA为阿伏加德罗常数,下列说法正确的是
A.常温下,28g C2H4含nA个碳碳双键
B.1 mol Cu和足量稀硝酸反应生成nA NO分子
C.常温常压下,22.4L CCl4含有n A个CCl4分子
D.1mol/L NaCl溶液含有n A个Na+
为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | NaBr溶液(NaI) | 氯水、CCl4 | 萃取、分液 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | CO2(CO) | CuO粉末 | 通过灼热的CuO粉末 |
| D | SiO2(Al2O3) | NaOH溶液 | 过滤 |
6.4g 铜与一定量硝酸充分反应后,硝酸的还原产物是NO,反应后溶液中所含 H+为 n mol,此时溶液中所含 NO3-物质的量为( )
| A. 0.28 mol | B. 0.31 mol | C. (n+0.2)mol | D. (n+0.4)mol |
P轨道电子云形状正确的是
A.球形对称 B.圆形对称
C.极大值在x、y、z轴上的纺锤形 D.互相垂直的花瓣形
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL 稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀 H2SO425mL,滴定终止时消耗NaOH溶液15mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25 mL,注入锥形瓶中,加入指示剂。
B.用待测的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终点? 。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) 。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度为 mol/L (计算结果保留两位小数)
NA表示阿伏加德罗常数,下列叙述正确的是
A.等物质的量的N2和CO所含分子数均为NA
B.1.7g H2O2中含有的电子数为0.9 NA
C.1mol Na2O2 固体中含离子总数为4 NA
D.标准状况下,2.24L戊烷所含分子数为0.1 NA
电子产品产生的大量电子垃圾对环境构成了极大的威胁。某化学兴趣小组将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

按要求回答下列问题:
(1)滤渣1中存在的金属有____________。
(2)已知沉淀物的pH如下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
①则操作②中X物质最好选用的是___________(填编号)
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是________________________。
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是____________________。
(4)用一个离子方程式表示在酸浸液中加入适量铝粉的反应:___________________。
(5)由CuSO4·5H2O制备CuSO4时,应把CuSO4·5H2O放在 (填仪器名称)
中加热脱水。
(6)现在某些电器中使用的高铁电池是一种新型可充电电池,与普通高能电池相比,该
电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O![]() 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,该电池放电时负极反应式为 ,每有1mol K2FeO4被还原,转移电子的物质的量为 ,充电时阳极反应式为 。
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,该电池放电时负极反应式为 ,每有1mol K2FeO4被还原,转移电子的物质的量为 ,充电时阳极反应式为 。
下列离子方程式与所述事实相符且正确的是( )
A.向FeBr2溶液中通入过量的Cl2:2Fe2+![]() +2Br-+2Cl2===2Fe3++Br2+4Cl-
+2Br-+2Cl2===2Fe3++Br2+4Cl-
B.用食醋除去水壶内的水垢:CaCO3+2H+ = Ca2++CO2↑+H2O
C.KHCO3与足量澄清![]() 石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+
加热蒸干氯化镁溶液时因水解不完全会得到一种灰白色沉淀——碱式氯化镁,化学式可表示为Mgx(OH)yClz·nH2O,设计如图所示装置验证其化学式。下列有关实验的说法不正确的是( )。

A.①②中依次盛装浓硫酸、氢氧化钠溶液
B.反应结束时,先停止加热,通一段时间N2后再关闭活塞K
C.碱式氯化镁受热分解可以产生氧化镁、氯气和水
D.只需称取原样品质量、反应结束后硬质玻璃管中剩余固体质量以及装置①增加的质量即可推出其化学式
关于下列各装置图的叙述不正确的是( )

① ② ③ ④
A.用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液
B.图②装置的盐桥中KCl的Cl—移向甲烧杯
C.图③装置中钢闸门应与外接电源的正极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
下列实验中金属或金属氧化物可以完全溶解的是
A.常温下将64g铜片投入过量浓盐酸中
B.向100.0mL 3.00mol/L的稀硝酸中加入5.6g铁
C.1 mol MnO2粉末与含4molHCl的浓盐酸共热
D.常温下1 mol铝片投入20.0mL 18.40mol/L硫酸中
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是
A.物质的量之比为1:1 B.体积之比为11:16
C.氧原子数之比为1:1 D.密度之比为11:16
党的十八大报告提出了“建设美丽中国”的宏伟蓝图。节能减排、低碳生活、合理利用资源、保护环境,走可持续发展的道路成为我国发展的重要战略。下列说法不符合这一主题思想的是( )
A.大力开采我省陇东地区的煤和石油,促进地方经济发展
B.实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染
C.积极推广太阳能、风能、地热能等新能源的使用,减少化石燃料的使用,有效降低PM2.5对环境的污染
D.对城市生活污水脱氮除磷、净化处理,遏制水体富营养化
短周期主族元素W、X、Y、Z在周期表中的位置如图所示。下列说法正确的是
A.原子半径:W>X>Y
B. W、X、Y不能存在于同一离子化合物中
C.最简单气态氢化物的稳定性:W<Z
D. X、Y、Z的最高价氧化物对应的水化物两两之间均能发生反应
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)⇌CH3OH(g).
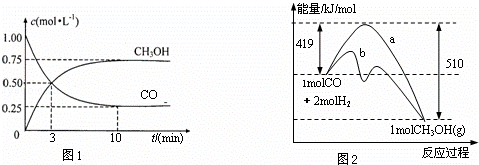
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是 (选填“吸热”或“放热”)反应,写出反应的热化学方程式 .
(3)该反应平衡常数K为 ,温度升高,平衡常数K (填“增大”、“不变”或“减小”).
(4)恒容条件下,下列措施中能使![]() 增大的有 .
增大的有 .
a.升高温度 b.充入He气
c.再充入2molH2 d.使用催化剂.
对于合金的说法,正确的是
A.常见的铜合金是青铜和黄铜 B.合金与各组分金属相比具有更低的熔点
C.钢是铁和碳的合金,生铁则是纯铁 D.合金与各组分金属相比具有更大的硬度
【答案】ABD
【解析】
试题分析:C选项中,生铁和钢都含有碳元素
考点:合金的相关知识
点评:本题考查的是合金的相关知识,合金与各组分金属相比,具有更低的熔点和更高的硬度,需要注意的是,生铁并不是纯铁,而是合金
5.下列各组物质发生化学反应时,由于反应物的量不同而生成不同产物的是
①CO2与NaOH溶液 ②NaHCO3溶液与盐酸 ③Na与氧气
④C与O2 ⑤AlCl3溶液与氨水 ⑥Na2S与FeCl3溶液
A.除③外 B.除①④⑥外 C.除②③⑤外 D.除②⑤外
已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5.0×10-13。该温度下,下列说法错误的是:
A.AgCl的悬浊液中通入少量HCl,c(Ag+)减小
B.AgCl和AgBr共存的悬浊液中,![]()
C.AgBr悬浊液中加入足量NaCl可能有AgCl沉淀生成
D.等浓度的NaCl和NaBr混合溶液中滴加AgNO3溶液,先析出AgCl沉淀
某种一元弱碱BOH的相对分子质量为M。在一定温度下将此碱ag完全溶解于水,配成VmL饱和溶液,测得此溶液的密度为dg·cm-3,B+为bmol,则在此温度下,下列算式中不正确的是 ( )
A.溶解度为![]() g B.此溶液中溶质的质量分数为
g B.此溶液中溶质的质量分数为![]() ×100%
×100%
C.电离度为![]() ×100% D.此弱碱溶液的浓度为
×100% D.此弱碱溶液的浓度为![]() mol·L-1
mol·L-1
下列叙述或书写正确的是
A. H2(g)+F2 (g)===2HF(g) △H=-270 kJ·mol -1,则相同条件下,2mol HF气体的能量大于1mol氢气和1mol氟气的能量之和
B. 2H2(g)+O2(g)===2H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热大于241.8kJ.mol-1
C. 含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该中和反应的热化学方程式为NaOH+HCl===NaCl+H2O △H =-57.4kJ·mol-1
D. 500℃、30MPa时,发生反应N2(g)+3H2(g) ![]() 2NH3(g) △H =-38.6kJ·mol-1在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ
2NH3(g) △H =-38.6kJ·mol-1在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ
I.制备水杨酸对正辛基苯基酯(![]() )如下:
)如下:
步骤一:将水杨酸晶体投入到三颈烧瓶中,再加入适量的氯苯作溶剂并充分搅拌使晶体完全溶解,最后加入少量的无水三氯化铝。
步骤二:按右图所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。

该反应方程式为:
![]()
步骤三:将三颈烧瓶中混合液升温至80℃,再加入对正辛苯酚[![]() ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥即得产品。
(1)实验时,冷凝管中的冷却水进口为 _______(选填“a”或“b”);
(2)步骤一中加入无水三氯化铝的作用是 ____________。
(3)步骤三中发生反应的化学方程式为 ________________________________________。
II.PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 | |
| 白磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
已知右图是实验室制备PCl3的装置(部分仪器已省略),则:

(1)实验室制备Cl2的离子反应方程式为:______________________________________。
(2)碱石灰的作用除了防止空气中的O2和水蒸气进入并与产品发生反应外还有:____________________________________。
(3)向仪器甲中通入干燥Cl2之前,应先通入一段时间的干燥CO2,其目的是_________________________________________________________。
(4)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过________(填实验操作名称),即可得到PCl3的纯品。
(5)测定产品中PCl3纯度的方法如下:迅速称取m g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1 mol/L V1 mL 碘溶液,充分反应后再用c2 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗V2 mL Na2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6
假设测定过程中没有其他反应,则根据上述数据,求出该产品中PCl3的质量分数为 ___________________________________________(用含字母的代数式表示、不必化简)。
- 观察下面两种政治体制的图示,这两种政治体制的相同点不包括A.都反映了中央各部门的构成 B.都实行分权 C.都顺应
- 我国当前实行的省制开端于( ) A.秦朝的郡县制 B.西汉的州郡县制 C.唐朝的军镇制 D.元朝的行省制
- 下列关于生态系统信息传递特征的描述,不正确的是 A.信息可沿食物链进行双向传递 B.植物可通过化学物质传递信息 C.生态
- 车尔尼雪夫斯基说:“真理之所以为真理,只是因为它是和谬误以及虚伪对立的。”这句话告诉我们A.真理只有一个,真理面前人人平
- 已知抛物线C:y2=8x与点M(-2,2),过C的焦点且斜率为k的直线与C交于A、B两点,若=0,则k=() A.
- 随着社会主义核心价值体系建设的推进,浙江“最美妈妈”、“最美司机”、“最美教师”、“最美警察”等“最美人物”不断涌现。他
- 书面轻翻,心旌微摇。叹梁祝身化彩蝶,喜崔张终成眷属,羡东坡把酒临风,慕清照泛舟浩淼。高山流水鸣于耳畔,瘦菊幽兰馨于鼻尖。
- 一个做自由落体运动,最后1s通过的位移为全程的19%,求其下落的高度?
- 已知椭圆上的一点P,到椭圆一个焦点的距离为3,则P到另一焦点距离为____________.
- 如图,在Rt△ABC中,∠BAC=90°,AC=2AB,点D是AC的中点,将一块锐角为45°的直角三角板如图放置,使三角
- 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正
- -----May I ________ your English-Chinesedictionary?
- 等比数列的前项和为,已知,,成等差数列 (I)求数列的公比; (II)若-=3,求
- (多选)在远距离输电时,输送的电功率为P,输电电压为U,所用导线电阻率为ρ,横截面积为S,总长度为L,输电线损失的电功率
- 对于N2(g)+3H2(g)⇌2NH3(g)△H<0的反应,达到化学平衡状态的标志为() A.断开1个N≡N键的同时有6
- 子曰:“岁寒,____________。”(《论语·子罕》)
- 方程(t为参数)的图形是()A.双曲线左支B.双曲线右支C.双曲线上支D.双曲线下支
- 北京奥运会开幕式呈现给世界一场精彩绝伦的视觉盛宴。书画汉字、丝绸之路等“中国元素”淋漓尽致地展现了中国深厚的文化。如图中
- 正常男性产生的精子中,非同源染色体的组合最多有多少种(不考虑同源染色体的互换)? A.23 B.223
- 秋窗日午,小院无人,抱膝独坐,聊嫌枯寂,宜读《庄子》秋水篇。大雪漫天,炉火小坐,人缩如猬,豪气欲销,宜读《水浒传》林冲走



