高三化学试题
氯气是氯碱工业的主要产品之一,常作强氧化剂,可与有机物和无机物进行反应生成多种氯化物。某兴趣小组在实验室中对以下反应进行了探究。回答下列问题:
Ⅰ、三氯化硼(BCl3)的制备,已知:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃; ②2B+6HCl ![]() 2BCl3↑+3H2↑。
2BCl3↑+3H2↑。

(1)按气流方向连接各装置的接口,顺序为a→( )→( )→( )→( )→( )→( )→f→g→h。
(2)装置D的作用是 ;实验中若不用装置C,可能产生的危险是 。
(3)BCl3遇水发生水解观察到大量的白雾,生成两种酸,其反应的化学方程式为: 。
Ⅱ、SO2与漂粉精溶液的反应
| 操作 | 现象 |
| 取4g 漂粉精固体,加入100mL 水,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
|
| 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(4)pH试纸颜色的变化说明漂粉精溶液具有的性质是 。
(5)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl- 发生反应。该反应的离子方程式为 。
(6)用离子方程式解释现象3中黄绿色褪去的原因 。
一种用硫酸烧渣(主要成分Fe2O3、FeO、Fe3O4、FeS2、SiO2)制备铵黄铁矾[(NH4)xFey(SO4)z(OH)n,其中Fe为+3价]的工艺流程如下:
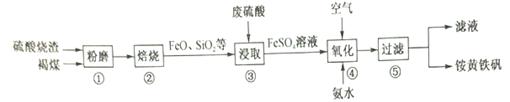
回答下列问题:
(1)焙烧前需进行“粉磨”的目的是 ;硫酸烧渣加褐煤高温焙烧的主要目的是 。
(2)“焙烧”的温度与“浸取”时浸出率的关系如下图1所示,超过800℃时,浸出率开始降低,其原因是
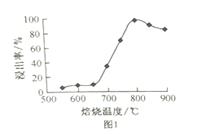
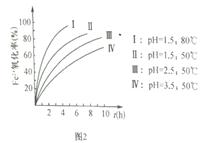
(3)步骤④Fe2+的氧化率随控制条件及时间的变化关系如上图2所示,适宜的条件为 (选填I、II、III、IV)。从滤液中可回收的产品是 (填化学式)。
(4)为测定产品铵黄铁矾的化学式,进行以下实验:
步骤1:取19.2 g铵黄铁矾,加足量的稀盐酸溶解,将所得溶液分为A、B两等份;
步骤2:向A中加入足量的NaOH溶液并加热,共收集到0.448L NH3(标准状况下)过滤后将所得滤渣洗涤干燥并灼烧至质量不再变化,可得1 8 g固体残渣;
步骤3:向B中加人足量的BaCl2溶液,过滤洗涤干燥,可得9. 32 g固体残渣。
则产品铵黄铁矾的化学式为 。
下列说法可以实现的是 ( )
① 酸性氧化物均能与碱发生反应,
② 弱酸与盐溶液反应可以生成强酸,
③ 发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成,
④ 两种酸溶液充分反应后,所得溶液呈中性,
⑤ 有单质参加反应,但该反应不是氧化还原反应,
⑥ 两种氧化物发生反应有气体生成
A.①②③④⑤⑥ B.①③⑤⑥
C.①②③⑤ D.③⑤
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成,经查资料得知:
Ag++2NH3•H2O![]() Ag(NH3)2++2H2O下列分析不正确的是
Ag(NH3)2++2H2O下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
B.实验表明实验室可用氨水洗涤银镜反应后的试管
C.实验可以证明NH3结合Ag+能力比Cl--强
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g) ΔH=Q kJ·mol−1。在T1℃时,反应进行到不同时间(min) 测得各物质的浓度(mol·L−1)如下:
| 时间 浓度 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是______(填字母)。
a.通入一定量的NO
b.加入定量的活性炭
c.加入合适的催化剂
d.适当缩小容器的体积
②若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3∶1∶1,则Q________(填“>”或“<”)0。
(2)某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应:2NO+2CO⇌N2+2CO2(有CO);2NO⇌N2+O2(无CO)

①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为_______________
___________________________________________________________;在n(NO)/n(CO)=1的条件下,应控制最佳温度在____________左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染,写出C2H6与NO2发生反应的化学方程式:___________________________________________________。
③以NO2、O2、熔融NaNO3组成的燃料电池装置如下图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电极反应式为________________________________________。

(3)天然气的一个重要用途是制取氢气,其原理如下:
已知:a.2CO(g)+O2(g)===2CO2(g) ΔH1
b.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH2
c.2H2(g)+O2(g)===2H2O(l) ΔH3
①科学家提出一种利用天然气制备氢气的方法:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=___________。
②这种方法的推广与使用,不仅实现资源综合利用,而且还能解决的环境问题是__________
________________________________________________。
丁烯(C4H8)是制备线性低密度聚乙烯(LLDPE)的原料之一,可由丁烷(C4H10)催化脱氢制备,C4H10(g)![]() C4H8(g)+H2(g)
C4H8(g)+H2(g) ![]() =+123kJ·mol-1。该工艺过程中生成的副产物有炭(C)、C2H6、C2H4、C4H6等。进料比[
=+123kJ·mol-1。该工艺过程中生成的副产物有炭(C)、C2H6、C2H4、C4H6等。进料比[![]() ]和温度对丁烯产率的影响如图1、图2所示。已知原料气中氢气的作用是活化固体催化剂。
]和温度对丁烯产率的影响如图1、图2所示。已知原料气中氢气的作用是活化固体催化剂。

下列分析正确的是
A. 随温度升高丁烯裂解生成的副产物增多,会影响丁烯的产率
B. 丁烷催化脱氢是吸热反应,丁烯的产率随温度升高而不断增大
C. 氢气的作用是活化固体催化剂,改变氢气量不会影响丁烯的产率
D. 一定温度下,控制进料比[![]() ]越小,越有利于提高丁烯的产率
]越小,越有利于提高丁烯的产率
下列说法错误的是
A.越王勾践剑(青铜)的铸造材料主要是铜锡合金
B.青花瓷制作原料的主要成分是硅酸盐
C.以毛竹为原料制作的竹纤维属于高分子材料
D.石墨烯是一种能导电的有机高分子材料
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
100mL 2mol/L的溴化钠溶液中通入一定量氯气后,将溶液蒸干得到固体16.15g。
求(1)通入的氯气在标况下的体积是多少 ?
(2)所得固体的成份及各自物质的量
下列各组混合物中,可以用分液漏斗分离的是
A.溴苯和水 B.乙酸和乙醇 C.酒精和水 D.溴苯和苯
化学与社会、科学、技术、环境密切相关。下列说法不正确的是
A.T-碳是一种新型三维碳结构晶体,与C60互为同素异形体
B.推广利用CO2合成聚碳酸酯可降解塑料符合低碳经济理念
C.将金属钛、铝混合后在空气中熔化可制得强度较大的钛合金材料
D.为汽车安装尾气催化转化装置,可将尾气中的部分CO和NO转化为无毒气体
一化工厂突发火灾,经消防支队全体官兵的奋力扑救,大火在2小时后被成功扑灭.起火原因经专家分析,是储存在该厂实验室的酒精由于管理不善,酒精滴漏到某种化学品上而酿成火灾.请你判断引起火灾的罪魁祸首的化学品可能是( )
|
| A. | 盐酸 | B. | 氯化钠 | C. | 碳酸氢钠 | D. | 高锰酸钾 |
下列指定反应的离子方程式正确的是( )
A.饱和Na2CO3溶液与CaSO4固体反应:CO32−+CaSO4![]() CaCO3+SO42−
CaCO3+SO42−
B.酸化NaIO3和NaI的混合溶液:I− + IO3−+ 6 H+![]() I2 + 3H2O
I2 + 3H2O
C.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3![]() 2FeO42−+3Cl−+4H++H2O
2FeO42−+3Cl−+4H++H2O
D.电解饱和食盐水:2Cl−+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
常温下,A是只含X和Y两种短周期元素的气体,X的原子序数小于Y,甲、乙、丙分别是X、Y、Z元素的单质,Z是地壳中含量最高的元素。甲、乙、丙和B、C、D都是常见的物质,其转化关系如图所示。下列说法正确的是

A.原子半径:Z>Y>X
B.反应②为化合反应,反应③为置换反应
C.常温常压下,Z的氢化物为气态
D.由X、Y、Z三种元素组成的化合物可能是离子化合物
设NA为阿伏加德罗常数.下列说法正确的是( )
A. 0.1 molFe和0.1molCu分别与0.1molCl2完全反应,转移的电子数均为0.2NA个
B. 4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA
C. 1 mol FeCl3 水解生成的Fe(OH)3胶粒数为NA
D. 64 g SO2与过量的O2在一定条件下反应生成的SO3分子数为NA
一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示。以下说法不正确的是

A.中间室Cl—移向左室
B.X气体为CO2
C.处理后的含硝酸根废水pH降低
D.电路中每通过1 mol电子,产生标准状况下氮气的体积为2.24L
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅、铁、铝等配制而成。试回答:
(1)30Si的原子的中子数为________。
(2)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则n=________。
(3)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是________。
(4)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为________。(只写结果)
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3.分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的是( )
A.  制取氧气 B.
制取氧气 B. ![]() 制取NaHCO3 C.
制取NaHCO3 C. ![]() 分离NaHCO3 D.
分离NaHCO3 D. ![]() 干燥NaHCO3
干燥NaHCO3
(NH4)2S2O8具有强氧化性,在酸性溶液中,可将Mn2+氧化为MnO4-,但一般情况下,该反应进行地非常缓慢,而加入AgNO3溶液后,混合液迅速变为紫红色。下列说法错误的是
A.AgNO3为该反应的催化剂 B.该反应中的还原产物为SO42-
C.反应中氧化剂与还原剂物质的量之比为2:5 D.S2O82-中-1价O与-2价O的个数比为1:3
已知某有机物的分子式为C3HaOb(a、b均是不为0的正整数),下列关于C3HaOb的说法中正确的是( )
A.当a=8时该物质可能发生加成反应 B.a一定是偶数
C.当a=6、b=2时该物质不可能含有两种官能团 D.1个C3HaOb可能含有3个醛基
- (09年湖北八校联考)要从名女生和名男生中选出名学生组成课外兴趣小组,如果按性别依比例分层随机抽样,则组成此课外兴趣小组
- 关于化学反应类型说法正确的是 A.有多种物质生成的反应叫做分解反应 B.氧化反应是指物质跟氧气发生的反应 C.氧气可以由
- “大将筹边尚未还,湖湘子弟满天山。新栽杨柳三千里,引得春风度玉关。”这首诗颂扬了哪一位为收复新疆做出贡献的历史人物是(
- 小明要制作一个圆锥模型,其侧面是由一个半径为9cm,圆心角为240°的扇形纸板制成的,还需要一块圆形纸板做底面,那么这块
- 今年是我国抗日战争胜利多少周年? A.65周年 B.70周年 C.75周年
- 10.如图所示为某动物卵原细胞中染色体组成情况,该卵原细胞经减数分裂产生3个极体和1个卵细胞。其中一个极体的染色体组成是
- ------ Thank you very much for your help! ------_______.
- 用自来水(用Cl2消毒)养金鱼时,将水注入鱼缸的前需在阳光下暴晒一段时间, 目的是
- 为防止灾后疫情出现,防疫人员用过氧乙酸( C2H4O3 )、次氯酸钠(NaClO)进行消毒。下列说法正确的是 A.次氯酸
- 取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( ) A.乙烯与溴水反应 B.丙烷与氯气在光照的作用
- “北通涿郡之渔商,南运江都之转输,其为利也博哉”。这句话指的是A.隋朝运河的作用 B.唐朝南北交通的发达C.元
- 若集合则“”是“”的____________条件。
- 下表为北半球年总辐射随纬度的分布表(可能总辐射:考虑了受大气减弱之后到达地面的太阳辐射;有效总辐射:考虑了受大气和云的减
- 国务院办公厅2013年3月1日发布的“国五条细则”规定,居民出售自有住房,按转让所得的20%征收个人所得税。这一规定
- Mrs. Bond is an old friend of . A.Jack mother B
- 对埋在地下的钢管常用如图所示方法加以保护,使其免受腐蚀。下列对金属棒X的材料分析正确的是()A.铜 B.钠 C.锌
- (26分)公平正义是衡量一个国家或社会文明发展的标准,是人类文明的标志之一。结合所学回答问题: (1)在党的十七大上,总
- 2010年12月10日至12日,备受市场关注的中央经济工作会议在北京举行,该会议为来年的经济发展作出规划。针对目前严峻的
- 今天,化学正在向着绿色化方面迈进,向着环境友好的方向发展“绿色化学”的核心是利用化学原理从源头消除污染,使所有作为原料的
- (七)下图示意我国东部主要石化基地和企业的分布。 18、图中兼有资源和市场区位优势的石化基地是 A、① B、②




