高三化学试题
铁镍可充电电池以KOH溶液为电解液,放电时的总反应为Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,下列有关该电池的说法正确的是
A、放电时,K+向Fe电极迁移 B、放电时,正极反应式为Fe-2e-+2OH-=Fe(OH)2
C、充电时,阴极附近溶液的pH增大
D、充电时,阴极反应式为2Ni(OH)2-2e-+2OH-=Ni2O3+3H2O
25℃时,下列各组离子在指定溶液中一定能够大量共存的是( )
A.0.1mol﹒L-1的AlCl3溶液中:Na+、K+、CO32-、NO3-、
B.pH=13的溶液中:Na+、NH4+、Cl-、NO3-
C.在含有大量I-离子的溶液中:Cl¯、Fe3+、Al3+、Cu2+
D.c(OH-)=1×10-13mol﹒L-1的溶液中:Mg2+、K+、Cl-、SO42-
下列离子方程式正确的是
A.向氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2—+2H2O
B.向硅酸钠溶液中滴加盐酸制取硅酸:SiO32—+2HCl=H2SiO3↓+2Cl—
C.Ba(OH)2溶液中滴加少量NH4HCO3溶液:
NH4++HCO3-+2OH-+Ba2+=NH3·H2O+H2O+BaCO3↓
D.用惰性电极电解饱和食盐水:2Cl-+ 2H+![]() H2↑ + C12↑
H2↑ + C12↑
下列各组物质中化学键的类型相同的是
A.HCl MgCl2 NH4Cl B.H2O Na2O CO2
C.CaCl2 NaOH H2O D.NH3 H2O CO2
下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
ClO2与Cl2的氧化性相近,常温下均为气体,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器C的名称是: 。安装F中导管时,应选用图2中的: (填“a”或“b”)
(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式: ;为使ClO2在D中被稳定剂充分吸收,可采取的措施是 。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是: .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为: ,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是: 。
(5)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂的保鲜原因是: 。
NH3、H2S等是极性分子,CO2、BF3、CCl4等是极性键构成的非极性分子。根据上述实例可以推测出ABn型分子为非极性分子的经验规律是
A.分子中必须含有π键 B.在ABn分子中A原子没有孤对电子
C.在ABn分子中不能形成分子间氢键 D.分子中每个共价键的键长应相等
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题:

①甲烷燃料电池负极的电极反应为________________________。
②闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是____________(填化学式),电解氯化钠溶液的总反应方程式为_________________________;
③若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1,列式计算),最多能产生的氯气体积为__________L(标准状况)。
能证明硅酸的酸性弱于碳酸酸性的实验事实是
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸盐反应生成CO2
D.HCl通入可溶性碳酸盐溶液中放出气体,氯化氢通入可溶性硅酸盐溶液中生成沉淀
下列说法正确的是( )
A. HCl溶液中无OH- B. NaOH溶液中无H+
C. KCl溶液中既无H+也无OH- D. 常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14
现有Al3+、Ba2+、Mg2+、Ag+四种离子的混合溶液,若要使这四种离子依次成为沉淀从溶液中分离出来(可供选择的粒子为H+、OH-、NH4+、Cl-、NO3-、SO42-、CO32-及CO2),则应加入的粒子的最佳选择及顺序依次为 。
部分弱酸的电离常数如下表:
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
下列有关说法不正确的是( )
A. 等体积、等浓度的HCOONa和NaCN两溶液中所含阴离子数目相等
B. HCOO-、CN-、HS-在溶液中可以大量共存
C. NaHS溶液中加入适量KOH后:c(Na+)=c(H2S)+c(HS-)+C(S2-)
D. 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
与有机物B相关的反应信息如下:
 |
(1)写出下列反应的反应类型:
B→A______________,D→E第①步反应________________。
(2)写出E、C的结构简式:E_______________。C_______________。
(3)C的一种同分异构体K有如下特点:1molK可以和3mol金属钠发生反应放出33.6LH2(标准状况下),1molK可以和足量的NaHCO3溶液反应,生成1molCO2,1molK还可以发生银镜反应生成2moIAg,试写出K的结构简式________________________。
(4)写出在浓硫酸存在并加热的条件下,F与足量乙醇反应的化学方程式
________________________________________________________________。
![]()
PET( ,M链节= 192 g·mol−1)可用来生产合成纤维或塑料。测某PET样品的端基中羧基的物质的量,计算其平均聚合度:以酚酞作指示剂,用c mol·L−1 NaOH醇溶液滴定m g PET端基中的羧基至终点(现象与水溶液相同),消耗NaOH醇溶液v mL。下列说法不正确的是
A.PET塑料是一种可降解高分子材料
B.滴定终点时,溶液变为浅红色
C.合成PET的一种单体是乙醇的同系物
![]() D.PET的平均聚合度 (忽略端基的摩尔质量)
D.PET的平均聚合度 (忽略端基的摩尔质量)
某小组以4H++4I-+O2=2I2+2H2O为研究对象,探究影响氧化还原反应因素。
| 实验 | 气体a | 编号及现象 |
|
| HCl | Ⅰ.溶液迅速呈黄色 |
| SO2 | Ⅱ.溶液较快呈亮黄色 | |
| CO2 | Ⅲ.长时间后,溶液呈很浅的黄色 | |
| 空气 | Ⅳ.长时间后,溶液无明显变化 |
(1)实验Ⅳ的作用是______________。用CCl4萃取Ⅰ、Ⅱ、Ⅲ、Ⅳ的溶液,萃取后下层CCl4的颜色均无明显变化。
(2)取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅲ的溶液变蓝;Ⅱ、Ⅳ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅲ中生成了______________。
(3)查阅资料:I2易溶于KI溶液。下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。

现象x是______________。
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:溶液中c(H+)较小。小组同学认为此假设不成立,依据是______________。
假设2:O2只氧化了SO2,化学方程式是______________。
假设3:I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
i.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ii.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。加入酸化的AgNO3溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
iii.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
| 电解时间/min | 溶液 | 阳极 | 阴极 |
| t1 | 黄色变浅、有少量SO42- | 检出I2,振荡后消失 | H2 |
|
| 溶液无色、有大量SO42- | 检出I2,振荡后消失 | H2 |
结合化学反应,解释上表中的现象:______________。
(6)综合实验证据说明影响I-被氧化的因素及对应关系______________。
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1L pH=5的醋酸溶液中含有的H+数目小于10NA
B.9.2g 14CO2与N218O的混合物中所含中子数为4.8NA
C.硝酸与铜反应生成0.1mol NO2时,转移电子数为0.2NA
D.1mol SO₂和0.5mol O2充分反应,生成SO3的分子数为NA
铜是一种重要的有色金属,含铜物质用途很广泛。
 (1)氯化亚铜是一种重要的化工产品。在CuCl2溶液中逐滴滴入过量KI溶液可能发生:
(1)氯化亚铜是一种重要的化工产品。在CuCl2溶液中逐滴滴入过量KI溶液可能发生:
a.2Cu2++4I-=2CuI↓+I2
b.2Cu2++2I-+2C1-=2CuCl↓+I2
若a反应为主反应,则KSP(CuI)_________KSP(CuC1)(填“>”“<”或“=”)。
(2)常温下,Cu+在水中会发生水解反应:![]() ,该反应的平衡常数K=_____________________。(已知CuOH的KSP=1.0×10-14)
,该反应的平衡常数K=_____________________。(已知CuOH的KSP=1.0×10-14)
(3)向含有C1-的溶液中同时加入Cu和Cu2+,会生成CuC1沉淀。溶液中平衡时相关离子浓度的关系如图1。
①上述反应的离子方程式为_______________________________________________。
②某同学由图可知:反应2Cu+=Cu2++Cu趋于完全,请列式计算说明他的观点正确______
___________________________________________________________________。
(4)锂—铜空气燃料低成本高效电池放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,其工作原理如图2。
①放电时,正极的电极反应式为_______________________________________________。
②分析装置图可知,整个反应过程中,氧化剂为_________________________________。
汞(熔点﹣39℃,沸点356℃)是制造电池、电极等的重要原料,历史上曾用“灼烧辰砂法”制取汞.目前工业上制粗汞的一种流程图如下.

下列分析错误的是( )
A. “灼烧辰砂法”过程中电子转移的方向和数目可表示为: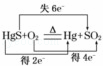
B. 辰砂与氧化钙加热反应时,CaSO4为氧化产物
C. 洗涤粗汞可用5%的盐酸代替5%的硝酸
D. 减压蒸馏的目的是降低汞的沸点,提高分离效率
下列气体中,既有颜色又有毒性的是( )
A.Cl2 B.CO C.N2 D.CO2
关于化合物2−苯基丙烯(![]() ),下列说法正确的是( )
),下列说法正确的是( )
A.不能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应
C.分子中所有原子共平面 D.易溶于水及甲苯
- 空间某一静电场的电势φ在x轴上分布如图所示,x轴上两点B、C的电场强度在x方向上的分量分别是EBx、ECx,下列说法中正
- 陈凯将以下历史事件按时间先后顺序整理,其正确的顺序应是( ) ①五四运动 ②辛亥革命 ③ 西藏和平解放
- 自2016年6月以来,湖南多个地方发生了暴雨灾害,家住怀化的宁宁也是受灾群众中的一员,看着眼前满目疮痍的家乡,宁宁内心
- 下图所示是我国古代一部杰出的史学巨著。下列对该著作的表述不正确的是A.是我国第一部纪传体通史 B
- 科学家对生长在某区域两个不同地段(水分条件相对较好的沟底和水分条件较差的坡面)的中国酸刺的雌、雄株进行了研究。测得一天中
- 线圈在转动过程中某一段时间内或从一个位置到另一个位置的过程中所产生的电动势,称为平均电动势,它不等于始、末两时刻瞬时值的
- 由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分
- 关于固体、液体和气体,下列说法正确的是 。(填正确答案标号。选对1个得3分,选对
- 将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(mi
- 名著阅读(2分)(1)《伊索寓言》中《 》的故事告诫人们,对恶人千万不能心慈手软。(2)在《
- 15℃时,声音在下列哪种介质中传播得最快 ( ) A.空气 B.海水 C.钢
- 依次填入下列各句横线处的词语,恰当的一组是 ①在这种态度下,就是 历史,只懂得希腊,不懂得中国,对于中国的昨
- Edward was excited to be toldthat his wife ____his children
- (10分)君权与相权的关系贯穿整个中国古代政治制度的发展历程。阅读下列材料: 材料一 丞相者,朕之股肱,所与共承庙宇,统
- (4分)飞机起飞时以100m/s的速度与水平成角飞行。第10s末飞机距地面高度等于________m,第10s末物体距出
- (16分)Ⅰ.下图是实验室制备乙酸乙酯的装置图,填写下列空白。(1)试管A中加入沸石的作用是:__________。导管
- 已知A(0,3),B(-1,0),C(3,0),求D点的坐标,使四边形ABCD为直角梯形(A、B、C、D按逆时针方向排列
- When you state your plan to improve the service of the hote
- 补写出下列名篇名句的空缺部分,任选两小题。 (1)_________ ,_________ ,颁白者不负戴于道路矣。(
- 31.下列辛亥革命时期的重大历史事件,按其发生的时间先后顺序排列,正确的是( ) ①孙中山就任中华民国临时大总统




