高三化学试题
已知KMn![]() O4与浓盐酸在常温下反应能产生Cl2。若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是(不考虑①单元的夹持装置)( )
O4与浓盐酸在常温下反应能产生Cl2。若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是(不考虑①单元的夹持装置)( )

A.只有①和②处 B.只有②处 C.只有②和③处 D.②、③、④处
常温下,物质的量浓度相等的下列物质的水溶液,pH最小的是 ( )
A.NH4ClO4 B.BaCl2 C.HNO3 D.K2CO3
将甲烷、氧气、过氧化钠放入密闭容器中,在150℃条件下不断用电火花引发反应,最终三种物质都恰好反应,容器中压强接近为零。由此计算:
(1)原混合物中甲烷、氧气、过氧化钠的物质的量之比是多少?(2)反应后容器中的物质是?
A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为 。
(2)F在元素周期表中的位置 。
(3)用电子式表示元素B与元素F形成的化合物: 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
(6)某混合物的稀溶液中,只可能含有B、C、F构成的简单离子或A、E的最高价氧化物对应水化物所电离出来的阴离子。现分别取一定体积的该溶液进行实验。两次每次取200.00mL进行实验。
实验1:取2mL溶液,向其中加入AgNO3溶液有沉淀产生;
实验2:取200mL溶液,向其中加入足量BaCl2溶液后,得干燥沉淀12.54g,沉淀经足量盐酸洗涤、干燥后,剩余4.66g。请回答:
①根据以上实验,不能判断是否存在的离子有 。
② B的简单离子是否存在 ;若存在,浓度至少为 mol/L(若不存在,则不必回答第二问)。
在抽滤瓶内放一小块金属钠,同时收集满CO2气体并塞紧瓶塞。从分液漏斗中放入一定量的水,待钠完全反应并恢复到反应前温度时,发现气球凹瘪,则抽滤瓶内溶液中的溶质是
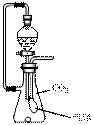
A.NaOH与Na2CO3 B.Na2CO3
C.Na2CO3与NaHCO3 D.NaHCO3
下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100 mL,放置一段时间后,有关叙述不正确的是(不考虑溶液体积变化)( )

A、a2电极上有亮红色固体
B、a1、a3电极上产生的物质,物质的量比是1:2
C、丙中的SO42-向a6电极移动
D、当装置电路中有6.02×1021个电子通过时,乙中溶液的pH是13
氯气是一种重要的化工原料。某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。

(1)实验室用二氧化锰和浓盐酸加热制取氯气,其反应方程式为__________________。
(2)装置 A 中盛有的试剂的作用是___________________________________。
(3)验证装置 B 发生反应后的产物实验方法是___________________________________ 。
某研究性学习小组用刚吸收过少量 SO2 的 NaOH 溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在 Cl-、OH-、CO32-和 SO42-,对于可能存在的其他阴离子,研究小组提出以下3 种假设。假设 1:只存在 ClO-;假设 2:只存在 SO32-;假设 3:既不存在 SO32-也不存在 ClO-。
()学习小组判断同时存在 SO32-和 ClO-是不可能的理由是_____________________。
(5)为了验证哪种假设是正确的,现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现
象和结论。
a.3 mol·L-1 H2SO4 b.0.01 mol·L-1 KMnO4
c.1 mol·L-1 BaCl2 溶液 d.淀粉碘化钾溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加 3 mol·L-1 H2SO4 至溶液呈中性,然后将所得溶液分装于 A、B 两试管中。
步骤二:向 A 试管中滴加少量__________(填序号),若溶液____________________(填现象),则假设 1 成立。
步骤三:向 B 试管中滴加少量__________(填序号),若溶液____________________(填现象),则假设 2 成立。
室温下,向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A. 溶液中导电粒子的数目减少
B. 溶液中c(CH3COO-)/c(CH3COOH)•c(OH-)不变
C. 醋酸的电离程度增大,c(H+)也增大
D. 再加入10mL pH=11的NaOH溶液,混合液的pH=7
室温下将l0mL c(H+)=0.00l![]() mol/L的醋酸溶液加水稀释10倍后,下列说法正确的是
mol/L的醋酸溶液加水稀释10倍后,下列说法正确的是
A. 醋酸的电离程度增大,c(H+)亦增大 B. 溶液中 不变
不变
C. 溶液中导电粒子的数目增多
D. 再加入l0mL c(OH-)=0.00lmol/L的NaOH溶液,混合液呈中性
有A、B、C、D四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
| 阳离子 | Na+、Ba2+、NH |
| 阴离子 | CH3COO-、OH-、Cl-、SO |
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象。
(1)A是__________,B是____________(填化学式) 。
(2)写出C和D反应的离子方程式________________。
(3)25 ℃时,0.1 mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=____________________(用含有a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是________________。
(5)在一定体积的0.005 mol·L-1的C溶液中,加入一定体积的0.00125 mol·L-1的盐酸,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是______。
通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+ H2O2+ BaCl2= BaSO4↓+ 2HC1 ,用NA表示阿伏加德罗常数的值,下列说法不正确的是
A. 0.1 molBaCl2中所含离子总数约为0.3 NA
B. 25℃时,pH=l的HC1溶液中含有H+的数目约为0.1 NA
C. 标准状况下,17gH2O2中所含电子总数约为9 NA
D. 生成2.33gBaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224L
下列元素在自然界中存在游离态的是
A.S B.Cl C.Al D.Mg
化学与生活、社会发展息息相关,下列有关说法不正确的是
A. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
B. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
C. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
D. “外观如雪,强烧之,紫青烟起”,该过程中利用了焰色反应
在t℃时,向xg 硝酸钾不饱和溶液中加入ag 硝酸钾或蒸发掉bg水,恢复到t℃,溶液都达到饱和,据此,下列推论不正确的是( )
A.在t℃时,硝酸钾的溶解度为![]()
B.若原溶液中溶质的质量分数为![]() ,则x=2b
,则x=2b
C. 在t℃时,所配的硝酸钾溶液中溶质的质量分数为![]() %
%
D. 若将原溶液蒸发掉2bg水,恢复到原温度析出2ag 硝酸钾
下列说法正确的是( )
A. 切开的金属Na暴露在空气中,光亮表面逐渐变暗的主要原因是:2Na+O2 = Na2O2
B. 漂白粉、氯水是混合物,水银、明矾是纯净物
C. HCl、NH3、BaSO4是电解质,CO2、Cl2、CH3CH2OH是非电解质
D. 水能、风能、煤、石油、天然气都是可再生能源
下列有关说法正确的是
A.4CuO(s)=2Cu2O(s)+O2(g)在室温下不能自发进行,说明该反应△H>0
B.向稀醋酸中加入醋酸钠固体,溶液pH升高的主要原因是醋酸钠水解呈碱性
C.室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN大
D.H2S(g)+FeO(s)![]() FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大
FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大
某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是

A. 曲线II代表HCl的稀释过程
B. 溶液中水的电离程度:b点>c点
C. 从b点到d点,溶液中![]() 保持不变
保持不变
D. 该温度下,b点Kw的数值比e点大
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)=2CO2(g);△H=-566kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ·mol-1
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
A.2912 kJ B.2953 kJ
C.3236 kJ D.3867 kJ
其它条件一定时,升高温度,下列数据不一定增大的是
A.化学反应速率v B.反应物活化分子百分数
C.化学平衡常数K D.水的离子积常数KW
钒和镍及其化合物是重要的合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的价电子排布式为_______,其排布时能量最高的电子所占据能级的原子轨道有_______个伸展方向。
(2)VO2+与 可形成配合物。
可形成配合物。 中,三种非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
中,三种非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______。与CN-互为等电子体的一种分子的化学式为________ 。
(4) 三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF5、H2O2等为主要原料来制取。
①H2O2分子中O 原子的杂化方式为_______。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为_______。

(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2 所示,该晶胞中S2-的配位数为_________。
(6)镧镍合金是重要的储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为_________。
②该镧镍合金储氢后氢的密度为_________(用NA表示阿伏加德罗常数的数值)g/cm3。
- 读“我国部分地区重大自然灾害点位图”(1900~2000年),完成下列问题。(10分)(1)此区域既是我国_______
- 能直接体现现阶段我国社会主要矛盾的是 ( )①2011年3月13日,
- --I’m not good at basketball, you know.-- ____ we’re playing
- 将图中的开关、螺丝口灯泡、插座接入家庭电路。要求开关控制灯泡。
- 盛夏来临,人们又为“怎样才能晒不黑”而犯愁,资料表明:将皮肤晒黑的罪魁祸首是太阳光中的长波紫外线.“好奇实验室”为此检测
- (2011年江苏徐州,21题)2011年我国长江中下游地区遭遇到持续干旱,造成人畜饮水困难,各地采取措施积极抗旱。请回单
- CCTV《科技博览》报道,中科院首创用CO2合成可降解塑料聚二氧化碳。下列相关说法合理的是( ) A.聚二氧化碳塑
- (2010·广东省梅州市,(二),4分)赏析诗歌,回答相关问题。早春呈水部张十八员外韩愈天街小雨润如酥,草色遥看近却无。
- 已基本干燥的抹灰白墙(熟石灰),住人后往往又会变得潮湿,这主要是由于() A.壁中有水渗出 B.熟石灰与二氧化碳反应的生
- 在一定条件下,RO和氟气可发生如下反应:RO+F2+2OH-RO+2F-+H2O 从而可知在RO中,元素R的化合价是 A
- Peter’s jacket looked just the same asJack’s, but it cost _
- 有关原电池的工作原理中,下列说法中不正确的是A.电池负极发生氧化反应 B.电池正极
- 以前的黄土高原和幼发拉底河流域曾是森林茂密的理想居住场所,为人类文明做出了重要贡献,而今却成了不毛之地,其主要原因是(
- (一)文言文阅读(19分) 阅读下面的文言文,完成10-13题。 郑岳,字汝华,莆田人。弘治六年进士。授户部主事,改刑部
- 下列词语中加点字注音有错误的一组是( ) A.汲取(jí) 慨叹(kǎi) 滞碍(zhì) 玄虚(xu
- △ABC中,D为BC边中点,已知向量则 () A.B.C.- D.
- 工业上常用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出)。(
- 世界上第一长河是………………………………………………………………………( ) A.尼罗河
- 全党同志“要不断丰富和发展马克思主义理论”。其哲学理论依据是( ) ①世界是客观存在的物质世界 ②人们对客观事物
- 尽管具体形式迥异、发展程度不同,现代资本主义国家的政体大都奉行分权制衡的原则,而我国的人民代表大会制度具有区别于任何资本



