高三化学试题
常温时,将0.1 mol Fe(NO3)3和2 mol HCl溶于水得2 L混合溶液,然后向该溶液投入m g铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法不正确的是( )
A.由于氧化性Fe3+>H+,首先发生的反应是Fe+2Fe3+===3Fe2+
B.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体
C.在铁粉充分反应后的溶液中,铁元素以Fe2+的形式存在
D.m至少等于28,反应过程中溶液的质量一直在增加
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品.某研究小组用粗铜(含杂质Fe)按如图1述流程制备氯化铜晶体(CuCl2•2H2O).(已知Fe3+沉淀完全的PH为3.6,Cu2+)开始沉淀的PH为6.4

(1)实验室采用如图2所示的装置,可将粗铜与C12反应转化为固体1(加热仪器和夹持装置已略去).
①仪器A的名称是 .
②装置B中发生反应的离子方程式是 .
③装置IV中盛装的试剂是 ,其作用是 (用离子方程式表示).
④CuCl2溶液经一系列操作可得氯化铜晶体,操作的程序依次为 、 过滤、自然干燥.
(2)由CuCl2溶液得到CuCl2•2H2O的过程中要加入盐酸的目的是 .
下列变化不属于化学变化的有几项
①用铁质容器盛放浓硝酸 ②给装有氯化铵的试管加热,在管口又有白色晶体产生 ③液氮用作制冷剂 ④ 明矾用作净水剂 ⑤碳酸钠晶体的风化 ⑥用氢报破刻蚀石英制艺术品 ⑦二氧化氮气体遇冷颜色变浅
A. 0 B. 1 C. 2 D. 3
直接排放含SO2 会形成酸雨,危害环境。某化学实验小组用如下装置进行有关SO2性质的探究活动。

(1)装置A 中反应的离子方程式为_____________。
(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是_________。正确的连接顺序是:A→C→_____________→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氣酸的酸性的实验现象是__________________________。
(3)将二氧化硫通入以下装置可以制备Na2S2O3:

①装置B 的作用是检验装置A 中SO2 的吸收效率,B 中试剂是________;
②写出装置A 中发生反应的化学方程式________;
③Na2S2O3 溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3( 化学式量:214)固体配成溶液;
第二步:加入过量KI 固体和H2SO4 溶液,滴加指示剂;
第三步用Na2S2O3溶液滴定至终点。消耗Na2S2O3溶液的体积为v mL。则c(Na2S2O3)=______ mol/L。(已知:IO3- +5I-+6H+=3I2+3H2O,2S2O32-+I2=S4O62-+2I-)
25℃时,对有关溶液的分析不正确的是( )
A.将0.1 mol.L-l Na2C03溶液加水稀释后,溶液中n(H+).n(OH一)不变
B.pH =2的醋酸溶液与pH =12的氢氧化钠溶液中水的电离程度相同
C.pH相同的①CH3COONa②NaHC03③NaClO三种溶液中c(Na+):①>②>③
D.C H3COONa和CaCl2混合溶液:
c(Na+) +2c(Ca2+)=c(CH3COO-)+c( CH3COOH) +c( Cl-)
在标准状况下,用一定量的水吸收氨气后得到浓度为12.0 mol/L密度为0.915g·cm-3的氨水,试计算(要求写出计算过程):
(1)该氨水溶质的质量分数ω是多少?(用百分数表示,保留到小数点后一位数)
(2)1 L水吸收标准状况下的氨气多少升可制得上述氨水?(水的密度以1.00g·cm-3计,计算结果取整数。)
试判断116号新元素在周期表中的位置
A、第6周期ⅣA族 B、第7周期ⅥA族
C、第7周期Ⅷ族 D、第8周期ⅥA族
某温度下,![]()
![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液
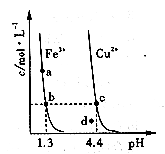
分别在溶液中达到沉淀溶解平衡后,改变溶液![]() ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
 A.
A. ![]()
B.加适量![]() 固体可使溶液由
固体可使溶液由![]() 点变到
点变到![]() 点
点
C.![]()
![]() 两点代表的溶液中
两点代表的溶液中![]() 与
与![]() 乘积相等
乘积相等
D.![]() 、
、![]() 分别在
分别在![]() 、
、![]() 两点代表的溶液中达到饱和
两点代表的溶液中达到饱和
在c(Ca2+)=0.1mol·L-1的新制漂白粉的溶液中,下列各组离子能大量共存的是
A.Na+、K+、CO32-、NO3- B.Na+、K+、SO32-、OH-
C. K+、Na+、NO3-、CH3COO- D. H+、NH4+、NO3-、SO42-

1 L某混合溶液中,溶质X、Y的浓度都为0.1 mol/L,向混合溶液中滴加某溶液Z(0.1 mol/L氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是
A.偏铝酸钠、氢氧化钡、硫酸
B.氯化铝、氯化镁、氢氧化钠
C.氯化铝、氯化铁、氢氧化钠
D.偏铝酸钠、氯化钡、硫酸
将aLNH3通过灼热的装有铁触媒(工业上合成氨所用的催化剂)的硬质玻璃管后,气体体积变为bL(气体体积均在同温同压下测定),该bL气体中的NH3体积分数是()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
a、b、c、d为常见短周期主族元素,a2-、b+、c3+的电子层结构相同;b、c、d位于同周期,b、c、d的最高价氧化物对应的水化物之间能相互反应。下列叙述错误的是( )
A. d一定位于周期表第三周期第Ⅷ族 B. 简单离子的半径:a2->b+>c3+
C. b的最高价氧化物对应的水化物碱性比c强 D. a能分别与b、c组成离子化合物
下列实验“操作和现象”与“结论”对应关系都正确的是( )
| 选项 | 操作和现象 | 结论 |
| A | 将少量氯水加入KI淀粉溶液中,溶液由无色变成蓝色 | 氧化性:Cl2>I2 |
| B | 常温下,打磨后的铁片放入浓H2SO4中,无明显反应现象 | 常温下,铁与浓H2SO4不反应 |
| C | 向足量NaOH溶液中,先滴加少量MgCl2溶液,再滴加FeCl3溶液,先出现白色沉淀,后出现红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 室温下用pH试纸测定同浓度的NaClO溶液和CH3COONa溶被可知:pH(NaClO)>pH(CH3COONa) | 酸性HClO>CH3COOH |
A. A B. B C. C D. D
下列叙述错误的是 ( )
A.生铁中含有碳,抗腐蚀能力比纯铁弱
B.用锡焊接的铁质器件,焊接处易生锈
C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
D.铁管上镶嵌锌块,铁管不易被腐蚀
钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:

已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解。
请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有 ;
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理 。
(3)已知钛的还原性介于铝与锌之间。如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是 。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式是 。
(5)为测定溶液中TiOSO4的含量,先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。
过滤后,取无色滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,
用 (填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,
发生Ti3++Fe3+=Ti4++Fe2+。滴定终点时的现象是 ,
若用去了30.00mL FeC13溶液,待测钛液中TiOSO4的物质的量浓度是 mol/L。
采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应)。下列说法正确的是
 A.Zn与电源的负极相连
A.Zn与电源的负极相连
B.ZnC2O4在交换膜右侧生成电解
C.电解的总反应:2CO2+Zn ======ZnC2O4
D.通入11.2 L CO2时,转移0.5 mol电子
对于下图所示实验,下列实验现象预测或操作正确的是

A.实验甲:匀速逐滴滴加盐酸时,试管中没气泡产生和有气泡产生的时间段相同
B.实验乙:充分振荡后静置,下层溶液为橙红色,上层为无色
C.实验丙:由MgCl2•6H2O制备无水MgCl2
D.装置丁:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去
Cl2是一种重要的化工原料,结合氯气的相关知识解决下列问题.
(1)运输氯气的钢瓶上应贴的标签为 .
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)工业上将氯气通入石灰乳制取漂白粉,写出该反应的化学方程式 .
(3)漂白粉的有效成分是(填化学式) .
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2.高锰酸钾溶液常用于物质的定性检验与定量分析.某化学兴趣小组在实验室里欲用KMnO4固体来配制500mL 0.1mol/L的KMnO4溶液.
①需用的仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、 .
②下列操作会导致实验结果偏小的是 (填字母).
a.转移时没有洗涤烧杯、玻璃棒
b.容量瓶内壁附有水珠而未干燥处理
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
d.加水定容时俯视刻度线
③用配好的该浓度的KMnO4溶液与300mL 0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为 mL.
(5)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空
(a、b、c、d重合部分代表物质间反应,且氯水足量,已知:Cl2+2Br﹣=2Cl﹣+Br2 ).

①能证明氯水具有漂白性的是 (填“a”、“b”、“c”或“d”),现象是 .
②a中发生反应的离子方程式是 .
生产、生活中常涉及化学知识,下列说法正确的是( )
A. ClO2、酒精、双氧水均能杀菌消毒,其原理相同
B.天然纤维的主要成分都是纤维素
C.煤的干馏和煤的液化均为化学变化
D.蛋白质、油脂、烧碱、碳酸钙是按纯净物、混合物、电解质和非电解质顺序排到
化学与生产、生活密切联系。下列有关说法不正确的是
A.网状结构的聚丙烯酸钠是高吸水性树脂,可用于制造“尿不湿”
B.光导纤维应避免在强碱性环境中使用
C.利用超临界CO2流体作为萃取溶剂符合绿色化学
D.船体镀锌或锡均可保护船体,镀层破损后将立即失去保护作用
- 下列离子方程式错误的是A.Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++====3Fe3++2H2O+NO↑B.
- 下列有关尿素[CO(NH2)2]的说法,错误的是 A.它可以作氮肥 B.尿素分子中碳、氢原子个数比为1:4 C.尿素由碳
- 印度、孟加拉、印度尼西亚等国的城市化表现为: A.高度城市化 B.虚假城市化 C.滞后城市化
- 已知是上的偶函数,若将的图象向右平移一个单位后,则得到一个奇函数的图象,若 (
- (2008山东烟台高一测试,3)已知a=()-,b=()-,c=()-,则a,b,c三个数的大小关系是() A.c<
- 计算(9分)(1) (2) (3)
- 中国领导的多党合作和政治协商制度 ①是我国的一项基本政治制度 ②是我国的一项
- 第二节:完形填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,从短文后各题所给的四个选项(A、B、C、和D)
- 因式分解 x2-9y2+x+3y.
- 我国资本主义萌芽自产生后发展十分缓慢。究其原因,从市场的角度看,主要包括 ①农民遭受残酷的封建剥削 ②清政府
- 等比数列前项的和为,则数列前项的和____________.
- Vitamin D helps our bodies make a special chemical, and thi
- 函数y=的定义域________.
- 用边长为1的正方形做了一套七巧板,拼成如图1所示的一座桥,则桥中阴影部分的面积为原正方形面积的( )A. B.
- 设数列的各项都是正数,, , . ⑴求数列的通项公式;⑵求数列的通项公式; ⑶求证: .
- 下列物质露置于空气中,一段时间后,质量增加的是 A.碳酸钙 B.氯化钠 C.浓盐酸
- 下图为细胞结构示意图,在细胞中能控制物质进出的结构是( )A.② B.④ C.⑤
- 关关雎鸠,在河之洲。__________,__________。(《诗经·关雎》)
- 已知:A是红色粉末,B、C是氧化物,D、I是常见金属,E为稀盐酸,H为浅绿色溶液。它们之间的转化关系如下: ② A
- 在现实生活中,人们的消费心理主要有: ①从众心理 ②求异心理 ③攀比心理 ④求实心理 A、①② B



