高三化学试题
铜能与稀硝酸反应,反应方程式为:
3Cu+8HNO3(稀)= 3Cu(NO3)2+2NO↑+4H2O,当有9.6克Cu参加反应时,
求:
(1)产生气体在标准状况下的体积
(2)被还原的硝酸的质量
土法酿造葡萄酒(只加糖的纯天然酿酒法)容易出问题,有报道说,喝了自制葡萄酒差点失明。主要原因是年木发酵过程产生的菌种多达百种,难以控制,而产生对神经有毒的甲醇等物质。科学酿酒加SO2等辅料。我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。
(1) 葡萄酒中添加SO2的作用可能是________。
A.氧化细菌 B.抗氧化 C.漂白 D.增酸作用
I.实验方案一
利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或HSO3。设计如图1的实验:

(2) 甲同学得出实验结论: 干白葡萄酒中不含SO2或HSO3。这个结论是否合理? 说明理由_____________。
Ⅱ.实验方案二
如图2是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。

(3) 关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没瓶中固体,写出C 装置反应的方程式______,每消耗1molNa2O2,则转移电子数___________。
(4) 关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F 中,为了证明SO2有还原性,并从绿色化学的角度考虑,则Z 试剂可以是___________,现象是___________。
Ⅲ.实验方案三
用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入图3 装置(电极均为惰性材料) 进行实验,可用于制备硫酸,同时获得电能:

(5)M 极发生的电极反应式为__________。N极区溶液pH______(变大、变小、不变)
(6) 若使该装置的电流强度达到2.0A,理论上8 分钟应向负极通入标准状况下气体的体积为_____ L (已知: 1个e所带电量为1.6×10-19C,阿伏伽德罗常数6×1023)。
下列实验中,①pH试纸的使用,②过滤,③蒸发,④配制一定物质的量浓度溶液,均用到的仪器是
A.蒸发皿 B.玻璃棒 C.试管 D.分液漏斗
甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,下列说法不正确的是( )
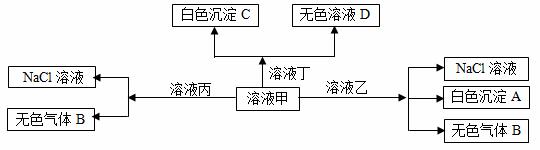
A.在甲中滴加丁可能发生反应:HCO3—+ Ba2++OH—= BaCO3↓+ H2O
B.溶液丙中还可以大量共存的离子有:I—、NO3—、SO42—
C.白色沉淀A可能溶解在溶液D中
D.甲为![]() NaHCO3,乙为 AlCl3
NaHCO3,乙为 AlCl3
某金属M的氢氧化物的水合晶体[M(OH)2•xH2O]与Na2CO3混合物共36.800g,加入足量的水后,生成MCO3的白色沉淀,将沉淀滤出,洗净烘干,其质量为9.850g。
(1). 将 9.850g MCO3高温灼热至恒重,得到7.650g MO固体,则产生CO2气体_______mol。
(2).滤液与酸作用不产生气体;若用足量的铵盐与滤液共热,则产生4.48L气体(标准状况),滤液中OH‑的物质的量为_______mol。
(3).M的相对原子质量为_________;试通过计算确定M(OH)2•xH2O中x的值:
某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | ||
| 验证不稳定性 |
25℃、101kPa下充分燃烧一定量丁烷气体放出的热量为Q kJ,用5mol/L的KOH溶液200mL完全吸收生成的CO2,并与之生成正盐,则丁烷的燃烧热的数值是
A.16Q B.8Q C.4Q D.2Q
下列关于有机化合物的说法不正确的是:
A. 可以用新制的氢氧化铜悬浊液(可加热)鉴别乙醇、乙酸和葡萄糖
B. 苹果酸的结构简式为HOOCCH(OH)CH2COOH,则该物质可发生氧化、酯化、缩聚反应
C. —C3H7和—C2H5O各取代苯分子中的一个氢原子形成的二元取代物共有24种
D. 高分子化合物![]() 的单体是CH2=CH2和C2H5COOH
的单体是CH2=CH2和C2H5COOH
利用下图装置(略去部分夹持仪器,气密性己检验)生产硷代硫酸钠晶体(Na2S2O3·5H2O)。实验步骤是先向装置①的烧瓶中滴加80%的浓H2SO4;充分反应后过滤装置③中混合物,滤液经结晶即得到产品。

已知:2Na2S +Na2SO3+3SO2=3Na2S2O3。下列判断不正确的是
A.应用装置①,利用H2O2和MnO2 可制取少量O2
B.实验过程中,装置②和装置④的作用相同
C.装置③中⑤Na2S和Na2SO3的物须的量之比最好为1:2
D.装置⑤中盛有NaOH 溶液、可吸收多余的尾气
图中各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1∶1。甲是发酵粉的主要成分,乙是一种常用的化肥,B、D常温常压下是气体。请回答下列问题:
(1)甲的俗名是________。
(2)A、D物质的水溶液分别滴入酚酞试液后,溶液均显红色,其原理________(填“相同”或“不相同”)。
(3)甲在潮湿的空气中会缓慢分解,A会吸收空气中的水分:A+nH2O===A·nH2O(n为平均值,n≤10),取没有妥善保管的甲样品9.16 g,溶于水制成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的B的体积(标准状况)如下表:(溶于水中的B不计)
| 盐酸的体积(mL) | 4 | 8 | 15 | 20 | 50 | 120 | 150 |
| 生成B的体积(mL) | 0 | 0 | 112 | 224 | 896 | 2240 | 2240 |
则:
① 稀盐酸的物质的量浓度为__________________________________。
② 样品中的成分及其物质的量分别为__________________________________。
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-中的几种。①用pH试纸测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
A.Na+ B.SO42- C.Ba2+ D.NH4+
化学知识在生产和生活中有着重要的应用。下列说法中正确的是( )
(1)钠的还原性很强;可以用来冶炼金属钛、钽、铌、锆等
(2)K、Na合金可作原子反应堆的导热剂
(3)明矾常作为消毒剂
(4)Na2O2既可作呼吸面具中O2的来源;又可漂白织物、麦杆、羽毛等
(5)碳酸钠在医疗上是治疗胃酸过多的一种药剂
(6)分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
(7)人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3。
A. (1)(2)(3)(4) B. (1)(2)(4)(6)
C. (1)(2)(4)(6)(7) D. (1)(2)(3)(4)(5)(6)(7)
设NA为阿伏加德罗常数值。下列有关叙述正确的是
A. 13g乙炔中含有共用电子对的数目为1.5NA
B.含有2NA个氧原子的氧气和臭氧的混合气体的质量为32g
C. 1 mol·L-1碳酸钠溶液中含有的碳酸根离子的数目小于NA
D.标准状况下,将22.4LCl2通入水中发生反应,转移的电子数为NA
工业上制纯碱是根据NaHCO3溶解度比NaCl、Na2CO3、NH4Cl、NH4HCO3都小的性质,在适宜温度下运用:CO2+NH3+H2O+NaCl→NaHCO3+NH4Cl等反应原理制取的。欲在实验室通过上述过程和其它的必要反应制取纯碱,可用下列图示中的①②③④几个步骤,其中A、B分别代表CO2和NH3之一。
![]()
(1)操作③所得到的晶体是下列的____;
A.NH4Cl B.NaHCO3 C.Na2CO3 D.NH4HCO3
(2)对于上述过程,下列叙述正确的是 。
A.气体A是CO2,气体B是NH3
B.气体A是NH3,气体B是CO2
C.步骤④是加热
D.①②两步操作的顺序与两种气体溶解度有重要的关系,不能颠倒
短周期主族元素X、Y、Z、W原子序数依次增大,X的原子核内只有一个质子,Y原子最外层比W原子最外层多1个电子,Z的单质是空气中含量最高的气体,W单质在常温下能被浓硫酸钝化。下列说法正确的是 ( )
A.原子半径:Y<Z<W
B.简单离子半径:Z>W
C.X、Y形成的化合物只含有极性键
D.Y的最高价氧化物对应水化物酸性比Z的强
根据下列有机化合物,回答问题。
 |
(1)上述互为同分异构体的化合物为 ![]() ;
;
(2)写出丙中官能团的名称 ;
(3)丁在一定条件下,可以发生水解反应,生成X、Y两种物质(相对分子质量:X<Y)。由X经下列反应可制得N、F两种高分子化合物,它们都是常用的塑料。

①X转化为M的反应类型是 。
②写出B转化为C的化学方程式 ;
③C与新制氢氧化铜反应的化学方程式为: 。
④在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式为 。
⑤写出3种含有一个羟基、一个酯基的E的同分异构体的结构简式:
、 、 。
某无色溶液中可能含有Na+、K+、![]() 、Cu2+、
、Cu2+、![]() 、
、![]() 、MnO4-、
、MnO4-、![]() 、
、![]() 、
、![]() 。用pH试纸检验该溶液,溶液的pH>7,且往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成了如下实验:
。用pH试纸检验该溶液,溶液的pH>7,且往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成了如下实验:

则关于原溶液的判断中不正确的是
A.肯定不存在的离子是Fe3+、Cu2+、![]() 、
、![]() 、MnO4-,而是否含
、MnO4-,而是否含![]() 另需实验验证
另需实验验证
B.肯定存在的离子是![]() 、
、![]() ,且Na+、K+离子至少有一种存
,且Na+、K+离子至少有一种存
C.若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断
无影响
D.无法确定原溶液中是否存在![]()
甲、乙、丙、丁为四种主族元素,已知甲与乙、丙、丁三元素相邻;甲、乙的原子序数之和等于丙的原子序数,四种元素原子的最外层电子数之和为20。下列判断中,正确的是
A. 原子半径:丙>乙>甲 B. 最外层电子数:丙=丁
C. 气态氢化物的稳定性:甲>丙 D. 最高价氧化物对应的水化物的酸性:丁>甲
下列仪器: ①漏斗 ②容量瓶 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥量筒 ⑦燃烧匙,常用于物质分离的是
A.①③④ B.①②⑥ C.①③⑤ D.③④⑦
一种白色固体可能由Na+、Ba2+、Cl-、Br-、HCO3-、SO32-、SO42-离子中的若干种组成,陶宝同学设计实验检验其组成,记录如下:
| 实验步骤 | 实验操作 | 实验现象 |
| ① | 将固体溶于水,用pH试纸检验 | 无色溶液pH=9 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | 产生气泡,CCl4层呈橙色 |
| ③ | 向②所得水溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列关于固体组成的结论错误的是
A. 肯定不含Ba2+,一定含有Cl- B.至少含有SO32-、SO42-中的一种离子
C. 肯定含有HCO3-和Br- D.无需焰色反应即可断定溶液中含有Na+
- 根据下列反应判断有关物质的还原性由强到弱的顺序正确的是 ( ) ①H2SO3+I2+
- 下列各组物质不属于同分异构体的是() A. 2,2﹣二甲基丙醇和2﹣甲基丁醇 B. 邻氯甲苯和对氯甲苯
- 对于做匀速圆周运动的物体,以下说法正确的是:A.速度和加速度均不变 B. 速度不变,角速度为零C. 速度和加
- 下列关于黄河与长江的说法正确的是 A、都发源于中国地势的第一阶梯,都流经高原气候区、温带季风气候区和亚热带季风气候区 B
- 文献记录片《走近》中有这样一个情节:在西柏坡村的院子里,警卫员给梳头时拔下一根白发,毛打趣的说:“打了三个胜仗,白了一根
- “化学家的主要工作是耕耘元素周期表”,下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题:(1)锂原子的核电荷
- “十月革命一声炮响,给中国送来了马克思主义。”十月革命后,新文化运动进入宣传十月革命,宣传马克思主义的新阶段。下列历史
- 在2016年邵阳市实验操作技能考试中,甲同学抽到了试题四:用量筒量取15.6mL的蒸馏水。则甲同学选用的量筒容积最适宜的
- 关于减数分裂的描述,下列各项中正确的是() A.第一次分裂,着丝点不分裂、同源染色体配对 B.第一次分裂,着丝点分裂、同
- 近年我国首创以Al──空气──海水为能源的新型电池,以海水为电解液.靠空气中的氧使铝不断氧化而产生电流.其工作时电极总反
- _______________________,江春入旧年。
- 如图,已知平行四边形中,,, 为边上的中点,为平行四边形内(包括边界)一动点,则的最大值为 ▲ .
- 突触小体不能完成的生理过程是 A.丙酮酸的氧化分解
- 请结合语境,选出填入下面句子横线处的词语最恰当的一项()一个藐视现在的人,________天才________庸才。天才
- (2011四川泸州,10,2分)如图是一些大小相同的小正方体组成的几何体的主视图和俯视图,则组成这个几何体的小正方体最多
- 已知a、b满足.
- 李某是一国有企业工程师,去年工资收入36000元,奖金8000元,个人专利转让收入5000元;其妻开一家个体杂货店,年收
- 下列解释不正确的一项是( )(2分) A.人迹罕至:少有人来。涉足 :指进入某种环境或生活范围。 B.骊歌:告别
- 材料一:据一份统计报告显示,24岁以下的网民占全国上网总人数的55%,在泡网吧的人群中青少年占80%以上。有的中小学生对
- A month’s _____ is required from whichever party wishes to e



