高三化学试题
脱除烟气中SO2有电化学法及液相催化氧化法等。
(1)Dennis等设计的电化学膜法脱除SO2的工艺如图-1所示。

多孔阳极上发生的电极反应为____;多孔阴极一侧发生的反应包括:
2S2O![]() +2e-=3SO
+2e-=3SO![]() +SO2(g) 、____和2SO3 +2SO
+SO2(g) 、____和2SO3 +2SO![]() = 2S2O
= 2S2O![]() 。
。
(2)研究FeSO4液相催化氧化脱硫的实验流程如图-2所示,循环槽中循环液的pH变化如图-3所示(起始时在脱硫塔中加入9LFeSO4溶液并向循环槽中鼓入空气5min)。

①图-2中设置分析取样点A和B的目的是____。
②脱硫塔中发生的主要反应为____;循环槽中产生的气体为____。
③图-3中430min后脱硫率基本稳定在93.5%左右的原因是____。
配制250mL ![]() 的盐酸溶液时,下列实验操作使配制溶液的浓度偏小的是
的盐酸溶液时,下列实验操作使配制溶液的浓度偏小的是![]()
![]()
A.用量筒量取所需的浓盐酸时俯视刻度线B.定容时,俯视刻度线
C.用量筒量取所需浓盐酸倒入烧杯后,用水洗涤量筒![]() 次,洗涤液倒入烧杯中
次,洗涤液倒入烧杯中
D.定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,可以不管它
某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是

A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动
B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是Fe3++e-= Fe2+
C.闭合K1断开K2,电流从石墨电极经过K1流向铁电极
D.闭合K1断开K2,左侧烧杯中的溶液pH将逐渐降低
在密闭容器中进行N2+3H2![]() 2NH3反应,起始时N2和H2分别为10 mol 和30 mol,当达到平衡时,N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是
2NH3反应,起始时N2和H2分别为10 mol 和30 mol,当达到平衡时,N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是
A、40 mol 35% B、20 mol 30% C、20 mol 70% D、10 mol 50%
向二氯化铂的HCl溶液中通入乙烯气体,再加入KCl可得K[Pt(C2H4)Cl3]·H2O(蔡氏盐),下列有关化学用语表示正确的是
A.KCl的电子式:![]() B.乙烯的结构简式:CH2CH2
B.乙烯的结构简式:CH2CH2
C.中子数为117,质子数为78的铂原子:![]() D. K+的结构示意图:
D. K+的结构示意图:
实验室需要0.1 mol·L-1NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。

(![]() 2)下列操作中,容量瓶所不具备的功能有________(填序号)。
2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液 B.测量容量瓶规格以下的任意体积的液体
C.贮存溶液 D.准确稀释某一浓度的溶液 E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为____![]() __g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1(填“大于”“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时未经冷却,则所得溶液浓度________0.1 mol·L-1。
__g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1(填“大于”“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时未经冷却,则所得溶液浓度________0.1 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
。
下列关于Si、Cl、S等非金属元素单质及其化合物的说法正确的是( )
A. 实验室可用浓硫酸干燥硫化氢
B. 陶瓷、水晶、水泥、玻璃都属于硅酸盐产品
C. 漂白粉变质后的残留固体有碳酸钙
D. 单质氯气及单质硫与铜反应生成的产物中,铜的化合价相同
下列离子方程式错误的是
A.乙酸与碳酸钠溶液反应:2CH3COOH+CO![]() == 2CH3COO--+CO2↑+H2O
== 2CH3COO--+CO2↑+H2O
B.醋酸溶液与新制氢氧化铜反应:
2CH3COOH+Cu(OH)2 —→ Cu2++2CH3COO-+2H2O
C.苯酚钠溶液中通入少量二氧化碳:
2C6H5O-+CO2+H2O ![]() 2C6H5OH+CO
2C6H5OH+CO![]()
D.甲醛溶液与足量的银氨溶液共热
HCHO+4[Ag(NH3)2]++4OH—![]() CO
CO![]() +2NH
+2NH![]() +4Ag↓+6NH3+2H2O
+4Ag↓+6NH3+2H2O
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )
A.A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B.B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C.B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D.原NaOH溶液的物质的量浓度为1.0mol/L
右图是实验室制取乙酸乙酯的装置。则下列说法正确的是

 A.右边导管插入饱和碳酸钠溶液
A.右边导管插入饱和碳酸钠溶液
B.反应结束后管C液体可能会变黑色
C.试管C中加入试剂的顺序是:2mL浓硫酸→3ml乙醇→2mL冰醋酸
D.试管D中油状物在下层,饱和碳酸钠溶液主要为了吸收随乙酸乙酯蒸出的少量乙酸和乙醇
 |
水溶液X中只可能含有K+、Mg2+、Al3+、AlO2—、SiO32—、SO32—、CO32—、SO42—中的若干种离子。某同学对该溶液X进行了如下实验;下列判断正确的是( )
A.气体甲一定是纯净物 B.K+、AlO2—和SiO32—一定存在于溶液X中
C.沉淀甲是硅酸和硅酸镁的混合物 D.凭以上实验能确定SO42—是否存在于溶液X中
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是 ( )
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出
标准状态下,一个容积为a ml 的烧瓶中盛满NO2气体,将其倒立于装有大量水的水槽中。向烧瓶里通入b ml 氧气,最终烧瓶顶端残留c ml 气体。
(1) 写出残留气体可能的分子式
(2)求c (用含有a、b的数学式表示)
在水电离出的C(H+)=10-14mol/L的溶液中,一定能大量共存的离子组是
A.K+、Na+、HCO3—、Cl— B.K+、AlO2—、Br—、Cl—
C.Na+、Cl—、NO3—、SO42— D.Al3+、NH4+、Cl—、SO42—
科学的假设与猜想是科学探究的先导和价值所在.在下列假设或猜想引导下的探究肯定没有意义的是( )
A.探究SO2和Na2O2反应可能有Na2SO4生成 B.探究NO和N2O可能化合生成NO2
C.探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3
D.探究向滴有酚酞试液的NaOH溶液中通入Cl2,酚酞红色褪去的原因是溶液的酸碱性改变还是HClO的漂白作用
汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3===K2O+5Na2O+16N2↑下列说法正确的是:
A.KNO3是还原剂,其中氮元素被氧化 B.生成物中的N2是氧化产物,K2O是还原产物
C.每转移1 mol电子,可生成标准状况下N2的体积为35.84 L
D.若有65 g NaN3参加反应,则被氧化的N的物质的量为3.2 mol
下列4种有机物:
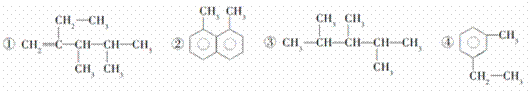
其中一氯取代物的同分异构体数目相同的是 ( )
A. ①和② B. ②和③ C. ①和③ D. ②和④
汽车尾气净化中的一个反应如下:

在一容积为5L的恒容密闭容器中充人0.2 mol NO和0.5mol CO,5 min后该反应达到平衡,此时N2的物质的量为0.06mol。下列说法正确的是( )
A.达到平衡后,若只升高温度,化学平衡正向移动
B.达到平衡后,再通人稀有气体,逆反应速率增大
C.0~5 min内,NO的反应速率为2.4×1 0-3 mol·L一1·min一1
D.使用催化剂,平衡常数不变
 |
25℃时,改变0.1mol·L-1H2SO3溶液的pH,各微粒的物质的量分数(α)变化如图所示,下列说法中错误的是
A.1gK1(H2SO3)=-1.9
B.pH=3时,c(HSO3-)>c(H2SO3)>c(SO32-)
C.反应H2SO3+SO32-![]() 2HSO3-的lgK=5.3
2HSO3-的lgK=5.3
D.pH=7.2时,c(HSO3-)=c(SO32-)=c(H+)
氯化亚砜(SOCl2)是一种液态化合物,在农药、制药行业中用途广泛。实验室合成原理为:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:

已知:①SOCl2 沸点为78.8℃,SCl2 的沸点为50℃,且两种液体可互溶。
②SOCl2 遇水剧烈反应,液面上产生白雾,并带有刺激性气味的有气体产生。
( 1 )实验室制取SOCl2在三颈烧瓶中进行,整个装置所选仪器的连接顺序是:
⑥→_____________________→①,②←____________________(某些仪器可以多次使用)。
(2)仪器a的名称是________,仪器b的作用是_________________________________。
(3)本实验中制Cl2的离子方程式为_________________________________________,本实验中制SO2的化学方程式为__________________________________________________,
SOCl2与水反应的化学方程式为__________________________________________________。
(4)实验结束后,从三颈烧瓶分离出SOCl2的实验操作名称是_________________。若反应中消耗Cl2的体积为896 mL(标准状况,SO2足量),最后得到纯净的SOCl2 7.14 g,则SOCl2的产率为_________________。
- 我国农耕区与牧区的界线大致与下列哪条线相当( ) A.400毫米等降水量线 B.一月0℃等温线C.秦岭—淮河一线
- A government is agroup of people ______ make decisions abou
- 一个物体以初速度v0水平抛出,落地时速度为v,那么物体运动时间是:( )
- 根据拼音写汉字或给加点字注音。(2分) 语文为我们打开了一片丰富多(cǎi)_______的新天地。“长征之歌”
- 苏轼《赤壁赋》中刻画曹操形象的句子是“ , 。”
- 2011年9月29日和11月1日我国分别成功发射了“天宫一号”目标飞行器和“神舟八号”飞船,并圆满实现“天一”与“种八”
- 文化创新的根本目的是 A.继承文化,提升文明 B.促进人类社会的发展 C.推动社会实践的发展
- 以“温馨”开头,发挥想象,精选细节,续写句子。注意:细致描摹让你动容的那个场景,注意锤炼语言,不少于50字。(4分) 温
- 下列说法正确的是( ) A.医疗上常用75%(体积分数)酒精作消毒剂 B.有机食品,就是有机合成的食品 C.加碘食
- 化工行业已合成出一种硬度比金刚石还大的晶体——氮化碳。已知氮化碳中氮元素的化合价为-3,则: (1)它的化学式是
- 细胞外液渗透压感受器、渴觉中枢、体温调节中枢分别位于 () A.下丘脑、下丘脑、大脑皮层 B.下丘脑、下丘脑、下丘脑 C
- 12.罗马帝国时期,除自由民和奴隶的区别外,公民和臣民之间的差别逐渐消失,“这样,至少对自由民来说产生了私人的平等,在这
- 2002年北京的空气质量状况如何呢?请你查阅有关资料,然后用简单随机抽样方法选取该年的30天,记录并统计这30天北京的空
- Height is just one of the thousands of features your genes(基
- 下列词语中加点的字,读音全都正确的一组是 A.狡黠(xiá) 盥洗(huàn) 肖像(xiào) 铩羽
- 某优质大米在我国市场每公斤售价近100元,约为普通大米价格的20倍,但在北京、上海等发达城市其销售状况依然良好。这体现了
- 在△ABC中,角A、B、C所对的边分别为a、b、c,若,则角A的大小为() A. 或 B. C.或D.
- 能正确表示下列反应的离子方程式为( ) A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ B.NH
- 过点A(-1,4),并且与圆(x-3)2+(y+1)2=5相切于点B(2,1)的圆的方程是___________.
- 已知反应:①2H2O(g) =2H2(g) +O2(g) ΔH1 ②Cl2(g)+H2(g)=2HCl ΔH2 ③2C



