高三化学试题
下列有关溶液的说法正确的是( )
A.向10 mL pH=3的醋酸溶液中加入10 mL pH=11的NaOH溶液,混合液的pH=7
B.实验测定,NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>H2CO3
C.NH4Cl溶液加水稀释过程中c(H+)+c(NH3·H2O)=c(OH-)
D.向AgI沉淀中加入饱和KCl溶液,有白色沉淀生成![]() ,说明AgCl比AgI更难溶
,说明AgCl比AgI更难溶
一种回收并利用含碘(I-)废液的工艺流程如下:

(1)“沉淀”中生成CuI的离子方程式为 。

(2) CuSO4的投加量对废水中I-的去除量影响较大,不同投加量(用过量系数表示)下,反应后I-和Cu2+的浓度如上图所示,则适宜的CuSO4过量系数应为 ,分析原因 _______________________ 。
(3) 滤渣转化为碘单质的化学方程式为 ,反应Ⅰ中生成铁与碘的化合物(其中铁与碘的质量比为21:127),则加入的水的作用是_______,反应Ⅱ的化学方程式是 。
(4) 操作Ⅰ包括 、 、过滤。
硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用。试回答下列问题:
⑴向大气中排放NOx可能导致的环境问题有 。(答两点)已知足量NaOH溶液能完全吸收NO2生成氮的含氧酸盐,试写出该反应的离子方程式
。
⑵光导纤维的使用,让人们的生活更加丰富精彩, 是制备光导纤维的基本原料。
⑶氮化硅陶瓷是一种新型无机非金属材料,其化学式为 ,可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了_____________作用。由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉。在烧结过程中,二氧化硅、碳、氮气以物质的量之比3:6:2反应生成两种化合物,该反应的化学方程式为
。
⑷硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源。与“氢能源”比较“硅能源”具有________________________________等更加优越的特点,从而得到全球的关注和期待。
既可以通过单质与单质化合,也可以通过溶液中的复分解反应来制得的化合物是( )
A. FeI2 ![]() B. Al2S3
B. Al2S3 ![]() C. FeCl2
C. FeCl2 ![]() D. FeS
D. FeS
Al、Fe、Cu都是重要的金属元素.下列说法正确的是( )
A.三者对应的氧化物均能溶于水
B.三者的单质放置在空气中均只生成氧化物
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al
(1)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为 。向反应后的溶液中通入少量CO2,反应的离子方程式为 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 (结果保留两位小数)。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式 ,反应中生成0.2mol HNO3,转移的电子数目为 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象 是 。
在两个容积相等的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器的体积一定具有相同的( )
A.原子数 B.密度 C.质量 D.质子数
下列离子方程式书写正确的是
A.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+===Fe3++3H2O
B.次氯酸钙溶液中通入过量的CO2
Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO
C.向100 mL 0.1 mol·L-1的FeBr2溶液中通入0.015 mol的Cl2
2Fe2++4Br-+3C12===2Fe3++2Br2+6Cl-
D.向明矾溶液逐滴加入Ba(OH)2溶液至铝离子刚好沉淀完全
A13++SO![]() +Ba2++3OH-===BaSO4↓+A1(OH)3↓
+Ba2++3OH-===BaSO4↓+A1(OH)3↓
元素周期表的过渡金属中能找到
A.新制农药元素 B.制催化剂元素
C.制半导体元素 D.非金属元素
塑化剂主要用作塑料的增塑剂,也可作为农药载体、驱虫剂和化妆品等的原料。添加塑化剂(DBP)可改善白酒等饮料的口感,但超过规定的限量会对人体产生伤害。其合成线路图如图I所示:
已知以下信息:
①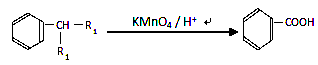
②R1CHO + R2CH2CHO![]()
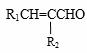 + H2O(—R1、R2表示氢原子或烃基)
+ H2O(—R1、R2表示氢原子或烃基)
③C为含两个碳原子的烃的含氧衍生物,其核磁共振氢谱图如图II所示

请根据以上信息回答下列问题:
(1)C的结构简式为 ,E中所含官能团的名称是 。
(2)写出下列有关反应的化学方程式:
①E和H2以物质的量比1︰1反应生成F: ;
②B和F以物质的量比1︰2合成DBP: ,该反应的反应类型为 。
(3)同时符合下列条件的B的同分异构体有 种,
写出其中任意两种同分异构体的结构简式 。
①不能和NaHCO3溶液反应
②能发生银镜反应
③遇FeCl3溶液显紫色
④核磁共振氢谱显示苯环上只有一种氢原子
X、Y、Z、W是原子序数依次增大的4种短周期元素.X与Z位于同一主族,X原子的最外层电子数是次外层电子数的2倍,Y元素的单质既能与盐酸反应又能与NaOH溶液反应,X、Y、Z、W原子的最外层电子![]() 数之和为18.下列说法不正确的是
数之和为18.下列说法不正确的是
A.X单质在一定条件下能与Z的最高价氧化物发生置换反应
B.原子半径:Y>Z>W
C.最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W
D.室温下,0.1mol/L W的气态氢化物的水溶液的pH=1
向含1 mol HC1和1 mol MgSO4的混合溶液中加入1 mol • L-1的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)的关系图正确的是

在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.NH4+、Ba2+、Cl﹣、NO3﹣ B.K+、AlO2﹣、Cl﹣、SO42﹣
C.Ca2+、Mg2+、NO3﹣、HCO3﹣ D.Na+、Cl﹣、CO32﹣、SO32﹣
.萃取碘水中的碘,可采用的萃取剂是
A.酒精 B.四氯化碳 C.醋酸 D.食盐水
下列关于合金的说法不正确的是( )
A.硬铝比纯铝的硬度低 B.合金中可以含有非金属元素
C.青铜是一种铜锡合金 D.储氢合金是一类能大量吸收H2成金属氢化物的材料
下列有关文献记载中涉及的化学知识表述不正确的是
A.“以曾青涂铁,铁赤色如铜”说明我国古代就掌握了“湿法冶金”技术
B.“墙塌压糖,去土而糖白”中的脱色过程发生了化学变化
C.“丹砂烧之成水银,积变又还成丹砂”讲的是单质与化合物之间的互变
D.“煤饼烧蛎房成灰(蛎房即牡蛎壳)”中灰的主要成分为氧化钙
准确称取6 g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛100 mL某浓度的H2SO4溶液烧杯中,充分反应后过滤,向滤液中加入10 mol·L-1的NaOH溶液,产生沉淀的质量W与加入NaOH溶液的体积V的关系如图所示。

求(1)H2SO4溶液的物质的量浓度是多少?
(2)若A=2.3 mL,铝土矿中Al2O3的质量百分含量是多少?
化学在生产和生活中有重要的应用,下列说法不正确的是
A.二氧化氯和三氯化铁都常用于自来水的处理,但二者的作用原理不同
B.14C 可用于文物年代的鉴定,14C与12C互为同位素
C.C、Si、S都是自然界中含量丰富的非金属元素,三种元素在自然界中既有游离态又有化合态
D.新型材料聚酯纤维,人造纤维都属于有机高分子化合物
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问
题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的
固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是 ;X与过量浓硝酸反应后溶液中含有的盐的化学式为 。
(2)某溶液中有Mg2+、Fe2+、A13+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,
过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 ;
A.Mg2+ B.Fe2+ C.A13+ D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作I的名称是 ;操作II的方法为 。
②Na2CO3溶液可以除油污,原因是(用离子方程式表示) ;
③请完成生成FeCO3沉淀的离子方程式 。
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定
(5Fe2++MnO-4+8H+====5Fe3++Mn2++4H2O)
① 实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要
的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需 。
②该实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
A.稀硝酸 B.稀盐酸 C.稀硫酸 D.浓硝酸
③某同学设计的下列滴定方式,最合理的是 。(夹持部分略去)(填字母序号)

下列各组物质充分反应后过滤,将滤液加热、蒸干至质量不变,最终不能得到纯净物的是( )
A.向含1 mol Ca(HCO3)2的溶液中加入1 mol Na2O2
B.向带有氧化膜的铝片中加入盐酸
C.向漂白粉溶液中通入过量CO2
D.向含1 mol KAl(SO4)2的溶液中加入2 mol Ba(OH)2
- 的展开式中的常数项是 .(用数字表示)
- 下列对南极洲的叙述正确的七大洲中是 ①夜空会有极光出现 ②七大洲中面积最大的洲 ③七大洲中跨纬度最多的洲
- 某市发改委就取暖价格调整举行听证会, 消费者代表提出要兼顾中低收入者的实际情况,最终初拟的综合价格上调40%改为上调25
- 已知角α的终边在直线y=2x上,则tan(α+)的值是.
- ________with the size of the whole earth, the biggest ocean
- 2016年1月7日,M镇召开2015年度党委领导班子成员民主测评会。党委领导班子 成员分别就过去一年的履职情况
- Jim _____ go to the party if he finish(完成)the homework today
- 组成纤维素、纤维素酶和控制纤维素酶合成的DNA的基本组成单位依次是() A.
- 17.阅读下面的文字,按要求作文。 为了在沙漠干旱恶劣的环境中生存,仙人掌把叶片蜷缩成针刺,以减少水分蒸发,在大漠中安营
- 下列春秋时期出现的霸主,曾经用过退避三舍、以退为进的战术打败对手的是( ) A.齐桓公
- 2011年5月17日,重庆市委书记薄熙来在会见“石油魂——大庆精神铁人精神”宣讲总队一行时指出,大庆精神.铁人精神不仅不
- 1842年中英《南京条约》的签订对中国来说最严重的后果是 ( ) A.列强在沿海开放通商口岸
- 下列关于分散系的说法正确的是 A.胶体有比较大的比表面积,能吸附离子使胶体带电荷 B.饱和溶液的导电能力一定比不饱和溶液
- Many new _____ will be opened up in the future for those wit
- 将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表: 物质 丙醇 氧气 水 二氧
- 人体运动系统组成不包括 A、骨 B、 关
- 1,2,3—三苯基环丙烷的3个苯基可以分布在环丙烷环平面的上下,因此有如下2个异构体。据此,可判断1,2,3,4,5—五
- 目前,亚太经合组织成员经贸联系日益紧密……当务之急是争取如期实现茂物目标,并推动世界贸易组织多哈回合谈判早日取得成果。…
- 下列有关氮气的用途中,错误的是 A.制氮肥 B.直接做燃料
- 阅读材料,完成下列各题。 材料一 《明史·职官志》载,自景泰后“六部承奉旨意,靡所不领。阁权益重……嘉靖以后,朝位班次



