高三化学试题
下列说法不正确的是
A.反应MgO(s) +C(s)=Mg( s) +CO(g) 在室温下不能自发进行,则该反应的△H>0
B.原电池输出电能的能力取决于组成原电池的反应物的氧化还原能力
C.0.1mol.L CH3COOH 溶液加水稀释后,溶液中![]() 值减小
值减小
D.锅炉中沉积的CaSO4 可用饱和Na2CO3 溶液浸泡,再将不溶物用稀盐酸溶解除去

通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一。对下列反应的推断或解释正确的是
| 选项 | 操作 | 可能的实验现象 | 解释 |
| A | 向FeCl2溶液中滴入用硫酸酸化的H2O2溶液 | 溶液变黄 | 发生氧化还原反应,且氧化性:H2O2>Fe3+ |
| B | 将CO2 通入Ba(NO3)2溶液中 | 有白色沉淀生成 | CO2与Ba(NO3)2反应生成BaCO3 |
| C | 某溶液中加入硝酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| D | 向淀粉-KI溶液中通入少量Cl2 | 溶液变蓝 | Cl2与淀粉发生显色反应 |
在图1所示的转化关系中,A、B、C分别为三种短周期元素组成的单质、其余均为它们的化合物,其中A、X、Z的晶体类型相同,y的分子与N2互为等电子体,B的一种同素异形体D的晶胞如图2所示


(1)图2对应的物质名称是______,其晶胞中的原子数为___________。
(2)A中基态原子核外电子占据的最高能级符号为_________,其电子排布图为_______________。
(3)Z晶体与A晶体的结构相似,组成Z的两种元素的原子的位置是交替的。在Z晶体中最小环上有____个原子;Z晶体与A晶体相比较,Z晶体熔点高,其原因是_____________________,在X晶体中,原子采取sp3杂化的元素有 种。
(4) Z晶胞如图3所示,![]() 键的键能为akJ·mol-1,理论上分解1mol Z形成气态原子所需的能量为_______kJ(用含a的式子表示) 。
键的键能为akJ·mol-1,理论上分解1mol Z形成气态原子所需的能量为_______kJ(用含a的式子表示) 。
表示一种原子 表示另一种原子
![]()
![]()

图 3
(5)w - 离子与SiCl4互为等电子体,则w - 离子中的中心原子对应的元素在元素周期表中位于_____族(填写族的符号),w - 离子的空间构型为_________。
(6)氧化物MO的电子总数与Z的相等,则M单质晶体的堆积模型为_________________________________。
二苯并呋哺的结构简式为![]() ,其一氯代物有( )
,其一氯代物有( )
A.3种 B.4种
C.5种 D.6种
单质碳和氧化铜在一定温度下反应时,氧化铜可被还原为Cu2O、Cu。现将2.00 g C与 16.0g CuO的混合物,隔绝空气加热一段时间后,将生成的气体通过足量的澄淸石灰水, 共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是( )
A.反应后的固体混合物中还含有碳。
B.反应后的固体混合物中Cu的质量为12.8 g。
C.反应后的固体混合物总质量为14.4 g。
D.反应后的固体混合物中氧化物的物质的量为0.05mol。
下列化学实验事实及其解释或结论都正确的是
A.测定同温度下相同浓度的Na2CO3和Na2SO3溶液的pH,前者大于后者,说明碳元素非金属性弱于硫元素
B.向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再加入0.5 mL有机物X,加热后未出现砖红色沉淀,说明X中不含有醛基
C.往苯酚的浊液中加入Na2CO3溶液,溶液变澄清,说明酸性:苯酚>HCO3—
D.向浓度均为0![]() .1 mol•L﹣1的MgCl2、CuCl2混合溶液中逐滴加入氨水,首先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]
.1 mol•L﹣1的MgCl2、CuCl2混合溶液中逐滴加入氨水,首先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]
向20 mL 0.5 mol/L的氨水中逐滴加入等物质的量浓度的盐酸,测定溶液的温度变化如图所示。下列关于混合溶液的说法错误的是
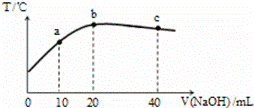
A.从a点到b点,混合溶液不可能存在:c(Cl-)=c(NH4+)
B.由水电离的c(H+):b点>c点
C.氨水的电离平衡常数:b点>a点
D.b焦到c点,混合溶液中可能存在:c(Cl一)>c(H十) >c(NH4+)>c(OH-)
)已知2NO2![]() N2O4。下图中,容器甲内充有0.1 mol NO气体,干燥管内装有一定量的Na2O2,从A处缓慢通入CO2气体,恒温下,容器甲中活塞缓慢地由B向左移动,当移至C处时,容器甲体积缩小至最小,为原体积的9/10,随着CO2的继续通入,活塞又逐渐向右移动。
N2O4。下图中,容器甲内充有0.1 mol NO气体,干燥管内装有一定量的Na2O2,从A处缓慢通入CO2气体,恒温下,容器甲中活塞缓慢地由B向左移动,当移至C处时,容器甲体积缩小至最小,为原体积的9/10,随着CO2的继续通入,活塞又逐渐向右移动。

(1)已知当活塞移至C处时,干燥管中物质增加了2.24 g,此时通入的CO2气体在标准状况下为多少L?容器甲中NO2转化为N2O4的转化率为多少?
(2)当活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至B处,则a值必小于0.01,其理由是 。
一种新型的合成氨的方法如图所示,下列说法正确的是( )

A.反应①属于“氮的固定”
B.反应②属于氧化还原反应
C.反应③可通过电解LiOH水溶液实现
D.上述三步循环的总结果为:N2+3H2=2NH3
化学与社会、生活密切相关,下列有关说法不正确的是 ( )
A.利用清洁能源代替化石燃料,有利于节约资源、保护环境
B.食品添加剂种类很多,其中的一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐
C.抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等
D.乙醇属于可再生能源
将1 mol金属Al全部转化为Al(OH)3,过程中共消耗HCl a mol、NaOH b mol,则a+b最小值为( )
A、1.5 B、6 C、8 D、2
用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,不需要使用的玻璃仪器是
A.容量瓶 B.玻璃棒 C.漏斗 D.烧杯
短周期主族元素a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;x、y、Z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25℃时,0.1 mol•L-1w溶液中,![]() =1.0×10-10。上述物质的转化关系如图所示。下列说法正确的是
=1.0×10-10。上述物质的转化关系如图所示。下列说法正确的是

A.原子半径的大小:a<b<c<d B.氢化物的沸点:b>d
C. x的电子式为:![]() D.y、w含有的化学键类型完全相同
D.y、w含有的化学键类型完全相同
实验室欲配制100 mL 0.92 mol•L-1的H2SO4溶液(本小题每空2分,共14分)
(1)需要用到的仪器,除了烧杯、空试剂瓶、玻璃棒、量筒、还必须有 ;
(2)若提供的是18.4 mol•L-1的浓H2SO4,求所需量取的浓H2SO4的体积为 mL;
(3![]() )对配制过程中的下列说法,正确的是 。(填序号,多选、少选均不得分)
)对配制过程中的下列说法,正确的是 。(填序号,多选、少选均不得分)
A.量筒量取浓硫酸后要冲洗并将冲洗液一起倒入小烧杯
B.量好体积的浓硫酸应先倒入小烧杯中然后再加水稀释
C.稀释好的稀硫酸要立即转移入容量瓶
D.若定容后摇匀液面又下降了。则必须再补加水至刻度线。
(4)配制稀硫酸的容量瓶必须洗涤,若用含有蒸馏水的容量瓶未干燥就配制稀硫酸,
则所配稀硫酸浓度将 (偏高、偏低、不变);若用刚配制过NaOH
溶液的容量瓶未洗涤就配制稀硫酸,则所配制的稀硫酸溶液的浓度将
(偏高、偏低、不变);若用刚配制过HCl溶液的容量瓶未洗涤就配制稀硫酸,则
所配制稀硫酸浓度将 (偏高、偏低、不变),
氢离子浓度将 (偏高、偏低、不变)。
钠着火后,可用于灭火的物质或器材是( )
A.水 B.泡沫灭火器 C.干冰灭火剂 D.干砂
已知高温下能发生如下反应SiO2+2C==Si+2CO↑,Si+C==SiC, 现有石英砂和碳粉的混合物 l mol,在高温电炉中隔绝空气充分反应完全后,冷却得到残留固体。若石英砂与混合物的物质的量之比为x(0<x<1), 试讨论x的取值范围,残留固体的成分和物质的量, 并将结果填入下表:
| 编号 | ① | ② | ③ | ④ | ⑤ |
| x值 | x= | ||||
| 残留固体及 物质的量 | Si |
将V1 ml 1.0 mol/L HCl溶液和V2 ml未知浓度的NaOH溶液混合均匀后测量并记录溶液的温度,实验结果如图所示(实验中始终保持V1+V2==50 ml)。下列叙述中不正确的是

A.当V1==30 ml时,盐酸和NaOH溶液恰好完全反应
B.NaOH溶液的浓度约为1.5 mol/L
C.做该实验时环境温度为22℃
D.该实验表明化学能可以转化为热能
下列关于化学键的说法正确的是( )
A.只存在于分子之间
B.只存在于离子之间
C.相邻原子之间的强相互作用
D.共价键只能存在于共价化合物中
现有 0.175 mol·L-1醋酸钠溶液500 mL,(已知室温下,醋酸的电离平衡常数Ka=1.75×10-5)。
⑴ 写出醋酸钠水解反应的化学方程式 ;
⑵ (双选) 下列图象能说明醋酸钠的水解反应达到平衡的是 ;


⑶ (双选) 向醋酸钠溶液中加入少量下列物质,水解平衡向正向移动的有 ;
A.冰醋酸 B.纯碱固体 C.醋酸钠固体 D.氯化铵固体
⑷ (双选) 在醋酸钠溶液中加入冰醋酸,溶液中微粒浓度的关系式能成立的有 ;
A.c(CH3COO-) + c(CH3COOH) > c(Na+)
B.c(Na+) > c(CH3COO-) > c(H+) > c(OH-)
C.c(CH3COO-) > c(Na+) > c(H+) > c(OH-)
D.c(CH3COO-) > c(H+) > c(OH-) > c(Na+)
⑸ 欲配制0.175 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案:
方案一:用托盘天平称取 g无水醋酸钠,溶于适量水中,配成500 mL溶液。[已知:M(CH3COONa) = 82g/mol ]
方案二:用体积均为250 mL且浓度均为 mol·L-1的醋酸与氢氧化钠两溶液混合而成(设混合后的体积等于混合前两者体积之和)。
⑹ 在室温下,0.175 mol·L-1醋酸钠(CH3COONa)溶液的pH约为 。
下列说法正确的是( )
A.t℃时,某溶液的pH=6,则该溶液一定为酸性
B.常温下,将pH=11的氨水稀释后,溶液中所有离子的浓度均降低
C.常温下,将pH=11的NaOH溶液和pH=3的CH3COOH溶液等体积混合后,溶液pH<7
D.常温下,物质的量浓度和体积相同的K2CO3、K2SO4、HC1溶液混合后,溶液的pH<7
- 读我国部分地区气温年较差分布图(单位:℃),回答问题。 (1)该区气温年较差的分布规律是
- 用适当的化学用语填空: (1)两个亚铁离子; (2)3个氧化钠分子; (3)纯碱; (4)含氯元素的氮肥.
- 关于甲醛-化学式为 CH2O 和甲醇-化学式为CH3OH的说法正确的是: A.甲醛和甲醇中都含有一个碳原子
- 形成天体系统的条件是() A.重量和体积 B.相互吸引和相互绕转 C.数量和亮度 D.物质组成和
- 在下面语段画线处选填一组连贯、恰当的语句。( ) ______________。书能教你为人宽厚,心地善良,使你生
- 用班氏试剂鉴别健康人的下列四种液体,出现红黄色沉淀的是 A.血清 B.唾液 C.胃液 D.尿液
- 把二次函数y=2x2-4x+5化成y=a(x-h)2+k的形式是 ,其图象开口方向 ,顶点坐标是 ,当x
- I have been to Beijing ________. A. one time B.twice C
- 已知f(x5)=lgx,则f(2)等于( )A.lg2 B.lg32
- 古诗文默写。 (1)《陋室铭》中概括全文主旨的句子是:斯是陋室, 。
- 1. 单词拼写根据句子意思及所给的中文或首字母提示完成单词,请将完整的单词写在右边的横线上。每空一词。 1.I’m g
- 下列溶液中Cl﹣的物质的量浓度与50mL 1mol/L FeCl3溶液中Cl﹣物质的量浓度相等是()A. 100mL 1
- —Whatplace is it? —Haven’t you seen that we back where we
- 微博(微博客MicroBlog的简称)是一个信息分享、传播以及获取平台。2010年被人们称为“微博元年”,两年来我国参与
- 为了强调物理学家对当今社会的重要作用并纪念爱因斯坦,2004年联合国第58次大会把2005年定为国际物理年,爱因斯坦在1
- 在光滑的水平面上有A、B两辆质量均为m的小车,保持静止状态,A车上站着一个质量为m/2的人,当人从A车跳到B车上,并与B
- 北京时间2012年6月18日14时07分,从酒泉发射的神舟九号飞船与天宫一号顺利实现对接。据此完成5~6题。5.
- 既能传导兴奋,又能分泌激素的结构是( ) A.垂体 B.下丘脑 C.胰岛 D.甲状腺
- 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是 A.a和b不连接时,铁片上会有金属铜析出 B.a和b用导线连接
- Form their ________ on the top of the TV Tower, visitors can



