高三化学试题
碳及其化合物在生活、化工领域发挥着重要的作用。试回答下列问题:

(1)有科学家提出由CO2制取C的太阳能工艺如图1所示。若重整系统发生的反应中![]() ,则重整系统中发生反应的化学方程式为______________。
,则重整系统中发生反应的化学方程式为______________。
(2)以CO2为原料利用电解法可制取乙烯,其装置如图2 所示。电极a为电源的_____(填正极”或“负极” ),溶液中的H+由_______(填“阴”或“阳”,下同)极区流向____极区。
(3)草酸锌可应用于有机合成、电子工业等。工业上制取ZnC2O4的原理如图3 所示(电解液不参加反应),Zn电极是________(填“正” “负”“阴”或“阳”)极。己知在Pb电极区得到ZnC2O4,则Pb电极上的电极反应式为_________________。
下图为氮及其化合物的类别与化合价对应的关系图。

(1)实验室制取氨气。
① 化学方程式是 。
② 可用向下排空气法收集氨气的原因是 。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是 。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2 ![]() 2NO。
2NO。
b. 氨的催化氧化:_________。
② 体现N元素的氧化性:_________。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。

① NO2溶于水的化学方程式是_________。
② 使试管中NO2完全被水吸收的操作是________。

科学家设计了一种可以循环利用人体呼出的CO2并提供O2的装置,总反应方程式为2CO2=2CO+O2。下列说法正确的是 ( )
A.由图分析N电极为电池的正极
B.阴极的电极反应为CO2+H2O+2e-=CO+2OH-
C.OH-通过离子交换膜迁向左室
D.反应完毕,该装置中电解质溶液的碱性增强
下图表示了中学化学中几种常见物质的转化关系,图中省略了部分产物和反应条件,已知常温下,B、G是液体,X、H是固体且两者化学式量相差1,其余物质均为气体,

试回答下列问题:
(1)X的化学式分别为: ,A的电子式是: 。
(2)反应①的化学方程式为: 。
(3)反应②的离子方程式为: 。
(4)在标准状况下收集到5.6L气体E,则参加反应的H为 g
四种短周期元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是
A.W的氢化物分子之间都能形成氢键
B.气态氢化物的稳定性Y>Z
C.W、X、Y三种元素组成的化合物的水溶液一定呈中性
D.W与X形成的化合物中只存在离子键
反应2A(g)![]() 2B(g)+C(g)(正反应为吸热反应),达到平衡时,要使逆反应速率降低,A的浓度增大,应采取的措施是 ( )
2B(g)+C(g)(正反应为吸热反应),达到平衡时,要使逆反应速率降低,A的浓度增大,应采取的措施是 ( )
A.减压 B.降温 ![]() C.加压 D.增大B的浓度
C.加压 D.增大B的浓度
下列说法中正确的是 ( )
A.第ⅦA族单质从上往下熔沸点逐渐升高,第ⅠA族单质从上往下熔沸点逐渐降低
B.Na2SiO3溶液可用作矿物胶、木材防火剂,还可用作制备硅胶的原料
C.品红溶液和滴有酚酞的NaOH溶液均能与SO2气体作用而褪色,且其实质相同
D.镁和铝性质稳定且都有很强的抗腐蚀能力,所以镁铝合金可用于飞机、轮船制造
在下列有关说法中正确的是
① 相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4 > C2H4 >C2H2
② 对于任意比混合的乙烯、丙烯和环丁烷混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不改变
③ 所有烷烃分子中的碳原子均为sp3杂化
④ 某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2∶3,则该有机物的肯定为烷烃
⑤ 所有氨基酸均为两性化合物,既能与盐酸反应又能与氢氧化钠溶液反应。
A、只有①②③ B、只有①②③⑤ C、只有①②④⑤ D、①②③④⑤
下列实验操作所得的现象及结论均正确的是
| 实验操作 | 现象及结论 | |
| A | 将AlC13溶液加热蒸干 | 得到白色固体,成分为纯净的AlC13 |
| B | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,则Na2SO3已变质 |
| C | 向Na2SiO3溶液中通入CO2 | 有白色沉淀产生,则碳酸的酸性比硅酸强 |
| D | 向FeI2溶液中通入少量C12 | 溶液变黄,则C12的氧化性强于Fe3+ |
四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃。分液漏斗中放浓盐酸,仪器a中放MnO2,二者用于制氯气,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)。请回答下列各问题。

(1)仪器a、b的名称分别是______、________,仪器b的作用是__________________。
(2)图中装置F与装置G之间连接干燥管的目的是______________________________。
(3)装置D中Sn发生反应的化学方程式为___________;装 置 G 的作用是____________。
(4)装置B中的试剂是______________________;装置C的作用是_________________。
(5)实验过程中。当观察到________时,即可熄灭装置D处的酒精灯。
(6)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,请写出四氯化锡水解的化学方程式______________________________________。
下列离子方程式书写正确的是
A.氯气通入水中:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B.将1mol Cl2通入含1 mol FeI2溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2
C.小苏打溶液与少量橙清石灰水混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.NH4Al(SO4)2溶液中加入足量Ba(OH)2溶液:
NH4++Al3++2SO42一+2Ba2++5OH-=NH3·H2O+AlO2-+2BaSO4↓+2H2O
利用天然气可制备合成气,进而制备甲醇等化工原料。
 (1)如图是以甲烷、氧气和水蒸气为原料制备合成气的能量图,某工厂为实现能量的零排放和零补充,则进料气中氧气与水蒸气的体积比为 。
(1)如图是以甲烷、氧气和水蒸气为原料制备合成气的能量图,某工厂为实现能量的零排放和零补充,则进料气中氧气与水蒸气的体积比为 。
(2)11.2 L CH4(g)(标准状况)不完全燃烧生成CO(g)和H2O(g),放出的热量为_____________________。
(3)以H2、CO为原料合成甲醇:
![]()
![]() 。在1L恒容密闭容器中充入2a mol H2(g)和a mol CO(g),在一定条件下进行10 min达到平衡,测定CO的转化率为
。在1L恒容密闭容器中充入2a mol H2(g)和a mol CO(g),在一定条件下进行10 min达到平衡,测定CO的转化率为![]() 。若改变某个条件,反应速率减慢,CO的平衡转化率增大。
。若改变某个条件,反应速率减慢,CO的平衡转化率增大。
①反应开始至10 min时间内H2的平均反应速率为 。
②上述平衡的平衡常数K为 。
③上述改变的某个条件是指 。
④上述反应达到平衡状态时,甲醇的体积分数为 。
下列说法不正确的是
A.煤属于生物质能 B.氢气是理想的绿色能源
C.地沟油可加工成航空煤油 D.沼气属于可再生能源
2SO2(g)+O2(g)![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A. 加入催化剂可加快该反应的速率,从而提高SO2的转化率
B. 增大反应体系的压强,反应速率一定增大
C. 该反应是放热反应,故温度越低,对提高SO3的日产量越有利
D. 在2min时间内,SO2的浓度由6 mol/L变为3 mol/L,则在相同时间段内,SO3(g)生成的平均速率为1.5 mol/(L·min)
锂空气电池充放电基本原理如下图所示,下列说法不正确的是
 A.充电时,锂离子向阴极移动
A.充电时,锂离子向阴极移动
B.充电时阴极电极反应式为
Li++e-===Li
C.放电时正极电极反应式为
O2+4e-+2H2O===4OH-
D.负极区的有机电解液可以换成水性电解液
下列离子方程式书写正确的是: ( )
A.用铂电极电解氯化镁溶液:Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH-===BaSO4↓+H2O
C.在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+====2Mn2+ +5O2↑+8H2O
D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br +OH-![]() CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O
某小组设计不同实验方案比较Cu2+、Ag+的氧化性。
(1)方案1:通过置换反应比较:向酸化的AgNO3溶液插入铜丝,析出黑色固体,溶液变蓝。反应的离子方程式是 ,说明氧化性Ag+>Cu2+。
(2)方案2:通过Cu2+、Ag+分别与同一物质反应进行比较

①经检验,I中溶液不含I2,黄色沉淀是 。
②经检验,II中溶液含I2.推测Cu2+做氧化剂,白色沉淀A是CuI。确认A的实验如下:

a.检验滤液无I2。溶液呈蓝色说明溶液含有 (填离子符号)。
b.白色沉淀B是 。
c.白色沉淀A与AgNO3溶液反应的离子方程式是 ,说明氧化性Ag+>Cu2+。
(3)分析方案2中Ag+未能氧化I-,但Cu2+氧化了I-的原因,设计实验如下:

(电极均为石墨,溶液浓度均为1 mol/L,b、d中溶液pH≈4)
①a中溶液呈棕黄色的原因是 (用电极反应式表示)。
②“实验3”不能说明Cu2+氧化了I-。依据是空气中的氧气也有氧化作用。设计实验证实了该依据,实验方案及现象是 。
③方案2中,Cu2+能氧化I-,而Ag+未能氧化I-的原因: 。
(资料:Ag++I-=AgI↓ K1=1.2×1016;2Ag++2 I-=2Ag↓+I2 K2=8.7×108)
温度为T K时,将 0.40 mol A气体充入2. 0 L固定容积的密闭容器中,发生反应A(g) ![]() 2B(g) ΔH>0,经过一段时间后达到平衡。反应过程中测得的部分数据见下表:
2B(g) ΔH>0,经过一段时间后达到平衡。反应过程中测得的部分数据见下表:
| 时间/s | 0 | 20 | 40 | 80 | 100 |
| n(A)/mol | 0.40 | 0.20 | 0.10 | ||
| n(B)/mol | 0 | 0.24 | 0.60 | 0.60 |
下列说法正确的是( )
A.0~40 s的平均反应速率v(B)=0.01 mol·L-1·s-1 B.T K时该反应的平衡常数为3.6
C.相同条件下,若起始时充入0.80 mol A,则达到平衡时c(B)小于0.60 mol·L-1
D.相同条件下,若起始时向容器中充入0.05 mol A、0.70 mol B,则反应达到平衡前v(正)>v(逆)
苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
A.相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B.提高CO2充气压力,饮料中c(A-)不变
C.当pH为5.0时,饮料中![]() =0.16
=0.16
D.碳酸饮料中各种粒子的浓度关系为:![]() c(H+)=c(HCO3-)+c(CO32-)+c(OH-)-c(HA)
c(H+)=c(HCO3-)+c(CO32-)+c(OH-)-c(HA)
2016年8月国际期刊eLife上发表了浙江医科大学第二医院和浙江大学肿瘤研究的晁明和胡汛等人的一片论文,引发轰动。媒体以廉价的小苏打协助饿死了癌细胞予以报道。在实验室中模拟工业制取NaHCO3的实验步骤如下:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让某一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:分离C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的某固体粉末,有NH4Cl晶体析出。
(1)下图所示装置的连接顺序是:a接 ; 接 ;![]() 接 (填接口编号)
接 (填接口编号)
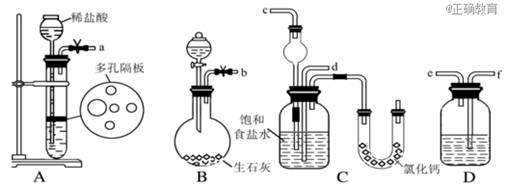
(2)检查A装置气密性的具体操作是 。
(3)A中常选用的固体反应物为 ;D中应选用的液体为 。
(4)装有无水CaCl2的U形管的作用是 。
(5)第四步所得的晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单实验,不使用其他任何试剂,证明所得晶体大部分是NH4Cl。简要写出操作和现象
。
- 当前的许多流行语都产生于中国语言创新最活跃的地方——互联网。“喜大普奔”是极受青睐的一个,表达极度激动和热情。它把“喜闻
- 宪法通过后共和派在众议院选举中获得多数席位。1877年支持君主制的法国总统麦克马洪迫使亲共和的内阁辞职,并解散众议院。共
- 作文 请以“为你而歌”为题写一篇不少于600字的作文。 要求:①除诗歌、剧本以外,文体不限。 ②文中不得出现真实的人名、
- —My brother hurt his legs when he rode his bike on the way
- (4分)小明想找到一种让物体快速冷却的方法.为此小明进行了如下的探究:小明注意到妈妈是把饭菜放在空气中冷却的,而厨房中适
- ______ I have will be yours sooner or later. A. Whatever
- 在研究同种哺乳动物的3个个体的2对相对性状时,发现其基因组成:甲为DBb;乙为DdBB;丙为dBb。下列推断错误的是 A
- 当人用手指将双耳堵住后,可出现的情况是:A.完全失去听觉; B.对听觉
- 诗人左思在其《咏史》中沉郁悲歌:“世胄蹑高位,英俊沉下僚。地势使之然,由来非一朝。”造成这一社会状况的制度原因是 A.征
- 某一动物死后,它所有的生理机能都停止了活动,当把它焚烧后,这一动物就不存在了。这说明 A. 物质的运动停止了
- “一山难容二虎”这一谚语,用生物学观点可以理解为( ) A.虎性情孤独,不群居 B.虎所需的生活空间很大 C.身
- A year after graduation, I was offered aposition teaching a
- 阅读下面的文字,完成题。 春天的梦 苏叔阳 黎明,窗外飘着雪花,静静地,静静地……啊,多像梦的使者。蓦地,几行诗句涌上心
- 读沿北回归线的东西向某剖面图,完成下列问题。 图15
- 随机抽取某中学甲乙两班各10名同学,测量他们的身高(单位:cm),获得身高数据的茎叶图如图7. (1)根据茎叶图判断哪个
- 一定量的石灰石与50g稀盐酸恰好完全反应,生成CO2 2.2g,求:(1)参加反应的CaCO3的质量;(2)盐酸的溶质质
- 花生油主要是从花生种子的( )中榨出来的。 A、胚根 B、胚芽 C、胚轴 D
- 国务院国资委10月22日公布的数据显示,今年上半年中央企业累计实现营业收入96874.6亿元,应交税费总额8514.2亿
- 3.填入下面一段文字横线处的语句,最恰当的一句是( ) 大数据的发展要遵循实践应用与理论升华相结合的科学路径
- 叶芽能发育成枝条,下列对叶芽发育的说法不正确的是 A.幼叶发育成叶 B.芽轴发育成茎 C.叶原基发育成幼叶



