高三化学试题
下列实验操作或装置符合实验要求的是( )

A.装置Ⅰ可用于测定中和热
B.装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
C.装置Ⅲ可用于高温煅烧石灰石
D.装置Ⅳ可用于吸收易溶于水的尾气
实验室需要0.80 mol·L-1 NaOH溶液475 mL 和0. 40 mol·L-1硫酸500 mL。根据这两种溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是__________(填编号),配制上述溶液还需用到的玻璃仪器是__________(填仪器名称)。
(2)容量瓶所不具备的功能有__________(填编号)。
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.贮存溶液
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度__________0.80 mol·L-1(填“大于”、“小于”或“等于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度____________0.80 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL的量筒,最好选用________mL的量筒。
取一定质量的Cu2O和CuO混合粉末,将其均匀混合后分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为
A. 3.6mol/L B. 3.2mol/L C. 2.8mol/L D. 2.4mol/L
目前的锂离子电池的正极材料多是LiCoO2、LiMn2O4、LiFePO4和双离子传递型聚合物等。改良正极材料的性能是锂离子电池领域的重点方向,如用碳包覆LiFePO4和向其中掺杂金属银等。下列过程是制备该正极材料的流程图:

回答下列问题:
(1)LiFePO4中铁元素的化合价为 价。已知原料是Li2CO3、FeC2O4·2H2O、NH4H2PO4和C6H12O6的混合物,其中Li、Fe、P三种元素的物质的量比为1:1:1,C6H12O6的用量占原料总质量的5%。若原料的质量为1000g,则需要称取NH4H2PO4的质量为 (保留两位小数)。
(2)将原料先行研磨4h目的是 。为了更快得到前驱体粉末,除了保持温度在50℃外,还应进行的常见操作方法是 。
(3)两次焙烧均需要在高纯氮气环境下进行,原因是 。葡萄糖分解产生的碳除了提供还原性环境,提高产物纯度,而且可以阻止晶粒的聚集长大,控制颗粒形状,提高LiFePO4的电导率。则葡萄糖分解的化学反应方程式(分解过程中只有C一种单质生成)为 。600℃加热时硝酸银发生分解生成红棕色气体和3种常见单质(其中两种气体单质物质的量比为2:7),则分解时的化学反应方程式为 。
(4)如图所示是用LiFePO4/Ag/C做正极材料制成的纽扣锂离子电池组装示意图。充电时,其正、负极材料所发生反应的电极方程式分别是 、 (锂离子电池是靠xLi+在两极的嵌入和嵌出进行工作)。

NA为阿伏伽德罗常数,下列叙述错误的是( )
A.标准状况下,足量Fe与22.4L Cl2反应,转移电子数为3NA
B.18g水中含有的电子数为10NA
C.28g CO和N2混合气体中含有原子总数为2NA
D.1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去电子数为NA
下列物质能发生消去反应的是( )
A.CH3Br B. ![]() C.
C.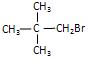 D.
D.
下表中实验操作、现象和所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用激光笔照射鸡蛋白水溶液 | 有丁达尔效应 | 鸡蛋白分子直径介于1nm~100nm |
| B | 向某氯化亚铁溶液中加入Na2O2粉末 | 出现红褐色沉淀 | 说明原氯化亚铁已氧化变质 |
| C | 碳酸的盐X加热分解,产生的气体通入酸化的BaCl2溶液 | 产生白色沉淀 | X可能是NaHCO3 |
| D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y一定是Cl2 |
市售食盐常有无碘盐和加碘盐(含KIO3和少量的KI)。
I. 某同学设计检验食盐是否为加碘盐的定性实验方法:
①取待检食盐溶于水,加入稀硫酸酸化,再加入过量的KI溶液,振荡。
②为验证①中有I2生成,向上述混合液中加入少量CCl4充分振荡后,静置。
(1)若为加碘盐,则①中发生反应的离子方程式为_________。
(2)②中的实验操作名称是_________。
(3)实验过程中能证明食盐含KIO3的现象是_________。
Ⅱ. 碘摄入过多或者过少都会增加患甲状腺疾病的风险。目前国家标准(GB/T13025.7)所用的食盐中碘含量测定方法:
①用饱和溴水将碘盐中少量的I-氧化成IO3-。
②再加入甲酸发生反应:Br2+HCOOH=CO2↑+2HBr。
③在酸性条件下,加入过量KI,使之与IO3-完全反应。
④以淀粉作指示剂,用Na2S2O3标准溶液进行滴定,测定碘元素的含量。
I2+2Na2S2O3=2NaI+Na2S4O6
(1)①中反应的离子方程式为_________。
(2)测定食盐碘含量过程中,Na2S2O3,与IO3-的物质的量之比为_________。
(3)有人提出为简化操作将①、②省略,但这样会造成测定结果偏低。请分析偏低![]() 原因:__________________。
原因:__________________。
下图是用明矾[KAl(SO4)2・12H2O]为主要原料制取Al2(SO4)3和K2SO4的操作步骤流程图(图中略去了沉淀物的洗涤操作)

分析图中圆括号内应填入何种试剂,使用何种分离方法,并回答下列问题。
(1)试剂a是_____________,b是_____________,c是_____________,
分离方法①是_____________,②是_____________,③是_____________。
(2)用离子反应方程式表示下列转化过程:
明矾溶液+a![]() A+B:___________________________________________。
A+B:___________________________________________。
B+C![]() E:____________________________________________________。
E:____________________________________________________。
(3)按上述操作不考虑损耗在理论上158 g明矾最多可制得Al2(SO4)3・18H2O_____g,
至少可制得K2SO4_______g。
在容积为2.0 L的密闭容器内,物质D在T ℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是 ( )

A.从反应开始到第一次达到平衡时, A物质的平均反应速率为0.0667 mol/(L·min)
B.该反应的化学方程式为2D(s)![]() 2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
C.已知:反应的∆H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D.若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.0.1 mol·L-1 Na2S溶液中含有0.2 NA个Na+
B.标准状况下,22.4 L 的H2O含有2NA个氢原子
C.常温下,44 g CO2含有NA个氧原子
D.0.1 mol Na与足量O2反应生成Na2O,转移0.1 NA个电子
[选修3—物质结构与性质]
CuSO4和Cu(NO3)2是自然界中重要的铜盐。请回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子的核外价电子排布式为 ,S、O、N三种元素的第一电离能由大到小的顺序为 。
(2)NO3-的立体构型是 ,与NO3-互为等电子体的一种非极性分子为 (填化学式)。
(3)CuSO4的熔点为560°C,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是 。
(4)往CuSO4溶液中加人过量NaOH能生成配合物[Cu(OH)4]2-。不考虑空间构型,
[Cu(OH)4]2-的结构可用示意图表示为(用箭头表示出配位键的位置)_______。
(5)化学实验室常利用新制氢氧化铜检验醛基的存在,乙醛分子中碳原子的杂化方式为 。
(6)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如下图所示。

该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(![]() ,
,![]() ,
,![]() )。则D原子的坐标参数为 ,它代表 原子。
)。则D原子的坐标参数为 ,它代表 原子。
已知某有机物中碳、氢原子个数比为1∶2。取wg该有机物在氧气中充分燃烧,消耗O2的体积在标准状况下为VL,产物只有CO2和H2O,其质量分别为w1g和w2g。
(1)通过计算确定该有机物中是否含氧,至少需上述数据中的 个,有 种
组合。将上述组合填入下表的空格中(不必填满)。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)若该有机物含有氧,则w1、w2应满足的关系是_________;若该有机物不含氧,则w、V应满足的关系是____________。
(3)从上表中任取一组数据,能否确定该有机物的分子式?_________,其原因是_________________________________________________________。
下列“实验现象”和“结论”都正确且有因果关系的是
| 选项 | 操作 | 实验现象 | 结论 |
| A | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 融化后的液态铝滴落下来 | 金属铝的熔点低 |
| B | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液中含有钠盐 |
| C | 向盛有酸性高锰酸钾溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 | 乙烯发生氧化反应 |
| D | 将20℃ 0.5 mol·L-1 Na2CO3溶液加热到60℃,用pH传感器测定pH | 溶液的pH逐渐减小 | Kw改变与水解平衡移动共同作用的结果 |
A. A B. B C. C D. D
垃圾分类并回收利用,符合可持续发展的理念。废易拉罐对应的垃圾分类标志是( )
A.  B.
B. 
C.  D.
D. 
某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) 。a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为________________;名称是 。
②A在一定条件下能发生加聚反应,写出该反应的化学方程式 。
③A与足量的溴水反应生成B,B与NaOH的醇溶液共热可以得到D,B和D的相对分子质量满足M(D)+81=M(B)。则D分子中含有的官能团有 (填名称)。
(3)若核磁共振氢谱显示链烃A中有三个峰,且峰面积比为3:2:1。写出A所有可能的结构简
式 (包括顺反异构)。
冬日,雪花漫舞,给人带来美的享受,但降雪却会导致道路通行问题。现有一种高速公路
的绿色融雪剂-CMA(醋酸钙、醋酸镁固体的混合物),其生产常以白云石(主要成分
MgC03·CaC03,含Si02等杂质)和生物质废液——木醋液(主要成分乙酸,以及少量的![]() 甲醇、苯
甲醇、苯
酚、焦油等杂质)等为原料,流程如下:

(1![]() )步骤①发生的反应离子方程式为 。
)步骤①发生的反应离子方程式为 。
(2)滤渣1的主要成分与NaOH溶液反应的热化学方程式为
(己知l mol NaOH发生反应时放出热量为QkJ);步骤②所得滤液常呈褐色,分析可知其原因主要是
 木醋液中含有少量的有色的焦油以及____ 。
木醋液中含有少量的有色的焦油以及____ 。
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪
效果成正比)关系如右图所示,步骤④的目的除调节
n(Ca):n(Mg) 约为____ (选填:1:3; 1:2; 3:7; 2:3)
外,另一目的是 。
(4)步骤⑥包含的操作有____ 、过滤、洗涤及干燥。
(5)取akg含MgC03![]() ·CaC03质量分数为b%的白云石,经
·CaC03质量分数为b%的白云石,经
过上述流程制备CMA。已知MgC03'·CaC03的损失率为
c%,步骤④之后到产品CMA的损失率为d%,
则结合(3)可知所得产品质量约为_ kg(请用含相关字母的计算式表达,不必化简)。
下列说法正确的是
A.Fe3+的水溶液呈红褐色,Fe2+的水溶液呈浅绿色
B.Fe3+具有氧化性,Fe2+具有还原性
C.Fe3+的溶液中滴入含KSCN的溶液,立即出现红色沉淀
D.铁粉可以和水蒸气在高温下反应生成Fe2O3
下列除杂质的操作中不正确的是
A.Na2CO3固体中混有少量NaHCO3:加热固体至质量恒定
B.CO2中混有HCl:将其通入NaOH溶液
C.NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体
D.NaCl溶液中混有少量I2:加入适量CCl4,振荡,静置,分液
【实验一】实验室常用的几种气体发生装置如图①、②、③所示:

(1)实验室如果用②装置制取氨气,写出该反应的化学方程式 ,如果用浓氨水和氧化钙混合制取氨气可以用 (填编号)装置,检![]() 验氨气已收集满的方法是 。
验氨气已收集满的方法是 。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是
① 密度 ② 颜色 ③ 溶解性 ④ 热稳定性 ⑤ 与氧气反应
(3)若用①装置与④装置相连制取并收集X气体,则X可以是下列的 。(填序号)
① CO2 ② NO ③ Cl2 ④H2
【实验二】I.氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。一旦泄露需要及时处理,一般可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。已知:氰化钠化学式为NaCN,氰化钠![]() 是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(4) CN-中C元素显+2价,N元素显-3价,则非金属性N_______C(填“﹤”“﹥”或“=”),请设计实验证明:_____________________。
(5) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝![]() 的气体,该反应的离子方程式是____________________。
的气体,该反应的离子方程式是____________________。
II.硫代硫酸钠的工业制备的反应原理为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。某化学兴趣小组用上述原理实验室制备硫代硫酸钠【查阅资料】
i.Na2S2O3易溶于水,其稀溶液与BaCl2溶液混合物沉淀生成;
ii.Na2S2O3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
实验室通过如下图所示装置制备Na2S2O3。

(6)实验中要控制SO2生成速率,可采取的措施有___________(写出一条)。
(7)b装置的作用是______________。
(8)反应开始后c中先有淡黄色浑浊产生,后又变澄清,此浑浊物为__________(填
化学式)。
(9)实验结束后,在e处最好连接盛__________(填“NaOH溶液”、“水”、“CCl4”中一
种)的注射器,接下来的操作为__________,最后拆除装置。
(10)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
- 中国领导的多党合作与政治协商制度是我国一项基本政治制度。在这一制度下,中国与各民主党派的关系是 ①执政党与参政党的关系
- 已知奇函数f(x)的定义域为实数集,且f(x)在[0,+∞)上是增函数,当0≤θ≤时,是否存在这样的实数m,使f(cos
- 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将两个甲烷燃料电池串
- 重100N的物体在40N水平拉力作用,由静止开始沿水平面运动了5m,拉力做功 J,重力做功 J。
- “互联网已成为思想文化信息的集散地和社会舆论的放大器”。党和政府高度重视这一新兴媒体,因为它( ) ①是公民参与政治
- 右图是NaCl、MgSO4的溶解度曲线。请回答下列问题: (1) 加热t2℃的MgSO4饱和溶液,会看到的现象是
- 右图是某二倍体生物细胞分裂模式图。下列有关此图的说法正确的是 ()A.该生物的基因型一定是AaBB B.该体细胞中染色体
- 下列有关生物变异原理的叙述,正确的是 A. 姐妹染色单体的交叉互换属于基因重组 B. 对青霉菌进行X射线照射后,培育成高
- 教育部正式启动《国家中长期教育改革和发展规划纲要》公开征求意见后,各界人士通过多种渠道发表意见和建议,阐述自己的观点达几
- 如图所示,弹簧下端悬一滑轮,跨过滑轮的细线两端系有A、B两物体, mB=2kg,不计线、滑轮质量及摩擦,则A、B两重物在
- “煤”变“油”的这一技术目前世界上只有少数几个国家掌握。煤炭变成的汽油和柴油不含硫、氮等污染物,是高质量的洁净油品。据
- 改革开放以来,海外华人群体中新移民的数量迅速增长,“海归派”“海鸥族”等
- 独学而无友, (《礼记·杂记》)
- (本小题满分9分)已知A、B两地的路程为240千米,某经销商每天都要用汽车或火车将x吨保鲜品一次性由A地运往B地,受各种
- 人类常从矿石中获取金属材料. (1)铁是冶炼最多的金属.工业炼铁主要反应的化学方程式是3CO+Fe2O3 2Fe+3CO
- 在各种玩具马的马背上放上钱,寓意“马上有钱”,放上一只茄子,称为“马上有一切”……农历马年,众多版本的“马上体”走红网络
- 下列除去杂质的方法中正确的是( ) 选项 物质 杂质 除杂质的方法 A CaCl2溶液 稀盐酸 过量碳酸钙、过滤 B K
- 104.读“我国部分城市大气质量周报”(1998年6月),完成下列问题。城市 污染指数 首要污染物 实质级别 北京 92
- 山东武氏祠有一汉画像石刻,上面刻有“因宜教田,辟土种谷,以振万民”的文字,该石刻应该是对谁的赞扬 A.神农氏
- 为测定某品牌食用纯碱中碳酸钠的质量分数,小红称取了11 g样品(杂质仅有氯化钠)加入足量的氯化钙溶液,使其充分反应。反应



