高三化学试题
中国传统文化对人类文明贡献巨大。下列常见古诗文对应的化学知识正确的是
| 选项 | 古诗文 | 化学知识 |
| A | 《本草纲目拾遗》中对强水的记载:“性最烈,能蚀五金,其水甚强,惟玻璃可盛。” | 强水 |
| B | 《诗经·大雅·绵》:“堇茶如饴。”郑玄笺:“其所生菜,虽有性苦者,甘如饴也。” | 糖类均有甜昧 |
| C | 《梦溪笔谈》中对宝剑的记载:“古人以剂钢为刃, 柔铁为茎干,不尔则多断折。” | 铁合金的硬度比纯铁的大,熔点比纯铁的高 |
| D | 《本草经集注》中记载鉴别硝石(KNO3)和朴硝(Na2SO4)的方法:“以火烧之,紫青烟起,乃是真硝石也。 | 利用焰色反应 |
A. A B. B C. C D. D
研究发现,NOx和SO2是雾霾的主要成分。NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:N2(g)+O2(g) ![]() 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g) ![]() 2CO2(g) ΔH=-564 kJ·mol-1
2CO2(g) ΔH=-564 kJ·mol-1
 (1)2NO(g)+2CO(g)
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=_________,该反应在_______下能自发进行(填写:高温或低温或任意温度)
2CO2(g)+N2(g) ΔH=_________,该反应在_______下能自发进行(填写:高温或低温或任意温度)
(2)T℃时,将等物质的量的NO和CO充入容积为2 L的密闭容器中,保持温度和体积不变,反应过程(0~15 min)中NO的物质的量随时间变化如图所示。
①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为p=20MPa,则T℃时该反应的压力平衡常数Kp=_______;平衡后,若保持温度不变,再向容器中充入NO和CO2各0.3mol,平衡将_____(填“向左”、“向右”或“不”)移动。
②15 min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是________(填序号) A.增大CO浓度 B.升温 C.减小容器体积 D.加入催化剂
[化学——选修3:物质结构与性质](每空1分,共10分)
铜及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是________(填字母)。
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)基态Cu原子中,核外电子占据的最高能层符号是________,其核外电子排布式中未成对电子数为________个,Cu与Ag均属于IB族,熔点:Cu________Ag(填“>”或“<”)。
(3)[Cu(NH3)4]SO4 中阴离子的立体构型是_______;中心原子的轨道杂化类型为______________,[Cu(NH3)4]SO4 中Cu2+与NH3之间形成的化学键称为___________________。
(4)用Cu作催化剂可以氧化乙醇生成乙醛,乙醛中σ键和π键的比值为________。
(5)碘、铜两种元素的电负性如表:
| 元素 | I | Cu | ||
| 电负性 | 2.5 | 高三年级12月份月考·化学试题 第8页 共8页 |
CuI属于________(填“共价”或“离子”)化合物。
 (6)Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρ g·cm-3,晶胞边长为a cm,则阿伏加德罗常数为________(用含ρ、a的代数式表示)。
(6)Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρ g·cm-3,晶胞边长为a cm,则阿伏加德罗常数为________(用含ρ、a的代数式表示)。
下列说法中正确的是
A.氯化钾溶液在电流作用下电离成K+和Cl-
B.氧化还原反应的本质是有化合价的升降
C.依据丁达尔效应可将分散系分为溶液、胶体与浊液
D.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第二位
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作及实验现象 | 结论 |
| A | 室温下,用pH 试纸分别测定浓度为0.lmol/L NaCIO 溶液和0.1mol/L CH3COONa 溶液的pH | 比较HCIO和CH3COOH 的酸性强弱 |
| B | 向某溶液中滴加KSCN 溶液,无明显现象,再滴加少量酸性高锰酸钾溶液,紫色褪去 | 溶液中含有Fe2+,不含Fe3+ |
| C | 取久置的Na2O2 粉末,向其中滴加过量的盐酸,产生无色气体,此气体能使澄清石灰水变浑浊 | Na2O2 已经变质 |
| D | 向浓度均为0.1mol/LNaCl 和Na2CrO4混合溶液中滴加0.1mol/LAgNO3溶液,先生成白色的AgCl沉淀 | Ksp( AgCl) <Ksp(Ag2CrO4) |
以固体氧化物为电解质(能传导O2-)的新型联氨(N2H4) 燃料电池,属于环境友好电池,其结构如图所示。下列说法中正确的是

A.电极甲上发生的电极反应为:N2H4+4O2--8e-=2NO+2H2O
B.该电池放电过程O2-由电极乙向电极甲移动
C.该电池要经常更换固体氧化物电解质
D.每有1mol联氨参与反应,固体氧化物电解质中有4mol电子通过
下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①过量Na2O2投入到FeCl2溶液中 ②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2SiO3溶液中通入过量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2.
|
| A. | 全部 | B. | ①⑤ | C. | ②③④ | D. | ②③④⑤ |
利用I2O5可消除CO污染,反应为5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是

A.T1<T2,ΔH>0
B.T1温度下,该反应的平衡常数为1 024
C.T2温度下,0~0.5 min内,CO的平均反应速率为0.3 mol·L-1·min-1
D.T1温度下,若向装有足量I2固体的2 L恒容密闭容器中通入10 mol CO2,达到平衡时,φ(CO2)=0.8
.在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1
mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积
之间关系的是

空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.图为RFC工作原理示意图,有关说法正确的是( )

A.当有0.1mol电子转移时,a极产生标准状况下1.12L H2
B.左端装置中化学能转化为电能,右端装置中电能转化为化学能
C.c极上发生的电极反应是:O2+2H2O+4e﹣═4OH﹣
D.d极上进行还原反应,右端装置B中的H+可以通过隔膜进入A
25℃时若体积为 Va、pH=a的某一元强酸与体积为Vb、pH=b的某一元强碱混合,恰好中和,且已知 Va<Vb和 a=0.5b,则下列符合 a值的是 ( )
A. 3 B. 4 C. 5 D. 6
生活中下列物质起还原作用的是( )
A.明矾作净水剂 B.硅胶作干燥剂
C.铁粉作脱氧剂 D.活性炭作吸附剂
某溶液可能含有Na+、Fe2+、Br-、CO32-、I-、SO32-六种离子中的几种①在该溶液中加入足量氯水后,有气泡产生,溶液呈橙黄色;②向橙黄色的溶液中加入BaC12溶液时无沉淀生成;③向淀粉溶液中滴加该橙黄色溶液未变蓝色,则在该溶液中肯定存在的离子组是
A.Na+、SO32-、I- B.Na+、Br-、CO32-
C.Fe2+、I-、SO32- D.Fe2+、CO32-、Br-
下列表示对应化学反应的离子方程式正确的是( )。
A.向AlCl3溶液中加入过量浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
B.将含有0.1 mol Ba(OH)2的溶液与含有0.2 mol NaHSO4的溶液混合:H++SO42-+OH-+Ba2+=BaSO4↓+H2O
C.向澄清石灰水中通入过量CO2:OH-+CO2=HCO3-
D.Na2O2溶于水:2O22-+2H2O=4OH-+O2↑
乙烯是一种重要的基本化工原料,实验小组同学欲制备乙烯并验证其与溴单质的反应类型为加成反应。
I.乙烯的制备
欲利用下图所给装置制备乙烯。反应原理为:CH3CH2OH ![]() CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。

(1)欲收集一瓶乙烯,选择上图中的装置,其连接顺序为_____(按气流方向,用小写字母表示)。
(2)C中盛放的试剂为______,其作用为_____。
(3)在烧杯中混合浓硫酸和乙醇时,应先添加___;实验开始一段时间后发现忘记加碎瓷片,此时应该进行的操作为____。
(4)尾气吸收可采用________(填选项字母)。
A.KMnO4酸性溶液 B.浓硫酸 C.饱和Na2CO3溶液 D.NaOH溶液
II.验证乙烯与溴单质的反应类型为加成反应。
实验小组同学将I中制得的乙烯干燥后,按下列两种方案进行实验。
| 方案 | 操作 | 现象 |
| 一 | 将纯净的乙烯通入溴水中 | 溴水褪色 |
| 二 | 向充满纯净乙烯的塑料瓶中注入适量溴的CC14溶液,振荡 | ①溴的CCl4溶液褪色 ② |
(5)乙烯与溴单质发生加成反应的化学方程式为_________。
(6)方案一不能证明乙烯与溴单质发生了加成反应,原因为_________。
(7)方案二中现象②应为______,要想用此方案证明乙烯与溴单质发生的反应是加成反应,还需补充的实验为:继续向方案二塑料瓶中加入少量______,振荡后,若_____,证明发生了加成反应。
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程图如下:(已知:Cl2+2I-==2Cl-+I2)


(1)指出提碘的过程中有关的实验操作名称:① ,③ ,④ 。
(2)操作③、④可以分解为如下几步:
A、旋开活塞,用烧杯盛接溶液
B、从分液漏斗上口倒出上层溶液
C、打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔
D、静置,分层
E、把盛有溶液的分液漏斗放在铁架台的铁圈上
F、把50mL碘水和15mL苯加入分液漏斗中,盖好玻璃塞
G、检查分液漏斗是否漏液
H、倒转分液漏斗,振荡
(i)正确的操作顺序是:G→ → E → D → → →B。
(ii)能选用苯做萃取剂的原因是: 。
(iii)上述(C)这样操作的目的是: 。
(3)从流程图中,将操作④后的 层液体(填 “上”或“下”)用右图仪器进行操作⑤,写出仪器的名称:X Y 。请指出右图装置中存在的一处错误: 。
(1)某芳族化物A由碳、氢、氧三种元素组成,其蒸气密度是相同条件下H2密度的69倍。已知0.1 molA在氧气中完全燃烧得30.8gCO2和0.3mol H2O, 则A的分子式是____________。
A可以与NaHCO3溶液反应、其苯环上有两个邻位的取代基,则A中含氧官能团的名称是
已知:![]()
(2)A可以与![]() 反应制得有机物B(分子式为C9H9O4,遇FeCl3溶液不能显色),该反应的化学方程式是____________________________________
反应制得有机物B(分子式为C9H9O4,遇FeCl3溶液不能显色),该反应的化学方程式是____________________________________
(3)已知下列下列信息。分子式为C3H4的烃可以发生下图转化:
![]()
![]()
其中E、F均呈酸性。F可以与有机物B和乙二醇共同发生反应得到有机物G,由G通过加聚反应可以进一步合成分子式为(C15H15O6)2的药物H。
①写出F的同分异构体结构简式,且满足a)属于链状酯类、b)分子中每个碳原子上都连有氢原子___________________________________________
②C→D的化学方程式是_________________________________
③H的结构简式是_______________________________
如果要除去粗盐中含有的可溶性杂质氯化钙、氯化镁和一些硫酸盐,按下表所示顺序,应加入什么试剂?完成下列表格:
| 杂质 | 加入试剂 | 化学方程式 |
| 硫酸盐 | ||
| MgCl2 | ||
| CaCl2 |
反应![]()
![]()
![]()
![]() 。温度为
。温度为![]() 时,平衡常数
时,平衡常数![]() 温度调至
温度调至![]() 时,
时,![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 该反应为放热反应 B. 由![]() 到
到![]() 是降温过程
是降温过程
C. ![]() 时,增大
时,增大![]() 不变 D.
不变 D. ![]() 时,
时,![]() 的转化率比
的转化率比![]() 时小
时小
葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6![]() 2CH3CH2OH+2CO2↑)
2CH3CH2OH+2CO2↑)
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH![]() CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
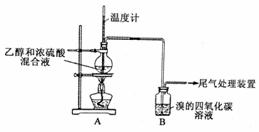
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| …… | |
| 实验完毕,清洗烧瓶 | III:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1![]() )溶液“渐渐变黑”,说明浓硫酸具有 性。
)溶液“渐渐变黑”,说明浓硫酸具有 性。
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是 ;
②乙根据现象认为实验中产生的SO2和 ,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题
A.甲设计实验中A、B间洗气瓶中盛放的试剂是 ;乙设计的实验D中盛放的试剂是 ,装置连接顺序为 。
B.能说明确实是SO2使E中溶液褪色的实验是 。
C.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是 。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色。
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如右图所示。写出Na2S2O5溶于水时发生的化学方程式 。
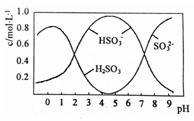
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤ 1×10-5mol·L-1],此时溶液中c(SO32-)≤ mol·L-1。
- His suggestion ____ to see the art exhibition interested eve
- 用起重机将质量为m的物体匀速地吊起一段距离,那么作用在物体上各力的做功情况应该是下面的哪种说法 A.重力做正功,拉力做负
- 实践的观点是辩证唯物主义认识论的首要的基本观点,实践是( ) A.人的精神活动 B.人的理性行为
- 已知tan=,tan=,则tan(α+β)=________.
- 1933年,美国成立农业调查署,购买并大量屠宰了大量牲畜。这一措施的主要目的是 A.增加肉类储备应急救济
- 如图所示,甲、乙两同学从河中O点出发,分别沿直线游到A点和B点后,立即沿原路线返回到O点,OA、OB分别与水流方向平行和
- 升高温度时,化学反应速率加快,主要原因是( )A.分子运动速率加快,使反应物分子间碰撞机会增多B.反应物分子的能量
- 古诗文默写。 (1)雕栏玉砌应犹在, 。问君能有几多愁?
- ①那水呢,____________不结冰,____________在绿萍上冒着点热气,水藻真绿,把终年贮蓄的绿色全拿出来
- 下图中MN、AB分别为北半球某纬线和晨昏线的一段,AB与MN交于O点。A点与M点地方时相同且该日A点正午太阳高度为0°,
- 有一批上万吨的化工原料要从北京通过海运运往南方的某一沿海城市,那么选择装货地点的港口位于的城市和濒临的海洋分别是(
- 物质的宏观性质与微观组成(或结构)相互联系是化学特有的思维方式,下列对物质性质的解释不正确的是() A.稀有气体可以用作
- 已知a,b,则的
- 在群落演替中,下列情况哪一种情况是不可能发生的?A.在群落演替过程中群落的物种组成不断发生变化 B.生态系统的恢复力稳定
- Hearing that most of the members voted against her, she ____
- Linda ________ her homework but________ on weekends. A.does
- 细胞中为生命活动提供能量的细胞器产( ) 。A. 核糖体 B. 中心体 C
- 如图,水平放置的三棱柱的底面是边长为2的正三角形,且侧棱AA1垂直底面,正视图是边长为2的正方形,该三棱柱的左视图面积为
- 形成欧洲西部气候东西部差异的最主要原因是( ) A.东西部所处气压带和风带不同 B.纬度不同
- 下列分子式一定只表示一种物质的是 ( ) A.CH2O B.CH4O C.C7H8



