高三化学试题
下列各项中,左、右两边说明的逻辑关系正确的是( )
| A | 乙烯使溴水褪色 苯使溴水褪色 | 均发生了加成反应 |
| B | 用pH试纸测定某盐酸的pH 用红色石蕊试纸检验某气体为氨气 | 试纸均需要蒸馏水湿润 |
| C | MnO2与浓盐酸反应制备Cl2 CaCO3与稀盐酸反应制备CO2 | 均发生氧化还原反应 |
| D | 淀粉在酶的作用下生成葡萄糖 蛋白质在酶的作用下生成氨基酸 | 均发生了水解反应 |
A.A B.B C.C D.D
下列说法中不正确的是( )
A.乙烷、乙醇和乙酸都能发生取代反应
B.苯分子中没有乙烯分子中的双键结构,因此苯不能发生加成反应
C.可用新制的Cu(OH)2悬浊液检验患者的尿液中是否含糖
D.蛋白质溶液中加入饱和(NH4)2SO4溶液后蛋白质会析出,再加水可溶解
一定温度下在容积恒定的密闭容器中,进行可逆反应: A(s)+2B(g)![]() C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是
①容器内气体的压强 ②混合气体的密度
③混合气体的平均相对分子质量 ④B的物质的量
A.只有④ B.②③
C.②③④ D.①④
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. lmol FeI2与足量氯气反应时转移的电子数为2NA
B. 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
C. 18gD2O和18gH2O中含有的质子数均为10NA
D. 1 mol Na2O2固体中含离子总数为4NA
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S![]() 6Ag+Al2S3
6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
电渗析法是指在外加电场作用下,利用阴离子交换膜和阳离子交换膜的选择透过性,使部分离子透过离子交换膜而迁移到另一部分水中,从而使一部分水淡化而另一部分水浓缩的过程。下图是利用电渗析法从海水中获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO![]() 等离子,电极为石墨电极。
等离子,电极为石墨电极。
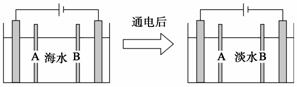
下列有关描述错误的是
A.阳离子交换膜是A,不是B
B.通电后阳极区的电极反应式:2Cl--2e-=Cl2↑
C.工业上阴极使用铁丝网代替石墨碳棒,增大反应接触面
D.阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀
在N2+3H2 ![]() 2NH3 △H<0的平衡体系中,当分离出NH3时,下列说法正确的是( )
2NH3 △H<0的平衡体系中,当分离出NH3时,下列说法正确的是( )
A.反应速率增大 B.平衡向逆反应方向移动
C.平衡体系中NH3的含量增大 D.N2的转化率增大
某混合气体的可能有CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,将该混合气体依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)![]() 和无水硫酸铜(变蓝)时,则可断定该混合气体中一定有( )
和无水硫酸铜(变蓝)时,则可断定该混合气体中一定有( )
A.HCl、CO2、H2 B.CO2、H2、H2O
C.CO、H2、NH3 D.HCl、CO、H2O
( ) ( )

25℃时,向浓度均为0.1 mol/L、体积均为100 mL的两种一元酸HX、HY溶液中分别加入NaOH 固体,溶液中lg![]() 随n(NaOH)的变化如图所示。下列说法不正确的是( )
随n(NaOH)的变化如图所示。下列说法不正确的是( )
A.HX为强酸,HY为弱酸
B.b点时溶液呈中性
C.水的电离程度:d>c
D.c点时溶液的pH=4
已知:苯环上连有的基团不同时,新的基团可能进入间位,也可能进入邻、对位。
煤是非再生能源,我国煤炭储量占能源总储量约94%。下图是煤干馏得到的主要产物,以及产物之一甲苯的有关反应。回答下列问题:

(1) 煤的干馏是指 。固态物质A是
(写名称),它是冶金工业的重要原料,还用于 (再写一种用途)。
(2)由甲苯制备物质C时,若反应①和②的顺序交换,得到的物质不是C,而可能是 (写结构简式,一种即可)。
(3)反应③的反应条件是 ;反应④是 反应(填反应类型)。
(4)与E含相同基团(苯基和—C≡C—)的E的同分异构体(包括E)共 种。
A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含有一种官能团,且每个碳原子上最多只连一个官能团:A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:
(1)A的分子式是 ,其结构简式是 。
(2)写出A与乙酸反应的化学方程式: 。
(3)写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是 。
某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成硫单质2.4g,FeCl2 0.425mol和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是( )
A.该磁黄铁矿中FexS的x=0.85
B.生成的H2S气体在标准状况下的体积为2.24L
C.100mL的盐酸中HCl物质的量浓度为7.5mol/L
D.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1
正确表示下列反应离子方程式是( )
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
B.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
某溶液中含有HCO![]() 、SO
、SO![]() 、CO
、CO![]() 、CH3COO- 4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是( )
、CH3COO- 4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是( )
A.CO![]() B.SO
B.SO![]() C.CH3COO- D.HCO
C.CH3COO- D.HCO![]()
下列叙述中正确的是
A.甲苯分子中共平面的原子最多是12个
B.对二甲苯分子中有四个碳原子在一条直线上
C.1一丁烯分子中的4个碳原子一定在同一平面内
D.2一丁烯分子中的4个碳原子一定在同一平面内
室温下,甲、乙两烧杯均分别盛有5 mL pH=3的盐酸和醋酸溶液,向乙烧杯中加水稀释至pH=4。
关于甲和稀释后乙烧杯中的溶液,描述正确的是
A.溶液的体积10V 甲>V乙
B.水电离出的OH-浓度:10c(OH-)甲=c(OH-)乙
C.若分别用等浓度的NaOH 溶液完全中和,所得溶液的pH:甲>乙
D.若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲<乙
化学在生活中有着广泛的应用,下列对应关系不正确的是
①Al2(SO4)3和小苏打反应,应用于泡沫灭火器灭火
②铁比铜金属性强,用FeCl3腐蚀Cu刻制印刷电路板
③HF与SiO2反应,利用氢氟酸在玻璃器皿上刻蚀标记
④SO2具有氧化性,可用于漂白纸浆
⑤NH4HCO3受热易分解,可用作氮肥
⑥Fe2(SO4)3易溶于水,可用作净水剂
⑦Al2O3熔点高,可用作耐高温耐火材料
⑧CO具有可燃性,用于冶炼金属
A.②④⑤⑥⑧ B.①③⑦ C.②⑤⑥⑧ D.②⑤⑧
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子。
 如下图分子,因其形状像东方塔式庙宇(pagoda—style temple),所以
如下图分子,因其形状像东方塔式庙宇(pagoda—style temple),所以
该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是
A、分子式为C20H20
B、一氯代物的同分异构体只有两种
C、分子中含有二个亚甲基(—CH2—)
D、分子中含有4个五元碳环
分离苯和溴苯的混合物,宜采用的方法是
A.分液 B.升华 C.蒸馏 D.过滤
若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,肯定不能共存的是
A. Fe3+、NO3-、Cl-、Na+ B.Ba2+、Mg2+、HCO3-、AlO2-
C.NO3-、Na+、K+、CO32- D.NO3-、K+、SO42-、Cl-
- 读几个地区农业基本情况比较表,回答44~46题 地区 种植业比重 畜牧业比重 商品率 投入劳动力数量 ① 86% 14%
- 下列化学反应与实验现象相符合的是 ( )
- 如图所示,螺旋测微器读数是___________mm.
- 请根据下表中的提示,以 “Kitchen—the Most Important Room in the House”为题
- 阅读下面一首宋词,完成1~2题。 水调歌头 黄庭坚 瑶草一何碧,春入武陵溪。溪上桃花无数,枝上有黄鹂。我欲穿花寻路,直入
- 目前,凡·高几乎是“荷兰”的代名词。他是荷兰历史上公认的最杰出的人物,以他命名的艺术馆成为荷兰最吸引参观者的地方之一。但
- 2008年5月1日 政府信息公开条例开始实施,第一时间将重大突发事件向社会公开,已经成为各地工作的新亮点。政府信息公开透
- 下列关于衰老细胞特征的描述,不正确的是( ) A. 细胞膜通透性改变,使物质运输功能降低,且细胞核的体积减小 B.
- 当x=2014时,分式的值为.
- 公元前5世纪后半期,伯利克里当政期间,达到全盛的城邦是( ) A.雅典 B.斯巴达C.奥林匹亚 D.罗马
- (二)阅读《幼时记趣》选段,然后答题(10分)于土墙凹凸处,花台小草丛杂处,常蹲其身,使与台齐,定目细视。以丛草为林,以
- 下列不属于生态系统的信息传递在农业生产中的应用的是 A.利用人工合成的化学信息素吸引昆虫前来,提高传粉率和结实率 B.草
- 当吸气时
- 下列关于真核细胞的结构与主要成分,对应有误的是 A.细胞膜:脂质、蛋白质、糖类 B.染色体:核糖核酸、蛋白
- 古诗文名句默写。1.子曰:“ ,思而不学则殆。”(论语《为政》)2.报君黄金台上意,
- 下图为水循环示意图,读图回答下列问题。(1)人类可以通过影响水循环中的 环节,缓解水资源时空
- 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定
- 2010年7月31日,《海南省实施<中华人民共和国国家通用语言文字法>办法》正式发布。该“办法”规定,电台、
- 下图Ⅰ的曲线表示某动物细胞有丝分裂过程中染色体的着丝点与中心粒之间的平均距离,则图Ⅱ中能正确表示此细胞分裂过程中着丝点分
- 下列哪些生态系统有“绿色水库”之称( ) A.海洋生态系统 B.农田生态系统 C.森林生态系统



