高三化学试题
关于苯的叙述中错误的是
A.苯在催化剂作用下能与液溴发生取代反应
B.在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色
C.在苯中加入溴水,振荡并静置后下层液体为橙黄色
D.在一定条件下,苯能与氯气发生加成反应
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程.

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则说明装置气密性良好.装置D的作用是 .装置E中为 溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 .
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 (填字母代号).
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验开始后,为使SO2缓慢进入烧瓶C,可采取的操作是 .
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 .
(6)反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器有 .(填字母代号)
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(7)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.请设计简单实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论 .
下列物质的水溶液因水解而显酸性的是
A.KNO3B.Fe2(SO4)3C.Na2CO3D.H2SO4
据报道,北京奥运会“祥云”火炬燃料为丙烷,悉尼奥运会火炬燃料为丁烷和丙烷混合气体。
(1)常温、同压下,等体积的丙烷和丁烷完全燃烧恢复到原状态,生成二氧化碳的体积比为 。
(2)已知丁烷的燃烧热(生成液态水)为2880kJ/mol,1mol丙烷和丁烷(物质的量之比1:1)的混合气完全燃烧放出的热量为2550kJ。写出丙烷燃烧的热化学方程式
(3)标准状况下,1.0mol丙烷和丁烷的混合气和足量氧气混合完全燃烧后,恢复至原状态,混合气体的体积减小了70.0L,混合气体中丙烷和丁烷的体积比为 。
(4)标准状况下,aL的某丙烷和丁烷的混合气体,在bL足量氧气中完全燃烧后,恢复到原状态体积为VL,所得气体体积V为(用a和b表示) 。
三氧化二镍(Ni2O3)是一种重要的化学材料。工业上利用含镍废料(镍、铁、 钙、镁合盒为主)制取草酸镍(NiC2O4).再高温煅烧草酸镍制取三氧化二镍。(已知草酸的钙、镁、镍盐均难溶干水。)工艺流程如图所示:

请回答下列问题:
(1)操作I为____。加入H2O2发生的主要反应的离子方程式为 ;加入碳酸钠溶液调节pH至4.0一5.0,其目的为 。
(2)若加入NH4F时滤液中c(Mg2+)=0.02 mol/L,设溶液体积不变,使滤液中Ca2+恰好沉淀完全,即溶液中c(Ca2+ )=1×10-5mol/L,判断此时是否有MgF2沉淀生成并加以解释: 。(已知CaF2、MgF2的Ksp分别为2.5×10-12、7.4×10-11)
(3)草酸镍高温煅烧,可制得Ni2O3,同时获得混合气体,该混合气体的主要成分为____。
 (4)工业上还可用电解法制取N12O3,用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后用惰性电极电解。电解过程中产生的Cl2在弱碱性条件下生成ClO -,再把二价镍氧化为三价镍。ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为____。以Al和Ni2O3为电极,NaOH溶液为电解质溶液组成一种新型电池,放电时,Ni2O3转化为Ni(OH)2,该电池反应的化学方程式是____。
(4)工业上还可用电解法制取N12O3,用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后用惰性电极电解。电解过程中产生的Cl2在弱碱性条件下生成ClO -,再把二价镍氧化为三价镍。ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为____。以Al和Ni2O3为电极,NaOH溶液为电解质溶液组成一种新型电池,放电时,Ni2O3转化为Ni(OH)2,该电池反应的化学方程式是____。
(5) Ni2O3还可用于制备合成氨的催化剂ConNi(1-n)Fe2O4。
在其他条件相同时合成氨的相对初始速率随催化剂中n
值变化的曲线如图,由图可知Co2+、Ni2+两种离子中催化效
果更好的是____。
如图是某种有机物分子的球棍模型。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子。对该有机物的叙述不正确的是

A.该有机物可能的分子式为C2HCl3 B.该有机物的分子中一定有C=C键
C.该有机物分子中的所有原子在同一平面上 D.该有机物可以由乙烯和氯化氢加成反应得到
高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,工业上用难溶于水的碳酸
锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体的过程为:

已知:I.SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
II.有关氢氧化物开始沉淀和完全沉淀的pH表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
(1)操作①加快反应速率的措施有 (写一种)。
碳酸锶与盐酸反应的离子方程式
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为 。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为 __。
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是 (填化学式)。
(5)步骤④的操作是
(6)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
粗盐提纯中除含有钙离子、镁离子、硫酸根离子等可溶性杂质,还含有泥沙等不溶性杂质。我们食用的精盐是用粗盐提纯而得到的。通过教材中“粗盐提纯”及你做过的该实验回答下列问题:
(1)如何运用最简单的方法检验溶液中有无SO42ˉ离子?________________。
如果有,应该如何除去SO42ˉ离子?_____________________。
(2)在粗盐经过溶解,过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止,请问这步操作的目的是_______________________。
(3)实验室将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:____________________________;
过滤时:____________________________;
蒸发时:____________________________。
下列各组物质中,分子数相同的是( )
A.2 L SO2和2 L CO2 B.9 g水和标准状况下11.2 L CO2
C.标准状况下1 mol氧气和22.4 L水 D.0.1 mol氢气和2.24 L氯化氢气体
某温度时,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+ ),所需S2-最低浓度的对数值lgc(S2-)与lg(M2+)的关系如图所示。下列说法正确的是
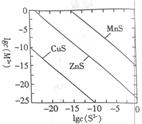
A.三种离子对应的硫化物中Ksp(CuS)最小,约为1×10-20
B.可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2
C.向MnS的悬浊液中加入少量水,沉淀溶解平衡向溶解的方向移动,c(S2-)增大
D.向浓度均为1×10-5 mol·L-1的Cu2+、Zn2+、Mn2+混合溶液中逐滴加入l×l0-4 mol·L-1的Na2S溶液,Zn2+最先沉淀
NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4L H2S和SO2的混合气体中含有的分子总数为NA
B. 1L1mol•L-1 FeCl3溶液完全水解产生的Fe(OH)3胶体粒子数为NA
C. 高温下,16.8gFe与足量的水蒸气完全反应失去的电子数为0.8NA
D. 28.6gNa2CO3•10H2O溶于水配成1L溶液,该溶液中阴离子数目为0.1NA
向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2,测得溶液中离子浓度的关系如图所示,下列说法正确的是
A.A、B、C三点对应溶液pH的大小顺序为:A<B<C
B.B点对应的溶液中存在:c(Ba2+)+c(Na+)+c(H+)=3c(![]() )+c(OH−)+c(Cl−)
)+c(OH−)+c(Cl−)
C.向C点溶液中通入CO2可使C点溶液向B点溶液转化
D.该溶液中存在:![]() <
<![]()
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A. 2.3 g钠由原子变成离子时,失去的电子数为 0.2NA
B.28 g氮气所含的原子数为NA
C.0.2NA个硫酸分子与19.6 g磷酸含有相同的氧原子数
D.NA个氧分子与NA个氢分子的质量比为8∶1
某实验小组通过下图所示实验探究Na2O2与水的反应:

下列说法不正确的是( )
A. ②中的大量气泡主要成分是氧气
B. ③中溶液变红,说明有碱性物质生成
C. ④中现象可能是由于溶液中含有强氧化性物质造成的
D. ⑤中MnO2的主要作用是降低了水中氧气的溶解度
下列选用的实验仪器或实验装置符合实验要求且安全的是( )。


A.实验室制备少量蒸馏水 B.实验室制备氨气


C.实验室制备NO2 D.实验室制备氢气
利用下图装置进行木炭粉和浓硫酸的反应及其产物的检验。
已知:紫红色的酸性高锰酸钾溶液能与二氧化硫发生氧化还原反应,向酸性高
(1)组装好上述装置后,首先要进行的操作是: 。
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式: 。
(3)用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入试剂的名称及其作用:A中加入的试剂和作用是 、 ;B中加入的试剂和作用是 、 。
(4)实验时,C中应观察到什么现象,才可以说明生成了二氧化碳: 。
常温下,pH=l 的某溶液 A 中除H+外,还含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、 Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol·L-1。现取该溶液进行有关实验,实验结果如下图所示,下列有关说法正确的是

A. 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B. 实物消耗Cu14.4g,则生成气体丁的体积为3.36L
C. 该溶液一定没有Fe3+,但是无法确定是否含有I-
D. 沉淀乙一定有BaCO3,可能有BaSO4
化学与生产,生活密切相关。下列说法正确的是
A.在燃放烟花爆竹时,硫燃烧生成SO3 B.六水氯化钙可用作食品干燥剂
C.太阳能电池板的材料是二氧化硅 D.乙烯可做水果的催熟剂
离子检验的常用方法有三种:
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法不合理的是( )
A.NH4+-气体法 B.I--沉淀法
C.Na+-显色法 D.CO32- -气体法和沉淀法
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化如图所示,下列说法正确的是

A.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓
B.原溶液中含有的阳离子必定有H+、NH4+、Al3+、Mg2+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.d点溶液中含有的溶质只有NaAlO2
- 质子、中子和氘核的质量分别为m1、m2和m3,一个质子和一个中子结合成氘核时,若放出的能量全部转变为一个光子的能量,已知
- 阅读下面的文字, 按要求作文。(10分) 当今中学里各种社团深受学生欢迎。新学年伊始,各种学生社团就纷纷开展“招新”活动
- 下列标点符号没有错误的一项是( ) A.人什么叫社会主义?什么叫马克思主义?我们过去对这个问题的认识不是完全清醒的。
- 下图为两分子系统的势能Ep与两分子间距离的关系曲线。说法正确的是( )A.当大于r1时,分子间的作用力表现为引力B.
- 下列有关表述正确的是 A.位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素
- 把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一
- 关于阻尼振动,以下说法中正确的是( )A.机械能不断减小 B.动能不
- 正四棱柱的一个侧面的面积为S,则它的对角面的面积为( )A.S B.2S
- 设NA为阿伏加德罗常数。下列叙述中正确的是A.标准状况下,22.4 L CO2和O2的混合气体中含有的氧原子数为2NAB
- 14.阅读下面这首诗,完成文后各题。 秋兴八首(其三) 杜甫 千家山郭静朝晖,日日江楼坐翠微。 信宿渔人还泛泛,清秋燕子
- 物体从离地高为h处下落,它在落地前的1s内下落35m,求下落时的高度和下落时间?
- (本小题满分15分)已知矩形纸片ABCD中,AB=6cm,AD=12cm,将矩形纸片的右下角折起,使得该角的顶点B落在矩
- 同学们以盖房子的方式总结出了如下物质间的关系。A、B、C均为纯净物, 且上、下相邻的物质问均可发生反应。回答下列问
- 阅读下面的文字,根据要求写一篇不少于800字的文章。 一天早晨,一位女士发现自己的邻居在下楼时把每家每户门口的垃圾袋都拿
- 下图是“白菜——甘蓝”杂种植株的培育过程。下列说法正确的是A.培育出的“白菜——甘蓝”植株不能结籽 B.愈伤组织的代谢类
- 放射性元素衰变时放出三种射线,按穿透能力由强到弱的排列顺序是A.a 射线,b 射线,g 射线 B.
- 若实数满足,则关于的方程有实数根的概率是_______________.
- 材料一:12月1日发展改革委发布:2008年我国粮食总产量预计将达到5250亿公斤、创历史最高记录,这将是我国近40年来
- 右表是某逻辑电路的真值表,该电路是



