高三化学试题
现有短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径如图所示,下列推断正确的是
A.Y、Z组成的化合物只含离子键
B.氢化物的沸点:R<X<Y
C.T的最高价氧化物的水化物酸性比R的强
D.Y和Z分别与T、X组成的二元化合物的水溶液一定呈中性
.混合动力汽车(HEV)中使用了镍氢电池,其工作原理如图所示:
 |
其中M为储氢合金,MH为吸附了氢原子的储氢合金,KOH溶液作电解液。关于镍氢电池,下列说法不正确的是
A.充电时,阴极附近pH降低
B.电动机工作时溶液中OH-向甲移动
 C.放电时正极反应式为: NiOOH+H2O+e-
C.放电时正极反应式为: NiOOH+H2O+e-![]() Ni(OH)2+OH-
Ni(OH)2+OH-
D.电极总反应式为:M+Ni(OH)2MH+NiOOH
向1mol炽热的Cu2S通入足量的水蒸气,充分反应后生成2mol H2,则Cu2S应转化为
A. CuO和SO2 B. Cu和S C. Cu和SO2 D. Cu2O和S
自热食品不用火电,将水倒在发热包上,发热包遇水自动升温,从而加热食物。发热包的主要成分是:生石灰、铁粉、铝粉、焦炭粉、活性炭、碳酸钠、焙烧硅藻土等,下列说法不正确的是
A.生石灰和水反应放出热量
B.铝粉和碱反应放出热量
C.氢氧化钙和碳酸钠反应使溶液碱性增强:Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
D.过程中有微小原电池形成,负极反应为:O2+2H2O+4e-===4OH-
用NaOH溶液清洗试管壁上的硫,发生反应S+NaOH—Na2SO3+Na2S+H2O(未配平)。下列说法不正确的是
A. 方程式中含钠元素的化合物均含离子键和共价键
B. 生成的Na2SO3 和Na2S的物质的量之比为1 : 2
C. 方程式中S和H2O的化学计量数相同
D. 清洗之后的废液呈碱性
A、B都是芳香族化合物,相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。1 molA与1mol某一元羧酸发生酯化反应生成B,B能在一定条件下发生银镜反应而A不能;A中氧元素的质量分数为31.6%,B的溶液有酸性,但不能和FeCl3溶液发生显色反应。请根据上述信息,完成下列填空:
⑴A的分子式是 ,你确定A分子中氧原子数目的理由是
⑵若1molA只能与1molNaOH发生反应,且A苯环上一取代产物只有两种,则A的结构简式为 。
⑶B的同分异构体甚多。其中不属于酚类且1mol能与3molNaOH反应的同分异构体的结构简式为 (任写一种)。
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H = + 74.9 kJ·mol-1,下列说法中正确的是
A.该反应中熵变、焓变皆大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
一种新型的合成氨的方法如图所示,下列说法正确的是

A.反应①属于“氮的固定”
B.反应②属于氧化还原反应
C.反应③可通过电解LiOH水溶液实现
D.上述三步循环的总结果为:N2+3H2=2NH3
KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。利用“KClO3氧化法”制备KIO3包括以下两个反应:①11KClO3+6I2+3H2O == 6KH(IO3)2+3Cl2↑+5KCl ②KH(IO3)2+KOH == 2KIO3+H2O
下列说法正确的是( )
A.化合物KH(IO3)2中含有共价键、离子键和氢键等化学键
B.反应①中每转移4mol电子生成2.24LCl2
C.向淀粉溶液中加入少量碘盐,溶液不会变蓝
D.可用焰色反应实验证明碘盐中含有钾元素
下列应用特征现象推断不正确的是( )
A.遇FeCl3溶液显紫色或加入溴水产生白色沉淀,表示物质中可能含有酚羟基。
B.加入新制Cu(OH)2悬浊液并加热,有红色沉淀生成,或加入银氨溶液并水浴加热有银镜出现,说明该物质中含有—CHO
C.加入金属钠,有H2产生,表示物质可能有—OH或—COOH
D.加入NaHCO3溶液有气体放出或能使紫色石蕊试液变红,表示物质中含有—COOH
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL B.45mL
C.30mL D.无法计算
下列物质与常用危险化学品的类别不对应的是
A.H2SO4、NaOH——腐蚀品 B.CH4、C2H4——易燃液体
C.CaC2、Na——遇湿易燃物品 D.KMnO4、K2Cr2O7——氧化剂
已知化合物A(C4Si4H8)与立方烷(C8H8)的分子结构相似,如下图,则C4Si4H8的二氯代物的同分异构体数目为
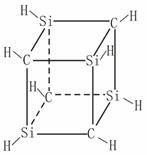
A.3 B.4 C.5 D.6
下列说法正确的是( )
A.将AgCl放入水中不能导电,故AgCl不是电解质
B.CO2溶于水得到的溶液能导电,所以CO2是电解质
C.金属能导电,所以金属是电解质
D.固态的NaCl不导电,熔融态的NaCl能导电,NaCl是电解质
二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)在处理废水时,ClO2可将废水中的CN-氧化成CO2和N2,写出该反应的离子方程式:_______________________________________。
 (2)某小组设计了如下图所示的实验装置用于制备ClO2。
(2)某小组设计了如下图所示的实验装置用于制备ClO2。
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是____________________。
②装置B的作用是__________________。
③装置A用于生成ClO2气体,该反应的离子方程式为_____________________。
④当看到装置C中导管液面上升时应进行的操作是______________________。
(3)测定装置C中ClO2溶液的浓度:取10mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入_______________________作指示剂,用0.1000mol·L-1的Na2S2O3标准液滴定锥形瓶中的溶液(2ClO2+10I-+8H+==5I2+2Cl-+4H2O,I2+2S2O32- = 2I- +S4O62-),测得标准液消耗的体积为20.00mL,通过计算可知C中ClO2溶液的浓度为________mol·L-1。
一杯澄清透明的溶液中,已知各离子的浓度均为0.1 mol/L,体积为1 L。可能含有的离子: K+、Fe2+、Ba2+、NH4+ 、Cl-、NO3-、CO32-、SO42-。向该混合液中加足量稀盐酸,有无色气体生成,且阴离子的种类不变。对该溶液的下列叙述错误的是( )
A.该溶液一定含有Fe2+、NO3-、Cl- B.该溶液一定不含K+、NH4+
C.该溶液一定不含CO32-、Ba2+ D.该溶液可能含有SO42—
下列离子方程式正确的是( )
A.过氧化钠与水反应:2O22﹣+2H2O═O2↑+4OH﹣
B.次氯酸钠与Fe(OH)3在碱性溶液中反应生成Na2FeO4:3ClO﹣+2Fe(OH)3═2FeO42﹣+3Cl﹣+H2O+4H+
C.向明矾[KAl(SO4)2•12H2O]溶液中逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀:2Al3++3SO42﹣+3Ba2++6OH﹣═2Al(OH)3↓+3BaSO4↓
D.向碳酸氢镁溶液中加入过量的澄清石灰水:Mg2++2HCO3﹣+2Ca2++4OH﹣═Mg(OH)2↓+2CaCO3↓+2H2O
某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:

请回答下列问题:
(1)步骤①的作用是清洗废铁屑表面的油污,其中加热的目的是 。
(2)写出步骤②中生成Fe2+的离子方程式 。(写一个即可)
(3)步骤③中“氯气”不引入杂质但有毒,可以用 代替(填化学式)。
(4)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验操作是 。
(5)步骤⑤产生金属铜的化学方程式为 。
 |
海水是重要的资源,可以制备一系列物质。下列说法正确的是
A.步骤②中,应先通CO2,再通NH3
B.除去粗盐中SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
C.步骤③中可将MgCl2·6H2O晶体直接进行灼烧制得无水MgCl2
D.步骤④、⑤、⑥反应中,溴元素均被氧化
下列选项所示的物质间转化均能实现的是
A.![]()
B.![]()
C.![]()
D.![]()
- 如图的几何体是由一个圆柱体和一个长方形组成的,则这个几何体的俯视图是() A.B.C.D.
- 有一种酸式盐AHB,它的水溶液呈弱碱性。则以下说法:①相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的
- 强学会成立后不久,两江总督张之洞等人相继加入,这说明 A.强学会为研究儒学的团体 B.张之洞等人与顽固派决裂 C.各省督
- 为使“神州七号宇宙飞船”安全着落,就必须选择地形开阔平坦、云量少、晴天多, 人口稀少的地点,你认为下列地点较为合适的是;
- 如下图是发酵工程的流程图,据图回答:( 1 )在配制培养基时,要注意各种营养的比例。假如利用谷氨酸棒状杆菌来生产谷氨酸。
- (09南昌市调研)一个九肽中最少含有的氨基个数是A.0 B.1
- 标准状况下一个空瓶的质量是20g,装满O2,称量其质量为21g,若装满A气体,称量其质量为22g,则A的相对分子质量是
- ......
- Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是 A、Na2CO3是碱 B.Na2
- 已知烯烃X和炔烃Y常温下为气体,烯烃X和足量的O2的混合气体充分燃烧前后体积不变(100 ℃以上,同温同压下)。现取烯烃
- 参考下图;你认为在中古的西欧,一个男人的梦想和最高荣耀是( )A.成为武士 B.成为绅士
- 设Z=(2+i)(1-i)2,则复数Z所对应的点在 ( )A.第一象限 B.第二象限
- 中国局部地图,完成: (1)属于季风区和非季风区分界线的山脉是 、 (字母);属于地势中第一、 二级
- Many accidents____ by careless drivers lastyear. A. are caus
- 下列葫芦藓植物的结构中,有助于孢子散发的为:A .蒴齿 B .弹丝 C .蒴帽 D .环带
- 下列各句中,有语病的一句是 A.汉语的魅力随着中国国力的日益强盛,开放度的日渐扩大而广为辐射,汉语热正遍及全球。
- 下图表示生物新物种形成的基本环节,对图示分析正确的是 A. 图中A表示基因突变和基因重组,为进化提供原材料
- 向如图所示试管的水中加入某种物质后,U形管左端的红墨水液面降低,则加入的物质是()。A.氢氧化钠
- 如图,点M是△ABC内﹣点,过点M分别作直线平行于△ABC的各边,所形成的三个小三角形△1、△2、△3(图中阴影部分)
- 右图是“我国某天气系统在某地过境时的气压与风速随时间变化规律图”,1.该天气现象是 A.大风寒潮天气 B.东南沿海台



