高三化学试题
下列有关化学用语表示不正确的是( )
 A .Al3+的结构示意图:
A .Al3+的结构示意图:![]() B.K2O的电子式:
B.K2O的电子式:![]()
C.CO2分子的结构式:![]() D.苯分子的填充模型:
D.苯分子的填充模型:
为测定碳酸钙纯度(设所含杂质为SiO2),同学们设计了如下两个实验方案:
【方案I】
(1)组装发生并测定生成气体体积的实验装置,并检验气密性;
(2)称取碳酸钙样品W g;
(3)加入过量盐酸;
(4)收集并测定生成的气体体积V mL。
问题I—1:如果称量样品时,砝码底部有一处未被实验者发现的残缺,那么测定的碳酸
钙的纯度会 (填“偏高、偏低、无影响”)。
问题I—2:在方框中画出测定生成的气体体积的装置简图。

【方案II】
(1)称取碳酸钙样品Wg;
(2)在锥形瓶中用C mol/L盐酸V mL(过量)溶解样品;
(3)加入甲基橙作指示剂,再用浓度为C1 mol/L的标准氢氧化钠溶液滴定过量的盐酸,用去氢氧化钠溶液V1毫升。(已知甲基橙的变色范围是pH=3.1~4.4)
问题II—1:未滤去不溶物SiO2,对测定结果是否有影响?(填有或无) ;
理由是 。
问题II—2:碳酸钙纯度表达式 。
【方案评价】
你认为以上两个方案中,最好的方案是 ,
另一个方案不够好的理由是 。
将0.1mol·![]() 的蜡酸钠溶液20mL与
的蜡酸钠溶液20mL与![]() 盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
A. ![]()
B. ![]()
C. ![]()
D. ![]()
下列氯化物中,既能由金属和氯气直接反应制得,又可由金属和盐酸反应制得的是( )
A. CuCl2 B. FeCl2 C. FeCl3 D. AlCl3
氰基烯酸酯在碱性条件下能快速聚合为 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:

已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;

回答下列问题:
(1)A的化学名称为 。
(2)G的结构简式为 ,G中的含氧官能团是________________。(填官能团名称)
(3)由B生成C的反应类型为 ,由C生成D的反应类型为 。
(4)由E生成F的化学方程式为 。
(5)H的同分异构体中,含有酯基,能发生银镜反应、核磁共振氢谱之比是1:1:3的同分异构体结构简式 。(写两种即可)
NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,一种生产NaClO2的工艺如下:

已知:①ClO2是一种强氧化性气体,浓度大时易分解爆炸。在生产使用时要用稀有气体或空气等进行稀释,同时避免光照、震动等。②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaC1。同答下列问题:
(1)最近科学家又在“反应”步骤的基础上研究出用H2C2O4代替SO2制备C1O2的新方法,该方法的化学方程式为_________________,该新方法最突出的优点是_______________。
(2)获得产品NaClO2的“操作”包括以下步骤:
①减压,55℃蒸发结晶;②趁热过滤;③_____________;④低于60℃干燥,得到产品。
(3)为了测定产品NaClO2的纯度,取上述所得产品12.5g溶于水配成1 L溶液,取出10.00mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(ClO2-被还原为C1-,杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度_______________________________。(提示:2Na2S2O3+I2==Na2S4O6+2NaI)
(4)NaClO2溶液中存在ClO2、HClO2、ClO2-、C1-四种含氯微粒。经测定25℃备含氯微粒浓度随pH的变化情况如图所示(C1-没有画出)。

①酸性条件下NaClO2溶液中存在C1-的原因是________________________(用离子方程式解释)。
②pH=5时,NaClO2溶液中ClO2、HClO2、ClO2-、C1-四种含氯微粒的浓度由大到小的顺序是____________________________________。
下列指定反应的离子方程式正确的是:
A.将铜丝插入稀硝酸中:Cu+4H++2NO===Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
关于原子结构、元素性质的说法正确的是 ( )
A 非金属元素组成的化合物中只含共价键
B. ⅠA族金属元素是同周期中金属性质最强的元素
C. 同种元素的原子均有相同的质子数和中子数
D. ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 7.8g Na2O2中含有的阴离子数为0.2NA
B. 在lL0.lmd·L-1氟化钠溶液中含有F-为0.1 NA
C. 标准状况下,3.36L乙烯和丙烯的混合气体中双键数目为0.15 NA
D. 56g铁粉和稀盐酸反应,转移的电子数为NA
某酸性溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法正确的是
A.溶液中离子浓度可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-)
B.该溶液不能由等物质的量浓度、等体积的盐酸和氨水混合而成
C.可由pH=3的盐酸与pH=11的氨水等体积混合而成
D.再通入适量氨气,溶液中离子浓度可能为:c(NH4+)>c(C1-)>c(H+)>c(OH-)
PVB(聚乙烯醇缩丁醛)和PI(聚异戊二烯)均为用途广泛的有机制品,用乙炔为原料制备PVB和PI的流程如图。

![]()
(1)A中的官能团名称是 。反应③的条件是 。
(2)已知反应⑤属于加成反应,上述转化中还有 (填序号)也属于该反应类型。
(3)E是A的同分异构体,E的核磁共振氢谱显示有2种不同化学环境的氢,且E能发生银镜反应E发生银镜反应的化学方程式是 。
(4)反应⑦的化学方程式是 。
(5)依照PI的合成路线,若将反应①中的反应物“![]() ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是 。
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是 。
(6)![]() ,以
,以 为原料合成
为原料合成 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。

具有去污作用的物质E可通过下列途径合成:
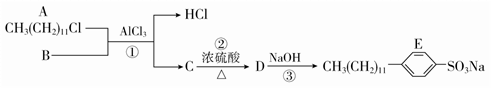
已知:![]() ;
;
苯磺酸能溶于NaOH溶液中。
请回答下列问题:
(1)A属于________(根据官能团写出其有机物类别)。
(2)烃B的结构简式为________________________,B与C的关系是____________。
(3)分别将B、C加入酸性高锰酸钾溶液中,现象是____________________。
(4)写出反应②的化学方程式:____________________________。
(5)写出A发生消去反应的化学方程式:____________________。
下列说法不正确的是
A.互为同系物的有机物,它们的分子结构必然相似
B.互为同分异构体的有机物,它们的分子式必然相同
C.凡相对分子质量相等、各元素的质量分数相等,而结构不同的有机物一定互为同分异
构体
D.凡分子组成相差一个或几个原子团的物质一定是同系物
钠与下列物质反应都能够产生氢气:①H2O;②CH3COOH;③CH3CH2OH。试推断这三种物质电离出H+的难易程度(从难到易的顺序)
A.①②③ B.②③① C.③①② D.②①③
X、Y、Z、W、R为五种短周期主族元素,且原子序数依次增大,X与W同主族,Z与R同主族,X的原子半径比Y的小,Y的最高价氧化物对应的水化物是强酸,Z的最外层电子数是其内层电子数的3倍。下列说法正确的是
A.原子半径:r(W)>r(Z)>r(Y)B.简单气态氢化物的热稳定性:Y>Z
C.R的氧化物对应的水化物均为强酸D.W2Z2与X2R均含有共价键
磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如图,下列说法正确的是( )

A. H3PO4的电离方程式为:H3PO4![]() 3H++ PO43−
3H++ PO43−
B. pH=2时,溶液中大量存在的微粒有:H3PO4、H2PO4−、HPO42−、PO43−
C. 滴加NaOH溶液至pH=7,溶液中c(Na+)= c(H2PO4−)+2c(HPO42−)+3c(PO43−)
D. 滴加少量Na2CO3溶液,3Na2CO3+2H3PO4 =2Na3PO4+3H2O+3CO2↑
瑞香素是一种具有抗菌、抗炎、抗凝血等生物活性的香豆素化合物,其分子结构如图所示。回答下列问题。

(1)瑞香素的化学式为 ,属于 类型有机物。
(2)1 mol此化合物可与 mol Br2反应,在一定条件下与H2反应时,最多消耗H2的物质的量为 mol。
(3)写出此化合物与强碱NaOH溶液反应的化学方程式 。
已知在一定条件下,Cl2、ClO2(其还原产物为 Cl-)、O3(l mol O3转化为 l molO2和molH2O)、H2O2等物质都具有氧化性,因而常被用作消毒剂。等物质的量的上述物质消毒效率最高的是 ( )
A. C12 B. ClO2 C. O3 D. H2O2
(一) 以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、CaO、MgO 等。现以硫酸渣制备铁红(Fe2O3),过程如下:

(1) 酸溶过程中Fe2O3与稀硫酸反应的离子方程式是_________________________。
(2) 还原过程中加入FeS2是将溶液中的Fe3+ 还原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:__________________________________________。
(3) 生产过程中,为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是_ __。
(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(二)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。

(1) 原混合物中NaOH的质量是________g。
(2) C点(此时沉淀恰好完全溶解)HCl溶液的体积为_________mL。
(三)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:


用右图装置可以测定混合气中ClO2的含量:
I、在锥形瓶中加入足量的碘化钾,用50ml水溶解后,再加入3ml稀硫酸;
II、在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
III、将一定量的混合气体通入锥形瓶中吸收;
IV、将玻璃液封装置中的水倒入锥形瓶中;
V、用0.1000 mol/L硫代硫酸钠标准溶液滴定锥形瓶中的溶液(![]() ),指示剂显示终点时共用去20.00ml硫代硫酸钠溶液。在此过程中:
),指示剂显示终点时共用去20.00ml硫代硫酸钠溶液。在此过程中:
①测定混合器中ClO2的质量为_____________g
②用![]() 处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是________。(填标号)
处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是________。(填标号)
A、.明矾 B、碘化钾 C、盐酸 D、硫酸亚铁
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体。W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是( )
A.原子半径:W>Y>Z>X
B.气态氢化物的稳定性:X<Z
C.最高价氧化物对应水化物的碱性:Y>W
D.Y、Z的氧化物都有酸性和碱性
- 如图所示,开关S闭合时,可能发生的现象是:A、L1被烧坏; B、L2
- (16分,每空1分)下图表示一个家庭的遗传图,请分析图并回答问题(1)如图所示,a.b分别表示父母的体细胞,他们的染色体
- 2010年9月6日,国民党荣誉主席连战宴请正在台湾访问的中华文化联谊会名誉会长蔡武等人时表示,文化是两岸的基础、是根,是
- “9·11”恐怖事件发生后,越来越多的国家认识到,反对恐怖主义是一场长期的艰巨的斗争,国际社会应加强合作,建立广泛的国际
- 面对“生辰纲”这笔巨大的财宝,负责押送的 A ,一路费尽心思,力求“生辰纲”不失;而 B 巧设妙计,众好汉志在必得。这场
- 根据所学知识,你认为贫血患者在平时的饮食中应多吃下列哪两种较丰富的物质( ) A.钙和维生素D B.
- 依次填入下列各句横线处的词语,最恰当的一组是 ①明确目的、设定目标后,为达到具体目标就需要的计划。 ②对于劳动竟赛中优胜
- 在一个平面内,任意三条直线相交,交点的个数最多有( )A. 7个 B. 6个 C. 5个
- 如图,在△ACB中,∠ACB=90°,AC=BC,点C的坐标为(﹣2,0),点A的坐标为(﹣6,3),则B点的坐标是 _
- 潜水员从水中观察到河岸树枝上的一只鸟,他看到的是 ( ) A、比实
- —Why don’t we choose that road to save time? —The bridge to
- 计算:.
- 下列属于化学变化的是 A.矿石粉碎 B.汽油挥发 C.石蜡熔化 D.煤气燃烧
- ......
- —Did Mr.White tell you______________? --Yes. He said he we
- 依次填入下列各句横线处的词语,最恰当的一组是 ( ) [1]经过全校师生的共同努力,这所普通
- 研究发现,长江干流江苏段河床在1985年前后平均冲淤状态发生了明显的转变,由淤积转变为冲刷,其主要原因是( ) A.
- 在运载庞大笨重的器件时,需用具有几十个轮胎的大型平板车,这是为了 ( )A 减小压力。 B 减小压强。
- Mr. Liu said he would come to the meeting.But he won’
- 新疆是古“ 丝绸之路”上的重要关结点,也是东西方文明的交汇点。西部大 开发战略又使新疆一跃成为西部贸易桥头堡,内联外引,



