高中 化学
(i) I2(g)+H2(g)⇌2HI(g)+9.48kJ
(ii) I2(s)+H2(g)⇌2HI(g)﹣26.48kJ,下列判断正确的是( )
 溶液中加入过量盐酸:
溶液中加入过量盐酸:  B . 将NaOH投入足量
B . 将NaOH投入足量  饱和溶液中:
饱和溶液中:  C . 铜与稀硝酸的反应:
C . 铜与稀硝酸的反应:  D . 向碳酸氢钠溶液中滴加少量石灰水:
D . 向碳酸氢钠溶液中滴加少量石灰水: 
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4 600 | 6 900 | 9 500 |
| Y | 580 | 1 800 | 2 700 | 11 600 |
 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列说法正确的是( )
 溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以
溶液的变化曲线
B . a处溶液的导电能力几乎为0,所以 是非电解质
C . c点两溶液中
是非电解质
C . c点两溶液中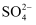 的物质的量关系:①
的物质的量关系:① ②
D . b~d的离子方程式为
②
D . b~d的离子方程式为

选项 | 生产活动 | 知识解读 |
A | 用干冰进行人工降雨 | 干冰升华吸热 |
B | 用生石灰作食品干燥剂 | 生石灰吸水,易与水反应 |
C | 向葡萄酒中通入少量 |
|
D | 利用氢氟酸刻蚀石英制作艺术品 | 氢氟酸可与 |
工业用铝上矿(组成: 主要Al2O3、还有Fe2O3、SiO2) 冶炼铝流程如下:

完成下列问题:
(1)填主要成分的化学式: 滤液A_______;滤渣B______;固体D_______。
(2)流程中每一步加入试剂都足量,X是无色无味无毒气体,X为_______。滤液B通入X气体生成沉淀的离子方程式________________。
(3)滤液A 加入足量的NaOH溶液过程中反应的离子方程式(不考虑过量盐酸的反应):________;____________。
(4)铝热反应可以焊接钢轨,写出铝与氧化铁用于焊接钢轨的化学方程式__________。
运用相关原理,回答下列各小题:
I.已知:硫酸氢钠在水中的电离方程式为___________________________
(1)常温下,pH=5的硫酸氢钠溶液中水的电离程度______pH=9的一水合氨中水的电离程度。(填“>”、”=”或“<”)
(2)等体积等物质的量浓度的硫酸氢钠与氨水混合后,溶液呈酸性的原因为______。(用离子方程式表示);若一定量的硫酸氢钠溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH4+)___2c(SO42-)(填“>”、“=”或“<”不同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的PH_____7(填“>”、”=”或“<”)
II.25℃时,电离平衡常数:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,bNaClO, c.CH3COONa d.NaHCO3;pH由大到小的顺序是:_______________________;(填编号)
(2)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中,c(CH3COO-)-c(Na+)=_____________。(填准确数值)
(1)如图是石油分馏塔的示意图。a、b、c三种馏分中________(填字母序号)。

A.a的沸点最高
B.b的熔点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
(2)裂化汽油中除含有C5~C11的烷烃外,还含有C5~C11的烯烃及甲苯、二甲苯等苯的同系物。已知甲苯、二甲苯能使酸性KMnO4溶液褪色。要用化学方法检验某裂化汽油样品中含有烯烃及苯的同系物,实验步骤为:
①先逐滴加入________,振荡,如果看到________,则证明有________存在;
②继续逐滴加入________至________为止,静置,用分液漏斗分出________(填“上”或“下”)层的裂化汽油样品,再加入________振荡,如果看到________,则证明裂化汽油中有________存在。
下列物质中,不含有硅酸盐的是( )
A.水玻璃 B.硅芯片
C.黏土 D.普通水泥
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mo1CH4中的氢原子被氯原子完全取代,共需要2NA个Cl2分子
B.常温常压下,mg乙烯与mg丙烯的体积相同
C.标准状况下,22.4 L苯所含的分子数为NA
D.46g乙醇与足量的金属钠反应,生成的气体在标准状况下的体积约为11.2L
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )

A. 甲能使酸性高锰酸钾溶液褪色
B. 乙可与溴水发生加成反应使溴水褪色
C. 丙中的碳碳键是碳碳单键和碳碳双键交替结合
D. 丁在稀硫酸作用下可与乙酸发生取代反应
- 下列函数中与y=x有相同图像的是( ) A. B. C.(且) D.
- 下列变化属于化学变化的是( ) A.铁杵磨针 B.胆矾被研碎 C .死灰复燃 D.葡萄榨汁
- 阅读下面的文字,完成15 — 17题。 “落后就要挨打”的观念是中国人在现代化过程中痛苦经历的总结。中国并不是自
- 当某种RNA存在时,生物体内的某种化学反应能正常进行,当这种RNA被有关的酶水解后,此种化学反应即可停止。由此可以说明
- 下图是某生态系统中食物网简图,图中甲~庚代表各种不同的生物。已知各营养级之间的能量传递效率为10%,若一种生物摄食两种前
- 温家宝总理在2010年新春团拜会上提出,“要让人民生活得更加幸福、更有尊严”。在十一届全国人大三次会议上,“人民的尊严”
- 有关基因工程的叙述正确的是() A.限制酶只在获得目的基因时才用 B.重组质粒的形成是在细胞内完成的 C.任何质粒都可作
- 填入下面横线处的句子,与上下文衔接最恰当的一项是( ) (2分)走进这所学校,会被一种大气震慑住。一条宽阔笔直的
- 如图所示,直立容器内部有被隔板隔开的A、B两部分气体,A的密度小,B的密度较大,抽去隔板,加热气体,使两部分气体均匀混合
- 现有一台显微镜,配有两个物镜A(10×)、B(40×)和两个目镜C(5X).D(lOX):(1)对光时,应选用的物镜是
- 下列图标中,表示“禁止吸烟”的是 A B C D
- 下面横线上填入句子组成一段语意连贯的话,句子排列的正确顺序是( )(2分) 宽展的湖面上到处浮动着大大小小
- 23.— What’s that terrible noise.David? — Oh,I forgot t
- 方程=1表示的曲线为C,给出下列四个命题: ①曲线C不可能是圆; ②若1<k<4,则曲线C为椭圆; ③若曲线C为双曲
- 已知等比数列{an}中,a1+a2=1,a3+a4=4,则a5+a6=() A. ±16 B. 16 C. 32 D.
- Parents should stop blaming themselves because there’s not
- —Why didn’t Betty come to school yesterday?—_________ she wa
- 有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式为( )A.I2O4
- What you said just now ________me of that American professor
- 如图所示的标志的意思是__________________________。若在空气不流通房间里,只要有一个人吸烟,整个
 进行防腐,起到保质作用
进行防腐,起到保质作用 反应
反应


