高中 化学
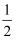 O2(g)△H=﹣485kJ•mol﹣1
B . H2O(g)═H2(g)+
O2(g)△H=﹣485kJ•mol﹣1
B . H2O(g)═H2(g)+ 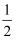 O2(g)△H=+485kJ•mol﹣1
C . 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D . 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1
O2(g)△H=+485kJ•mol﹣1
C . 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D . 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1
 减少的是( )
减少的是( )
 ,将其转化为氮肥
B . 大力推广使用风能、水能、氢能等清洁能源
C . 大力推广使用干冰实现人工增雨,缓解旱情
D . 通过植树造林,利用光合作用吸收大气中的
,将其转化为氮肥
B . 大力推广使用风能、水能、氢能等清洁能源
C . 大力推广使用干冰实现人工增雨,缓解旱情
D . 通过植树造林,利用光合作用吸收大气中的 
| 选项 | 操作和现象 | 结论或目的 |
| A | 将饱和的 | 制备 |
| B | 向钠与水反应形成的溶液中滴加几滴酚酞,溶液变红 | 钠与水反应生成了碱 |
| C | 向 | 沉淀为 |
| D | 向某溶液中通入 | 原溶液中一定含有 |
-
(1) I.制备氢气
制备氢气常采用以下方法:
①电解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑②水煤气法:C+H2O(g)
 CO+H2 , CO+H2O
CO+H2 , CO+H2O  CO2+H2↑
CO2+H2↑③太阳能光催化分解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑三种方法中最节能的是(填标号)。
-
(2) 已知拆开1 mol H -H、1 mol O=O和 1 mol H-О分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每3.6 gH2O(g)完全分解,需(填“放出”或“吸收")能量kJ。下列能正确表示该过程的能量变化示意图的是(填标号)。

-
(3) II.氢燃料电池
氢燃料电池具有清洁高效等优点,其简易装置如下图所示。

该电池正极反应式为;反应过程中将能转化为能。
A.化学键没有被破坏的是;
B.仅发生离子键破坏的是;
C.仅发生共价键破坏的是;
D.既发生离子键又发生共价键破坏是.
-
(1) I.制备银镜
下列有关制备银镜过程中的相关描述错误的有____(填标号)。
A . 边振荡盛有2%的 溶液的试管,边逐滴滴入2%的氨水,使最初产生的沉淀溶解,得到银氨溶液
B .
溶液的试管,边逐滴滴入2%的氨水,使最初产生的沉淀溶解,得到银氨溶液
B .  是配位化合物,配位原子是N,中心离子的配位数是2
C . 将几滴银氨溶液滴入2mL乙醛中,用酒精灯的外焰给试管底部加热,一段时间后,产生银镜
D . 只有醛类物质才能发生银镜反应
是配位化合物,配位原子是N,中心离子的配位数是2
C . 将几滴银氨溶液滴入2mL乙醛中,用酒精灯的外焰给试管底部加热,一段时间后,产生银镜
D . 只有醛类物质才能发生银镜反应
-
(2) II.去除银镜
用一定浓度的
 去除银镜,此法的缺点是。
去除银镜,此法的缺点是。 -
(3) 利用
 溶液去除银镜:
溶液去除银镜:i.配制溶液:配制
 溶液时,需用到的玻璃仪器除了烧杯、量筒、胶头滴管、玻璃棒外,还有①。
溶液时,需用到的玻璃仪器除了烧杯、量筒、胶头滴管、玻璃棒外,还有①。ii.将
 溶液(pH≈2)加入有银镜的试管中,充分振荡,银镜部分溶解。于是,进行如下相关实验探究。
溶液(pH≈2)加入有银镜的试管中,充分振荡,银镜部分溶解。于是,进行如下相关实验探究。猜想a:
 氧化了Ag;猜想b:
氧化了Ag;猜想b: 时,
时, 氧化了Ag
氧化了Ag为验证猜想,设计如下实验。
(限选试剂:A.
 溶液
溶液 B.
B. 溶液C.
溶液C. 溶液
溶液 D.
D. 溶液)
溶液)操作
现象
结论
取少量上述溶解银镜后的溶液,滴加几滴
 溶液
溶液②
猜想a成立,溶解银镜的离子方程式为③
将④(填试剂对应标号)两种溶液等体积混合,取4mL混合溶液,加入有银镜的试管中,充分振荡
银镜不溶解
猜想b不成立
-
(4) 利用
 溶液去除银镜:将
溶液去除银镜:将 溶液,加入有银镜的试管中振荡,银镜全部溶解,且有白色沉淀产生。将分离得到的白色沉淀置于试管中,滴加氨水,沉淀溶解,该沉淀溶解的离子方程式为。
溶液,加入有银镜的试管中振荡,银镜全部溶解,且有白色沉淀产生。将分离得到的白色沉淀置于试管中,滴加氨水,沉淀溶解,该沉淀溶解的离子方程式为。
-
(5) 相同条件下,
 溶液比
溶液比 溶液去除银镜更彻底,其原因是。
溶液去除银镜更彻底,其原因是。
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验 |
| D | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
已知A~G是几种烃分子的球棍模型,据此回答下列问题:

(1)如图七种烃中:
①常温下含氢量最高的气态烃是 (填对应结构简式).
②能够发生加成的烃有 种.
③分子中所有原子共面的是 (填对应字母).
④属于芳香烃的是 (填对应分子式)
(2)由D可制取重要的化工原料聚氯乙烯,其中涉及到的反应类型有2种,依次是 和 .
下列化学反应在冶金工业中没有得到广泛应用的是 ![]()
A.MgC12(熔融)![]() Mg+C12↑ B.A12O3+3C
Mg+C12↑ B.A12O3+3C ![]() 2A1+3CO↑
2A1+3CO↑
C.Fe2O3+3CO![]() 2Fe+3CO2 D.2Ag2O
2Fe+3CO2 D.2Ag2O![]() 4Ag+O2↑
4Ag+O2↑
在一定温度下,发生如下反应:N2+3H2
和H2的物质的量分别是3.0 mol和6.0 mol,平衡时生成NH3的物质的量是2.4 mol。
已知容器的容积为5.0 L,试求:(1)H2的转化率。(2)平衡时混合气体中N2的体积分数。
等温等压时,等质量的CH4与X气体的体积比为15 : 8 ,则X气体的摩尔质量
为______
将一小块钠投入到FeCl3溶液中,观察到的现象是( )
A.钠溶解,有铁析出并有气体产生 B.只有气体产生
C.既有气体产生,又有红褐色沉淀产生 D.只有沉淀产生
下列分子中,所有原子均在同一平面的是
A.甲醛 B.甲苯 C.一氯甲烷 D.2甲基丙烯
下列说法正确的是![]()
![]()

A. 由图甲可知,升高温度醋酸钠的水解程度增大
B. 由图乙可知,a点![]() 的数值比b点
的数值比b点![]() 的数值大
的数值大
C. 由图丙可知,反应![]() 是吸热反应
是吸热反应
D. 由图丁可知,反应![]() 金刚石,
金刚石,![]() 石墨,
石墨,![]() 的焓变
的焓变![]()
- 函数f(x)=ax3+bx2+cx+d的部分函数值如下表,则函数y=lgf(x)的定义域为______________.
- 17.阅读下面的材料,根据要求写一篇不少于800字的文章。(60分) 台湾爱乐乐团到大陆某市演出,场地两侧不断打出“演出
- 秋水仙素使染色体数加倍的生理作用机制是 A.抑制细胞有丝分裂时形成纺缍体 B.使细胞连续进行染色
- When I learned that my71-year-old mother was playing Scr
- 直线在轴上的截距是( ) A. B. C. D.
- 下列实验操作正确的是 ( )
- 如图,在数轴上的点A、点B之间表示整数的点有 个
- 解不等式
- (8分)某溶液仅含下表离子中的5种(不考虑水的电离及离子的水解,且各种离子物质的量均为0.1mol。 ①若向溶液中加入
- 1956年,我国工业总产值642亿元,占工农业总产值的51.3%,比1952年增长84%。其中生产资料工业产值占工业总产
- 汉字凝聚着中华民族的智慧,包藏着丰富的艺术内蕴。汉字的艺术内蕴大致饱含形美、音美、义美、意美和情美几个方面。汉字无穷的生
- 如图1-53(原图1-56)所示,直杆OA可绕O轴转动,图中虚线与杆平行.杆的A端分别受到F1、F2、F3、F4四个力作
- 根据汉语拼音写出汉字。 (yì)_____断 宽(yòu)_____ (jié) _____然不同
- 江西不仅山清水秀、景色迷人,特色美食更是遍布各地令各路“吃货”流连忘返. (1)南昌“藜蒿炒腊肉”风味独特,清香扑鼻.从
- 下列物质在氧气中燃烧,火星四射,有黑色固体生成的是( ) A.硫 B.木炭 C.铁丝 D.红磷
- 下列说法中,正确的是 A.SO2和SO3互为同分异构体 B.二氧化碳和干冰互为同素异形体 C.金刚石和
- 在平面直角坐标系中,对于任意两点与的“非常距离”,给出如下定义: 若,则点与点的非常距离为; 若,则点与点的非常距离为;
- 化简求值 2(a2+ab2)-2(a2b-1)-2ab2+a-2,其中a=-2,b=2。
- 如图所示,开关S1闭合,当S2由1掷到2,电流表和电压表的示数变化情况是 A.电流表示数变小,电压表示数变大 B.电
- (2013·四川文综·14)(24分)课程变化与时代发展紧密相关。阅读材料,回答问题。 材料一 1912年四川军政府令
 溶液滴加到浓
溶液滴加到浓  溶液中
溶液中 胶体
胶体 溶液中加入一小块钠,生成气体和沉淀
溶液中加入一小块钠,生成气体和沉淀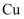
 ,再加入
,再加入  溶液,溶液变红色
溶液,溶液变红色




