高三化学试题
NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol
若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式____________。
,请写出此反应的热化学方程式____________。
(2)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:_________________________。
(3)NO2用氨水吸收能生成NH4NO3,25℃时,将amolNH4NO3溶于水配成bL溶液,溶液显酸性,常温下向该溶液通入标准状况下VL氨气后溶液呈中性,则通入氨气的过程中水的电离平衡将_____(填“正向”“不”“逆向”)移动,通入标准状况下氨气的体积为_________L(设通入氨气后溶液的体积不变,用含a的代数式表示,已知常温下NH3·H2O的电离平衡常数为2.0×10-5)
(4)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO![]() 5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:
5N2+6H2O不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示:

①由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是________。
②曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_____________mg/(m3·s)。
③曲线c对应NH3与NO的物质的量之比是____________。
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.足量的铁在1 mol氯气中燃烧,转移电子数为2 NA
B.42g NaHCO3晶体中含有CO32-的数目为0.5NA
C.0.1 mol/L的NaClO溶液,含有的ClO-数目小于0.1NA
D.常温常压下,5.6 L二氧化碳气体中含有的氧原子数为0.5NA
中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )
A.用胆矾炼铜 B.用铁矿石炼铁
C.烧结粘土制陶瓷 D.打磨磁石制指南针
Ⅰ.某厂废水中含KCN,其浓度为0.01 mol·L-1,现用氯氧化法处理,发生如下反应(化合物中N化合价均为-3价):
KCN+2KOH+Cl2 = KOCN+2KCl+H2O
(1)上述反应中被氧化的元素是________(用元素符号表示)。(1分)
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:(2分)
______KOCN+____Cl2+______![]() = ______K2CO3+______N2+______KCl+______
= ______K2CO3+______N2+______KCl+______![]()
(3)若将10 L含KCN的浓度为0.01 mol·L-1的废水中KCN氧化除去,最少需要氯气________ mol。(2分)
Ⅱ.某实验小组为了测定(3)中溶液多余Cl2的含量,常用Na2S2O3标准溶液进行定量测定。
(4)现实验室需用480 mL一定浓度的Na2S2O3溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需________。(1分)
(5)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO![]() ,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为_________________。(2分)
,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为_________________。(2分)
下列说法正确的是( )
A.阳离子只有氧化性,阴离子只有还原性
B.失电子难的原子获得电子的能力一定强
C.得到电子越多的氧化剂,其氧化性就越强
D.要实现Fe2+到Fe3+的转化,必须加入氧化剂
下列有关化学用语使用不正确的是 ( )
A.NH4Br的电子式:![]() B.S2-的结构示意图:
B.S2-的结构示意图:![]()
C.乙酸的结构简式: CH3COOH D.原子核内有l8个中子的氯原子:![]()
 下表是元素周期表的一部分,有关说法不正确的是
下表是元素周期表的一部分,有关说法不正确的是
A.元素e的氧化物对应的水化物均为强酸
B.a、b、d、e四种元素的离子半径:![]()
C.b、f两种元素形成的化合物为离子化合物
D.a、c、e的最高价氧化物对应的水化物之间能够相互反应
常温下,向10mL0.1mol·![]() 的HA溶液中逐滴滴入0.1mol·
的HA溶液中逐滴滴入0.1mol·![]() 的ROH溶液,所得溶液pH及导电能力的变化如图,下列判断正确的是
的ROH溶液,所得溶液pH及导电能力的变化如图,下列判断正确的是

A. ROH在溶液中的电离方程式为![]()
B. c点由![]() 电离出的
电离出的![]() 浓度最小
浓度最小
C. b点存在: ![]()
D. 若升高温度,a、d两点pH增大
.把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水配制成100 mL混合溶液,用石墨作电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下的体积相同。则下列描述正确的是( )
A.电路中共转移0.9 mol电子
B.阳极得到的气体中有O2,且其物质的量为0.35 mol
C.阴极的质量增加3.2 g
D.铝元素仅以Al(OH)3的形式存在
在一定温度下的定容密闭容器中,下列情况能表明可逆反应:H2(g)+I2(g) ![]() 2HI(g)已达平衡的是
2HI(g)已达平衡的是
A.H2的生成速率与I2的生成速率相等
B.若单位时间内生成n mol H2的同时生成2n mol HI
C.H2、I2、HI的浓度相等
D.反应容器内的压强不随时间的变化而变化
.某实验小组对一含有Al 3+ 的未知溶液进行了如下分析:(1)滴入少量氢氧化钠,无明显变化;(2)继续滴加NaOH溶液,有白色沉淀;(3)滴入过量的氢氧化钠,白色沉淀明显减少。实验小组经定量分析,得出如图所示沉淀与滴入氢氧化钠体积的关系。下列说法正确的是( )

A.该未知溶液中至少含有4种阳离子
B.滴加的NaOH溶液的物质的量浓度为0.5 mol·L -1
C.若另一种离子为二价阳离子,则a=10
D.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6g
下列离子方程式不正确的是( )
A.用Fe电极电解NaCl溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.四氧化三铁溶于氢碘酸:Fe3O4+8H+ +2I-=3Fe2+ +4H20+I2
C.碳酸氢钠溶液中加入足量澄清石灰水:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.硫酸氢钠溶液与氢氧化钡溶液混合显中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
某国外化学教材中有一张关于氧化还原反应的插图:
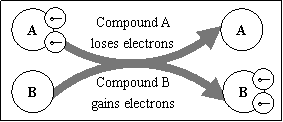 |
由图可知,
![]() 在该反应中是
在该反应中是
A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接和油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
| C | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+ 2Fe(s),ΔH=+234.1kJ••mol-1
CO2(g)+ 2Fe(s),ΔH=+234.1kJ••mol-1
C(s)+O2(g)=CO2(g);ΔH=-393.5kJ••mol-1
则2Fe(s)+ ![]() O2(g)=Fe2O3(s)的ΔH是
O2(g)=Fe2O3(s)的ΔH是
A、-824.4 kJ••mol-1 B、-627.6kJ••mol-1
C、-744.7kJ••mol-1 D、-169.4kJ••mol-1
用下图表示的一些物质或概念之间的从属或包含关系中错误的是( )

| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 溶液 | 分散系 | 混合物 |
| B | 铜 | 金属元素 | 元素 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
已知:①甲醛(HCHO)与葡萄糖化学性质相似,都具有还原性。②甲醛易挥发,甲酸钙易溶于水。为探究过量的甲醛和新制Cu(OH)2反应的产物,进行如下实验:
(1)在下图装置中进行实验,向a中加入0.5mol·L-1CuSO4溶液50mL和5②甲醛易挥发,甲酸钙易溶NaOH 溶液100mL,振荡,再加入40%的甲醛溶液50mL,缓慢加热20分钟后冷却至室温。

仪器a、b的名称分别是________________、_______________。
(2)上述实验有副反应发生,产生的气体为CO、H2中的一种或两种。为确认气体成分,将装置A 和如下图所示装置连接后进行实验。

依次连接的合理顺序为A→____→____→____→____→____→G
副产物中如果有CO,实验现象是:_____________________________________。
(3)已知HCHO 最终被氧化为CO32-,请写出a容器中发生的反应化学方程式:_________________________________________。
(4)反应后a中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O 假设二:只有Cu
假设三:Cu2O和Cu 假设四:_______________;
其中假设三明显不成立,理由是___________________________________。
(5)为了对(4)的猜想进行验证,进行如下实验(以下任步均充分反应):
已知:已知:Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+ (蓝色)
[Cu(NH3)4]2+ (蓝色)

①锥形瓶ii中固体加入浓氨水后,完全溶解得到深蓝色溶液,该过程所发生的离子方程式为 __________________________________________;
②将容量瓶ii中的溶液稀释20倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为_________________________________
.随着现代科学技术的快速发展,防腐蚀技术也在不断提高。
Ⅰ.金属的腐蚀原理
(1)中性环境中多为吸氧腐蚀,其正极的电极反应为________。
(2)析氢腐蚀和吸氧腐蚀的均会导致体系中c(OH-)________(填“增大”、“不变”或“减小”)。
(3)不同酸性介质中,金属腐蚀原理并不相同。下图是密闭容器中,生铁在pH=2和pH=4的盐酸中压强随时间的变化过程。

图中代表pH=2的曲线是________(填“a”或“b”)。
Ⅱ.金属的电化学防护
(1) 富锌涂料是使用广泛的防锈底漆,涂层中锌对钢铁保护的原理是________。
(2) 缓蚀剂是能明显减缓或阻止金属腐蚀的物质,钼酸钠(Na2MoO4)和磷酸二氢锌[Zn(H2PO4)]2是常用自来水(pH范围6.5~8.8)介质碳钢缓蚀剂。
①钼酸钠(Na2MoO4)在电极表面被还原为MoO2形成保护膜,减缓腐蚀,该电极反应为______;同时,MoO42-能与Fe2+反应生成难溶的Fe2O3和MoO2,沉积在碳钢表面减缓腐蚀。写出MoO42-与Fe2+反应的离子反应方程式:_______。
②电化学反应可使缓蚀剂成分中的Zn(H2PO4)2转化为难溶性的Zn3(PO4)2,形成保护膜,减缓腐蚀。用平衡移动原理解释发生转化原因________。
下列现象反映了硫酸的哪些主要性质:
(1)浓硫酸滴在木条上,过一会儿,木条变黑. .
(2)敞口放置浓硫酸时,质量增加. .
(3)锌粒投入稀硫酸中,有气泡产生. .
(4)铜片放入浓硫酸里加热,有气体产生. .
(5)浓硫酸可用铁制或铝制的容器储存和运输. .
某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是________________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是______________________________。再由a向c中加2mL蒸馏水,c中的实验现象是_______________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是_____________,理由是_____________________________________。

(4)该小组同学向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸。观察到的实验现象是________________________;该小组同学实验目的是_________________,但此实验的不足之处是_____________________________。
- 下列对必要劳动时间与剩余劳动时间的认识中,正确的有( )。 ①.雇佣工人在必要劳动时间内创造劳动力自身的价值 ②.雇佣工
- 20世纪初来中国访问的美国学者杜威在写给女儿的信中说:“要使我们国家14岁多的孩子领导人们展开一场大清扫的政治改革运动,
- 下列各句中,加点的成语使用恰当的一句是( ) A、时间真如行云流水,一晃这么多年过去了,望着镜中的两鬓白发,他不由
- 茶叶要求在避光、干燥的条件下贮存,常温下保质期一般为18个月。为延长茶叶的保质期,贮存少量茶叶的方法是:将茶叶包装好放入
- 阅读下面文段,回答以下问题: 于休烈,河南人也。至性贞悫,机鉴敏悟。自幼好学,善属文。举进士,授秘书省正字。转比部员外郎
- 两列波叠加发生了干涉现象,得到了稳定的干涉图样.则下列关于干涉的说法中,正确的是( )A.两列波的频率一定相等,振
- 已知函数是奇函数,且,则 为( ) A.0 B.1 C.
- 当交叉路口的信号灯转变为绿灯时,一辆汽车以3m/s2的加速度由静止开行,恰在此时,有一辆货车经过此处,并以6m/s的速度
- 下列两幅示意图反映了欧洲人对世界认识的巨大变化,导致这种变化的主要原因是 A.新航路的开辟
- 过氧化氢与硫酸酸化的高锰酸钾溶液进行反应生成硫酸钾、硫酸锰、水和氧气。如果过氧化氢中的氧原子是示踪原子(18O),当反应
- 读下面这首诗,完成(1)~(3)题。 遇旧友 吴伟业 已过才追问,相看是故人。乱离①何处见,消息苦难真。 拭眼惊
- 下列关于物质跨膜运输的叙述,正确的是( ) A.离子都是通过被动运输进入细胞的 B.大分子物质只能通过主
- 下图装置中,构成原电池的是( )
- 在温度、光照等适宜条件下,将消毒后有生活力的小麦种子一直浸没在无菌水中,会使种子死亡。下列对种子死亡原因的分析,合理的是
- The pair of leather boots that I bought last weekend_______
- (13分)大麦种子结构如图1所示,发芽时,胚产生赤霉素。有人推测赤霉素扩散到糊粉层,诱导合成淀粉酶,淀粉酶再分泌到胚乳中
- 人的唾液腺细胞中,比汗腺细胞中显著增多的细胞器是 A.中心体 B.高尔基体 C.线粒体 D
- 对下列四种情况:①崇明岛的形成;②用黄豆制豆腐;③向某浓度的硅酸钠溶液中滴加适量盐酸无可见现象;④钢笔灌用不同牌号蓝墨水
- 千百年来,中华民族一次次战胜了天灾人祸,昂首挺胸地走到今天,因为中华民族拥有自强不息的意志和精神。这表明,自强不息是中华
- 近代中国有人提出:“议院者,公议政事之院也。……使昏庸之君无所施其虐,跋扈之君无所擅其权……”从中可以看出此人主张在中国



