高三化学试题
下列用品的有效成分及用途对应错误的是 ( )
| A | B | C | D | |
| 用品 |
|
|
|
|
| 有效 成分 | NaCl | Na2CO3 | Al(OH)3 | Ca(ClO)2 |
| 用途 | 做调味品 | 做发酵粉 | 做抗酸药 | 做消毒剂 |
短周期元素X、Y、Z、W在元索周期表中的相对位置如右下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
 A.原子半径:W>Z>Y>X
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:X>W>Z
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素X、Z、W的最高化合价分别与其主族序数相等
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是 ( )
①2Na2O2+2H2O=4NaOH+O2↑ ②4Fe(OH)2+O2+2H2O=4Fe(OH)3
③2F2+2H2O=4HF+O2 ④2Al+2NaOH+2H2O=2NaAlO2+3H2↑
A.①③ B.②③ C.③④ D.②④
酒石酸是某种降压药物的载体,可用1,3-丁二烯为原料合成,其流程如下:
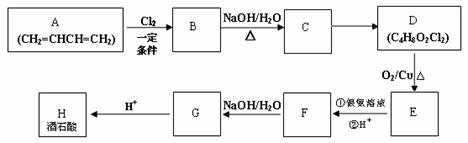
已知:① 
② D的分子组成是C4H8O2Cl2 ,核磁共振氢谱显示其有三个峰。
(1)D中所含官能团的名称是 ,C转化为D的反应类型是 。
(2)B存在顺反异构,它的顺式结构简式是 。
(3)写出A生成B的化学方程式 。
(4)与C互为同异构体,且属于酯类、能发生银镜反应的有机化合物的
结构简式 。
(5)F转化为G的化学反应方程式是 。
(6)F与乙二醇在一定条件下可以发生缩聚反应,该反应的化学方程式是
__ 。
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2===2Fe(OH)2。以下说法正确的是( )
A.负极发生的反应为:Fe-2e-===Fe2+
B.正极发生的反应为:2H2O+O2+2e-=4OH-
C.钢和铁都是铁合金,所以它们的组成基本相同
D.插在水中的钢柱在水下部分比在空气与水交界处更容易腐蚀
对下列化学用语的理解和描述均正确的是
A.离子方程式H++OH-===H2O可表示所有强酸与强碱溶液的反应
B.原子结构示意图![]() 可以表示12C,也可以表示l4C
可以表示12C,也可以表示l4C
C.比例模型![]() 可以表示二氧化碳分子,也可以表示水分子
可以表示二氧化碳分子,也可以表示水分子
D.电子式![]() 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子
已知a g气体X2中含有b个X原子,那么c g该气体在0℃、1.01×105 Pa条件下的体积是(NA表示阿伏加德罗常数的值) ( )
A.![]() L B.
L B.![]() L C.
L C.![]() L D.
L D.![]() L
L
下列说法正确的是
A.120℃,将wg甲醛在足量空气中燃烧,将生成产物用固体Na2O2(过量),固体增重wg
B.24gMg带在足量CO2气体中燃烧,生成固体质量为40g
C.相同物质的量的Al、Al2O3、Al(OH)3与足量NaOH溶液反应,溶液增重相等
D.在Fe3O4与足量浓硝酸的反应中,参加反应的Fe3O4与体现酸性的HNO3物质的量之比为1:10
氯气用于自来水的杀菌消毒,但在消毒时会产生一些负面影响,因此人们开始研究一些新型自来水消毒剂。某学习小组查阅资料发现NCl3可作为杀菌消毒剂,该小组利用下图所示的装置制备NCl3,并探究NCl3的漂白性。NCl3的相关性质如下:
| 物理性质 | 制备原理 | 化学性质 |
| 黄色油状液体 熔点为-40℃,沸点为71℃ 不溶于冷水,易溶于有机溶剂 密度为1.65 g/mL | Cl2与NH4Cl水溶液在低温下反应 | 95℃爆炸热水中发生水解 |

回答下列问题:
(1)根据实验目的,接口连接的顺序为______________________。
(2)C装置中盛放的试剂为_____________;E装置中盛放的试剂为______________。
(3)A装置中发生反应的离子方程式为_________________________。
(4)B装置中发生反应的化学方程式为_________________________,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为______________ 。
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,写出该油状液体与热水反应的化学方程式_____________ _。

二异丙烯基苯是工业上常用的交联剂,可用于制备高性能超分子聚合物,其结构如下图所示。下列有关二异丙烯基苯的说法错误的是
A.在催化剂存在下可发生加聚反应
B.与液溴混合后加入铁粉可发生取代反应
C.分子中所有碳原子可能都处于同一平面
D.其一氯代物有6种
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )

A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
下列离子方程式正确的是
A. 铝溶于NaOH溶液中:Al+2OH-=AlO2-+H2↑
B. 用Pt电极电解饱和氯化镁溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C. 向Fe(OH)3浊液中滴加HI溶液:Fe(OH)3+3H+ =Fe3++3H2O
D. 向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++2HCO3—+2OH—=CaCO3↓+CO32-+2H2O
下列指定反应的离子方程式正确的是
A.Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+H++Cl-+ HClO
B.向FeCl2溶液加入足量NaClO溶液:6Fe2++3ClO-+3H2O=2Fe(OH)3↓+4Fe3++3Cl-
C.NH4HCO3溶液和少量的NaOH溶液混合:NH4++OH-=== NH3.H2O
D.向Fe(NO3)3溶液中加入足量的HI溶液:2Fe3++2I- = 2Fe2++I2
用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验合理的是 ( )
A.上下移动①中铜丝可控制产生SO2的速率
B.②中选用KMnO4溶液验证SO2的漂白性
C.③中选用NaHSO3溶液吸收多余的SO2
D.为确认CuSO4生成,向①加水,观察颜色

已知NH4CuSO3与足量的3 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )
A. 构反应中硫酸作氧化剂
B. NH4CuSO3中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 1 mol NH4CuSO3完全反应转移0.5 mol电子
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为______。
③、④、⑤、⑥简单离子半径由小到大的顺序为______。
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是______。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______。
(4)由表中两种元素的原子按1:1组成的常见液态化合物易被催化分解,可使用的催化剂为__________。
a.MnO2 b.FeCl3 c.CuSO4 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

a) X溶液与Y溶液反应的离子方程式为_________,
b) N→⑥的单质的化学方程式为________________。
由有机物A合成G(香豆素)的步骤如下:

已知反应:![]()
(X为卤原子,M为烃基或含酯基的取代基等)
回答下列问题:
(1)G中含氧官能团名称为_________;写出反应类型:B→C_______________
(2)写出结构简式:F_________
(3)C + D→F化学方程式为:_________________
(4)符合下列条件的D的同分异构体有___________种。
①能发生银镜反应②能与FeCl3溶液发生显色反应
(5)参照上述合成路线,写出以苯和乙烷为原料(无杌试剂任选)制备合成苯乙烯的合成路线:______________________________________

A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C元素的最高价氧化物的水化物是一种中强碱,甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )
A. C、D两元素形成化合物属共价化合物
B. C、D的简单离子均能促进水的电离
C. A、D分别与B元素形成的化合物都是大气污染物
D. E的氧化物水化物的酸性大于D的氧化物水化物的酸性
下列化学用语或名称表述不正确的是( )
A. 葡萄糖的分子式:C6H12O6
B. HCl的电子式:![]()
C.  的名称:2﹣甲基丙烷
的名称:2﹣甲基丙烷
D. 含有10个中子的氧原子可表示为:![]() O
O
已知:①25℃时弱电解质电离平衡数:Ka(CH3COOH)=![]() ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=![]()
②25℃时,![]() mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:


请根据以下信息回答下列问题:
(1)25℃时,HF电离平衡常数的数值Ka= 。
(2)25℃时,将20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与20mL 0.10 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为图2所示:
反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是 ,反应结束后所得两溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)
(3)![]() mol·L-1HF溶液与
mol·L-1HF溶液与![]() mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。
(4)已知CH3COONH4溶液为中性,又知CH3COOH溶液加到Na2CO3溶液中有气体放出,试推断NH4HCO3溶液的pH 7(填“>”、“<”或“=”);
将同温度下等浓度的四种盐溶液:
A. NH4Cl B. NH4SCN C. CH3COONH4 D. NH4HCO3
按(NH4+)由大到小的顺序排列是: (填序号)。
按pH由大到小的顺序排列是: (填序号)
- 一列简谐横波沿x轴传播,某时刻的波形如图所示.关于波的传播方向与质点a、b、c、d、e的运动情况,下列说法正确的是(A)
- 香港政府庆祝回归10周年的时候,推出了一首名为《始终有你》的主题曲,其中唱道:“明艳紫荆风中争胜,找对了路径,花瓣开的繁
- 中学生活充满竞争,学习生活之中难免会感到紧张、产生压力。关于学习压力,以下看法正确的是 A.学习压力都是由过度的考试焦虑
- 阅读下面文章,完成13-17题。(16分)
- .—May I speak to Professor Brown, please? —Sorry, he isn’t i
- 下列对于基因突变的叙述中,正确的是( ) A.基因突变只发生在减数分裂中 B.基因突变多数
- 有一个小灯泡上标有“4V,2W”的字样;现要用伏安法溅量这个小灯泡的伏安特性曲线。现有下列器材供选用:A.电压表Vl (
- 有关燃料的下列说法中,不正确的是()A. 化石燃料都是可再生的能源 B. 氢气是理想的清洁、高能燃料 C. 石油是由不同
- 如图所示,A、B、O、C为在同一竖直平面内的四点,其中A、B、O沿同一竖直线,B、C同在以O为圆心的圆周(用虚线表示)
- 若a,b,c>0且ab+bc+ca=1,则a+b+c的最小值为( )A.1 B.2
- 假设你们学校将于本周六在学海路举行一次慈善义演。请写信告诉你的好朋友Alan, 希望他能参加这次公益演出,以支持希望工程
- 材料一 天上的一切星宿,地上的一切陈设,总之,构成大宇宙的一切物体,在心灵以外都没有任何存在;它们的存在就是被感知或被
- “假日经济”充分说明旅游资源具有( )A.美学价值 B.科学价值 C.历史文化价值 D.经济价
- 对商鞅变法历史作用的评价不准确的是() A.秦国的经济得到迅速发展 B.军队战斗力显著提高 C.秦国很快成为战国后期最富
- He managed to cross the b_______ into Germany.
- (2013年甘肃省五市联考)如图所示,放在水平地面上的质量为m的物体,与地面的动摩擦因数为μ,在劲度系数为k的轻弹簧作用
- 天坛是明清皇帝用来祭天、祈谷的地方,其建筑“反映出天地之间的关系”,“还体现出帝王将相在这一关系中所起的独特作用”。最早
- 小李设计的以下实验方案中,可行的是() A.用二氧化锰鉴别过氧化氢和蒸馏水 B.用稀盐酸检验某黄金饰品中是否含有铜 C.
- 有六种无色溶液,已知它们分别是Na2CO3、Na2SO4、NaClO、KI、BaCl2和HCl的溶液,要求不用试剂把它们
- (2013年乐山) 不容忽视的“镉大米” 人们总是在食品安全中学习化学知识,两年前“10%大米镉超标”的新闻让人们空前关







