高三化学试题
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
请回答下列问题:(1)B、C、D三种元素的电负性由小到大的顺序为 ,E的基态原子的电子排布式为 。(2)由B、D形成的BD32-离子中,其VSEPR模型名称是 ,离子的中心原子采用 杂化。
(3)已知由A、C、D三种元素按照4:2:3的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=5,则该溶液中水电离出的氢离子浓度为 。
 (4)D、E和钡三种元素构成的某化合物的晶胞结构如右图所示,该化合物的化学式为 。纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
(4)D、E和钡三种元素构成的某化合物的晶胞结构如右图所示,该化合物的化学式为 。纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
向溶液中分别通入足量的相应气体后,下列各组离子还能大量存在的是( )
A.氯气:K+、Na+、SiO32-、NO3- B.二氧化硫:Na+、NH4+、SO32-、Cl-
C.硫化氢:H+、K+、MnO4-、SO42- D.氨气: K+、Na+、AlO2-、CO32-
常压下羰基化法精炼镍的原理为: Ni(s)+4CO(g) ![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断不正确的是( )
A. 该反应达到平衡时,v分解[Ni(CO)4]=4v消耗(CO)
B. 第一阶段应选择稍高于42.2℃的反应温度
C. 第二阶段,230℃时Ni(CO)4分解率较高
D. 其他条件不变,增加c(CO),平衡向正向移动,反应的平衡常数不变
向一定量的Fe,FeO,Fe2O3,Fe3O4的混合物中,加入150 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,并放出标准状况下NO气体2.24 L,往所得溶液中加KSCN溶液,无红色出现。若用足量的氢气在加热条件下还原相同质量的该混合物,所得铁的物质的量可能为( )
A.无法确定 B.0.6 mol C.0.5 mol D.0.25 mol
下列实验可以达到预期实验目的的是( )
| 实验 | 实验内容 | 实验目的 |
| A | 将木炭与浓硫酸共热,得到的气体通入 澄清石灰水 | 检验木炭的氧化产物是 CO2 |
| B | 加入足量铁屑,充分反应后,过滤 | 除去 FeCl2 溶液中的少量 FeCl3 |
| C | 将 1moLCuSO4·5H2O 溶解在 1L 水中 | 制备 1moL/L 的 CuSO4 溶液 |
| D | 饱和氯化铁溶液中滴加氨水 | 制备 Fe(OH)3 胶体 |
一定温度下,下列溶液的离子浓度关系正确的是
A.pH=5的H2S溶液中,c(H+) = c(HS—) = 1×10—5mol·L—1
B.pH = a的氨水溶液,稀释10倍后,其pH =b,则a = b + 1
C.pH =2的H2C2O4溶液与pH =12的NaOH溶液任意比例混合:c(Na+)+ c(H+) = c(OH—) + c(HC2O4—)
D.pH相同的①CH3COONa,②NaHCO3,③NaClO三种溶液的c(Na+):①>②>③
铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是( )
A. NaCl ![]() B. KNO3
B. KNO3 ![]() C. FeCl2
C. FeCl2 ![]() D. Fe2(SO4)3
D. Fe2(SO4)3
碳、及其化合物在生产中有重要应用。
(1)设反应①Fe(s) + CO2(g)![]() FeO(s) +CO(g) △H=Q1平衡常数为K1
FeO(s) +CO(g) △H=Q1平衡常数为K1
②Fe(s) +H2O(g)![]() FeO(s) + H2(g) △H= Q2 平衡常数为K2
FeO(s) + H2(g) △H= Q2 平衡常数为K2
不同温度下,K1、K2 的值如下表
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
现有反应③H2(g) +CO2(g)![]() cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
(2)已知CO2 催化加氢合成乙醇的反应原理为:
2CO2(g) +6H2(g)![]() C2H5OH(g) + 3H2O( g) △H<O
C2H5OH(g) + 3H2O( g) △H<O

①图1、图2 分别是CO2 的平衡转化率随压强及温度的变化关系,已知m 为起始时的投料比,即m=n(H2)/n(CO2),图1中投料比相同,温度从高到低的顺序为__________,图2 中m1、m2、m3从大到小的顺序为_________。
②图3 表示在总压为5MPa的恒压条件下,且m=3 时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质为_________(填化学式),T4温度时,该反应的平衡常数Kp=___________。(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)
下列过程中都涉及到饱和食盐水,其中氯离子被氧化的是
A.氯碱工业 B.侯氏制碱 C.制取乙炔 D.除去Cl2中的HCl
今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是( )
A 1:1:1 B 3:2:1 C 3:2:3 D 1:1:3
已知:E是石油裂解气的主要成份,分子式为C2H4,D是一种具有香味的物质,各物质间的转化如下图所示(有的反应条件和产物已略去)。

请回答下列问题:
(1)化合物B的结构简式为
(2)反应①的反应类型
(3)写出反应②的化学方程式
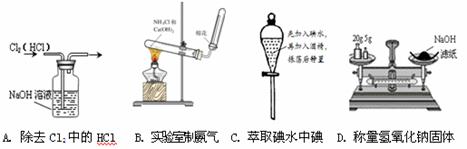
下列有关实验操作正确的是
醋酸可以通过分子间氢键双聚。在一定温度下,将一定质量的冰醋酸加水稀释的过程中,溶液导电性的变化如右下图所示。下列有关说法正确的是
 A.a、b、c三点溶液的pH:a>b>c
A.a、b、c三点溶液的pH:a>b>c
B.若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小
C.a、b、c三点溶液用1 mol/L的NaOH溶液中和,消耗NaOH溶液的体积a>b>c
D.若在O点醋酸双聚成八元环。则其结构式为:

化学与生产、生活、社会密切相关,下列说法不正确的是
A. 钢铁在潮湿额定空气中放置,易发生电化学腐蚀而生锈
B. SO2、NO、NO2都是大气污染物,它们在空气中都能稳定存在
C. 水泥、玻璃、陶瓷是生产生活中用量最大的无机非金属材料
D. 用NH4Cl浓溶液除铁锈,因为NH4Cl水解显酸性
绿矾(FeSO4·7H2O)广泛用于工农业生产。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生成纯净绿矾的一种方法:

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)操作II中,通入硫化氢至饱和的目的是_________________________;在溶液中用硫酸酸化至pH=2的目的是_________________________;
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是______________;用冰水的原因是_________________________;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为_______________;
(4)25℃时,将FeSO4·7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=________mol/L。[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4·7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示:
①在100℃时M的化学式为______________________;
②FeSO4·7H2O晶体中有______种不同结合力的水分子。

水的电离平衡曲线如图所示,下列说法不正确的是( )
A.图中四点KW间的关系:A=D<C<B
 B.若从A点到C点,可采用温度不变在水中加少量CH3COONa固体
B.若从A点到C点,可采用温度不变在水中加少量CH3COONa固体
C.若从A点到D点,可采用温度不变在水中加少量酸
D.若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性
丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如图24所示:

已知:
(1)A的名称是_______;E到F的反应类型是___________。
(2)试剂a是________,F中官能团名称是_______。
(3)E的含苯环同分异构体共有______种(不含E)。
(4)J是一种酯,分子中除苯环外还含有一个五元环,J的结构简式为__________-。H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为________。
(5)利用题中信息写出以乙醛和苯为原料,合成 的路线流程图(其它试剂自选)。____________
的路线流程图(其它试剂自选)。____________
下列有机物分子中,在核磁共振氢谱中只给出一种峰(信号)的是( )
A.CH30H B.C(CH3)4 C.CH3COOH D.CH3COOCH3
化学在资源利用、 环境保护等与社会可持续发展密切相关的领域发挥着积极作用。下列做法与社会可持续发展理念相违背的是
A. 改进汽车尾气净化技术,减少大气污染物的排放 B. 开发利用可再生能源,减少化石燃料的使用
C. 研发可降解高分子材料,减少“白色污染” D. 过度开采矿物资源,促进地方经济发展
甲、乙两人分别用不同的方法配制100ml 3.6mol/L的稀硫酸。
(1)甲:量取20 ml 18 mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地 向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
① 实验所用的玻璃仪器除烧杯和胶头滴管外,还有的玻璃仪器有 , , ;
(2)乙:用100 ml 量筒量取20 ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处 , , 。
- (本题12分)设函数的定义域为A, 函数 (其中)的定义域为B. (1) 求集合A和B; (2) 设全集,当a=
- 英国资产阶级代议制的主要特点是 A.议会与责任制内阁为核心 B.君主制、贵族制与民主制三结合 C.采取
- +2 写出以下符号中数字“2”的意义: (1)2H__________; (2)H2________________
- 4y2﹣x2﹣y+x2﹣4y2,其中x=﹣28,y=18.
- 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述错误的是
- The congressman will his speech tomorrow. A.deliver B.tell t
- 此题要求改正所给短文中的错误。对标有题号的每一行作出判断:如无错误,在该行右边横 线上画出一个钩(√);如果有错误(每行
- 设方程(q为参数)表示的曲线为C,求在曲线C上到原点O距离最小的点P的坐标.
- 甲、乙、丙三种固体物质的溶解度曲线如右图所示,下列有关说法中正确的是
- 下列属于人类社会特有的文化现象的是①2010年上海世博会吉祥物“海宝” ②“南海一号”的打捞工作 ③我
- 如图,在正方形ABCD中,AB=3cm,动点M自A点出发沿AB方向以每秒1cm的速度运动,同时动点N自D点出发沿折线DC
- 厨房中有许多化学物质,小芳列出了以下几种,其中属于纯净物的是 A.黄酒 B.加碘食盐 C
- 人们按方位把亚洲分为6个地区,其中我国位于哪个地区( ) A.南亚 B.西亚 C.东
- 下列各句,没有语病、句意明确的一句是 ( ) A.厂长严肃地说:“我们应该节约用水,尽量减少不必要的浪费。”
- 如图,在Rt△ABC中,∠C=90°,AB= 5,AC= 4,则cosA=
- 下列句子中加点的成语,使用恰当的一句是 A.两次攀登世界最高峰的失败没有使他灰心,经过三年的精心准备,他终于功败垂
- 下列词语中加点的字的读音,全都不相同的一组是() A、拾掇 辍学 啜泣 缀字成文 B、湍急 祥瑞 颛臾 惴惴不安 C、伯
- NM﹣3和D﹣58是正处于临床试验阶段的小分子抗癌药物,结构如下:关于NM﹣3和D﹣58的叙述,错误的是() A.都能与
- 若(logax)=x(a>0,a≠1),则x的值等于( )A.1或a B.1或
- 土壤动物具有趋暗、趋湿、避高温的习性,下图A、B、C、D4种土壤微型节肢动物分离收集装置中,最合理的是( )



