高三化学试题
化学与生活及社会发展息息相关,下列有关说法不正确的是( )
A.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.向豆浆中加入盐卤可制作豆腐,利用了胶体聚沉的性质
下列离子或分子能够在指定的分散系中大量共存的是
A.空气中:CO2、NO、N2、NH3
B.明矾溶液中:H+、Mg2+、Na+、Cl-
C.过量铁与稀硝酸反应后的溶液中:H+、Cl-、I-、Na+
D.常温下,水电离出的c(H+)=1×10-12 mol/L的溶液中:NH4+、Na+、Cl-、CO32-
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出12种元素的X的数值:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | N |
| X的数值 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系______________________________。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某有机物结构简式为: ,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
(5) 预测元素周期表中,X值最小的元素位置________(放射性元素除外)。
龙葵醛( )是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。以下是以苯为原料生成龙葵醛的一种合成路线(部分反应条件及副产物已略去):
)是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。以下是以苯为原料生成龙葵醛的一种合成路线(部分反应条件及副产物已略去):
![]()
![]()

![]()

![]()

![]()
龙葵醛![]()

![]()

(1)龙葵醛的分子式为 ,其中含氧官能团的名称是 ;
A物质得到的1H-NMR谱中有 个吸收峰,B的结构简式可能为 。
(2)反应③的反应类型为 ,反应⑤的反应条件为 。
(3)反应⑥的化学方程式为 。
(4)龙葵醛具有多种同分异构体,其中某些物质有下列特征:a.其水溶液遇FeCl3溶液呈紫色;b.苯环上的一溴代物有两种;c.分子中没有甲基。写出符合上述条件的物质可能的结构简式(只写两种):
 下列图示与对应的叙述相符的是( )
下列图示与对应的叙述相符的是( )
甲 乙 丙 丁
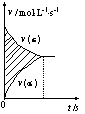
A.图甲中阴影部分的面积表示v(正)与v (逆)的差值
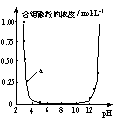
B.图乙表示溶液中含铝微粒浓度随pH变化曲线,a点所示溶液中存在大量AlO![]()
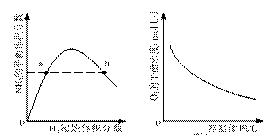
C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
D.图丁表示同一温度下,在不同容积的容器中进行反应2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 ![]() 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
不正确的操作顺序是
A.③②①⑤④ B.②③①⑤④
C.③①②⑤④ D.①②③⑤④
Fe(OH)3胶体和MgCl2溶液共同具备的性质是 ( )
A.两者均有丁达尔效应 B.两者均能透过半透膜
C.加入盐酸先沉淀,随后溶解 D.分散质粒子可通过滤纸
资料表明,MnO2和Fe3+对H2O2制备O2均具有催化作用。某课外小组同学在实验室进行了验证试验并研究了H2O2其他性质。回答下列问题:
(1)现有三支分别盛有2 mL10% H2O2溶液的试管,甲同学在第一、第二支试管中分别加入MnO2和少量FeCl3溶液,发现均有大量气泡生成,向第三支试管中加入少量的盐酸溶液并观察现象,其目的是________。
(2)该同学查阅相关资料,获得催化机理如下图所示:

①图1中微粒M1是_______(填化学式)。
②图2中若M4为Mn2+,则反应Ⅲ的离子方程式为_____________。
(3)乙同学在试管中加入2 ml. 3%的H2O2溶液,0.5mL乙醚,l mL1 mol/LH2SO4溶液和3~4滴0.5mol/L的K2Cr2O7溶液,发现上层有机相为蓝色(CrO5的乙醚溶液),下层水相为无色。
①乙醚除作为CrO5的稳定剂外,另一作用是____________。
②一段时间后蓝色褪去,并产生大量的气泡同时水相中溶液变为绿色(含Cr3+),褪色反应的离子方程式为________________。
如图是A分子的球棍模型和B分子的比例模型,回答下列问题:

(1)A和B的关系是_____。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式___________。
(3)写出B分子和金属钠反应的化学方程式_____________________。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是____________。
某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
A.肯定不含I- B.肯定不含SO42-
C.肯定含有SO32- D.肯定含有NH4+
某无色溶滚中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种.为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,.无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448ml气体.下列关于原溶液的说法正确的是
A.肯定存在NH4+、Cl﹣、Br﹣
B.SO42﹣、SO32﹣至少含有一种
C.是否存在Na+需要通过焰色反应来确定
D.肯定不存在Ba2+、Cu2+、SO32﹣、CO32﹣
将高温水蒸气通到硫氰化钾的表面,会发生反应:4KSCN + 9H2O(g) → K2CO3 + K2S + 3CO2 + 3H2S + 4NH3完成下列填空:
(1)上述反应所涉及的各元素中,离子半径最大的是_____________(填离子符号);属于第二周期元素的非金属性由强到弱的顺序为_________________。
(2)上述反应所涉及的各物质中,属于非电解质的是_________________。
(3)写出CO2的电子式____________,其熔沸点低的原因是___________________________。
(4)已知物质的量浓度均为0.10 mol/L的K2CO3和K2S溶液pH如下:
| 溶液 | K2CO3 | K2S |
| pH | 11.6 | 12.5 |
K2CO3水溶液呈碱性的原因是______________________________(用离子方程式表示)。从表中数据可知,K2CO3溶液中c(CO32-)_______K2S溶液中的c(S2—)(填“>”“<”或“=”)。
(5)K2S接触潮湿银器表面,会出现黑色斑点(Ag2S),其原理如下:____K2S + ____Ag + _____O2 + _____H2O → _____Ag2S + _____KOH
①配平上述反应________________。
②每消耗标准状况下224 mL O2,转移电子数目为_____________。
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8g O2含有4NA个电子
B.1L 0.1mol·L-1的氨水中有NA个NH4+
C.标准状况下,22.4L四氯化碳含有NA个分子
D.1molNa被完全氧化生成Na2O2,失去2NA电子
.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过H2O。以下叙述正确的是( )
A.硫酸盐都易溶于水
B.检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品![]() 粉碎
粉碎![]() 加水溶解
加水溶解![]() 过滤
过滤![]() 向滤液中滴加KSCN溶液
向滤液中滴加KSCN溶液
C.分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3∶2∶3
D.明矾含有结晶水,是混合物
N2 (g)与H2 (g)在铁催化剂表面经历如下过程生成NH3(g): 下列说法正确的是

A.I中破坏的均为极性键 B. IV中NH3与H的总键能大于NH3中总键能
C. n、m、IV均为放热过程 D·N2 (g)+3H2 (g)![]() NH3 (g) △H>0
NH3 (g) △H>0
利用废铁屑(主要成分为Fe,还含有C,S,P等)制取高效净水剂K2FeO4流程如图:

下列说法不正确的是
A.废铁屑在酸溶前可用热的纯碱溶液去油污
B. 步骤②是将Fe2+转化为Fe(OH)3
C. 步骤③中发生的反应的离子方程式为 2Fe(OH)3+3ClO-==2FeO42-+3Cl-+4H++H2O
D.步骤④中反应能发生的原因是在相同条件下,K2FeO4的溶解度小于Na2FeO4
[化学——选修3]物质结构:(15分)
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1)C60分子中每个原子接2个单键和1个双键,它与F2发生加成反应,其加成产物的分子式为_____;
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是 。
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有____。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C—C<石墨中C—C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为_______,B原子与N原子之间共价键与配价键的数目比为_____,一个晶胞中N 原子数目为_______。

(5)炭与孔![]() 雀石共热可以得到金属铜,基态铜原子的电子排布式为_______,铜采用_____堆积,则铜的晶体中Cu 原子的配位数为________。已知铜单质的晶体密度为pg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的半径为________。
雀石共热可以得到金属铜,基态铜原子的电子排布式为_______,铜采用_____堆积,则铜的晶体中Cu 原子的配位数为________。已知铜单质的晶体密度为pg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的半径为________。
实验室需配制一种溶液,除水电离出的离子外还含有五种离子,且在该溶液中这五种离子的物
质的量浓度均为1 mol·L-1,下面四个选项中,能达到此要求的是( )
A.Al3+、K+、SO、Cl-、HCO B.Fe2+、H+、Br-、NO、Cl-
C.Na+、K+、SO、NO、Cl- D.Al3+、Na+、Cl-、SO、NO
下列关于![]() 和
和![]() 的说法正确的是
的说法正确的是
A.两种物质均含有相同的含氧官能团
B.两种物质互为同分异构体,具有相同的化学性质![]()
C.两种物质均可以发生加成反应、取代反应和氧化反应
D.两种物质均有酸性,在水溶液中均能电离出氢离子
将足量BaCO3分别加入:
①30 mL水②10 mL 0.2 mol·L-1 Na2CO3溶液
③50 mL 0.01 mol·L-1氯化钡溶液④100 mL 0.01 mol·L-1盐酸中溶解至溶液饱和。各溶液中Ba2+的浓度由大到小的顺序为( )
A.①②③④ B. ④③①②
C. ③④①② D.②①④③
- 沈浩,安徽小岗村党委书记,他以振兴小岗为己任,敢于突破,勇于创新,大力弘扬小岗村精神,为加快小岗村发展做出了突出贡献。据
- 下列计算正确的是() A. a3•a2=a6 B. (﹣a3)2=a6 C. D.
- 下图是兴奋在神经元之间传递的示意图,关于此图的描述错误的是A.神经递质是从①处释放的
- Great efforts to increase grain production if food sho
- 乙苯()的二氯代物共有() A.15种 B.12种 C.9
- 直角坐标系中, 是原点; ,动点P在直线 上运动,若从动点P向Q点的轨迹引切线,则所引切线长的最小值是 A.
- 已知直线AC的中点为B点,物体沿AC做变速直线运动,在AB段的平均速度为4 m/s,在BC段的平均速度为6 m/s,则它
- 材料 1979年,中央对21个省、自治区、直辖市实行“收支挂钩、超收分成”的办法,地方超收分成比例在50%以下的按照5
- 如图所示,A、B、C、D是匀强电场中一正方形的四个顶点,已知A、B、C三点的电势分别为φA=15 V,φB=3 V,φC
- 下列物质中,属于氧化物的是() A.石灰水 B.空气 C.生铁 D.干冰
- 下列说法正确的是 ( ) A.-1的相反数为-1 B.-1的倒数为1 C.-1的绝对值为1 D.(-1=
- 读某地正午太阳高度角年变化折线图(图3),完成10-11题。 10.根据该地正午太阳高度角年变化的规律,判断该地点可能位
- 如图所示,一端封闭的两条平行光滑长导轨相距L,距左端L处的右侧一段弯成半径为的四分之一圆弧,圆弧导轨的左、右两段处于高度
- 下列有关高中生物实验中实验材料、试剂的使用及实验现象描述正确的是( ) A.用甲基绿染液单独对洋葱鳞片叶内表皮染色,观
- 下列关于单倍体的叙述中,不正确的是 ( ) A.单倍体的体细胞中只有一个染色体组 B.花粉粒发育成的花粉植株是单倍体
- 若a是最大的负整数,b是绝对值最小的数,则a-b= .
- 中国传统文化对人类文明贡献巨大,《本草纲目》中有如下记载:“(火药)乃焰消(KNO3)、硫黄、杉木炭所合,以为烽燧铳机诸
- 传感器是一种采集信息的重要器件.如图4-4-6所示是一种测定压力的电容式传感器.当待测压力F作用于可动膜片电极时,可使膜
- Mother is too busy to wash clothes for.I have to wash them
- 人体内静脉血变为动脉血,是由血液流经下列哪一部分毛细血管实现的( )A.鼻腔黏膜毛细血管 B.



