高三化学试题
在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )

A.反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间不能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
实验室制备氨基甲酸铵(NH2COONH4)的反应如下:
2NH3(g)+CO2(g) ![]() NH2COONH4(s)
NH2COONH4(s)
该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
(1)该反应在一定条件下能够自发进行,则反应的ΔH ▲ 0。(填大于、小于或等于)
(2)写出生成碳酸氢铵的化学方程式 ▲ 。
(3)实验步骤如下:
步骤1:按图所示组装仪器,检查装置气密性。
步骤2:在相应仪器中装入药品,其中在三颈烧瓶中加入氢氧化钠固体,恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品
……
①干燥管中盛放的药品是 ▲ 。
②对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有 ▲ , ▲ 。
③以恒压滴液漏斗代替分液漏斗的目的是 ▲ 。
④反应后期CO2气流量下降时,可采取的相应措施是 ▲ 。
(4)该实验装置可能面临的安全问题是 ▲ 。

咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(Ka约为10−6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如下图所示。

索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:

1.实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________,圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒______________。
2.提取过程不可选用明火直接加热,原因是______________,与常规的萃取相比,采用索氏提取器的优点是______________。
3.提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂的优点是______________。“蒸发浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________(填标号)。
A.直形冷凝管 B.球形冷凝管 C.接收瓶 D.烧杯
4.浓缩液加生石灰的作用是中和____________和吸收__________
5.可采用如上图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是______________。
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为11;Y、Z在同一
周期;Z原子最外层电子数是X原子内层电子数的2倍,也是Y原子最外层电子数的2倍。下列说
法中,正确的是
A.离子半径:Y>X B.气态氢化物的稳定性:Z>X
C.Y的氧化物中含有离子键 D.Z的氧化物对应的水化物是弱碱
 |
有机物F( )是合成某种药物的中间体,它的一种合成路线如下:
 |
回答下列问题:
(1)A的结构简式为__________________,分子中处于同一平面的原子最多有_____个。
(2)E中官能团名称是__________,①~④中属于加成反应的是___________(填序号)。
(3)反应③的化学方程式为____________________________________________________。
(4)反应⑤的生成物有两种,除了F以外,另一种生成物的名称是__________________。
(5)满足下列条件的D的同分异构体有________种。
①能与FeCl3溶液发生显色反应 ②能发生银镜反应 ③分子中有1个甲基
(6)仿照E的合成路线,设计一种由![]() 合成
合成![]() 的合成路线
的合成路线
________________________________________________________________________。
下列关于古籍中的记载说法不正确的是( )
A.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
B.《吕氏春秋•别类编》中“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性
C.《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
D.《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体经过如图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为

A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D.NO、CO2、N2
.下图曲线a表示反应X(g)+Y(g) +N(s) ![]() Z(g)+M(g) △H<0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g) △H<0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
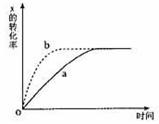
A.升高温度 B.加大N的投入量
C.缩小体积 D.加大X的投入量
已知下列反应的能量变化示意图如下:
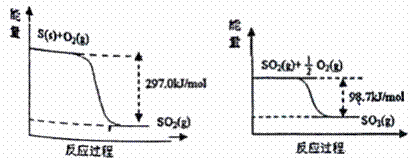
下列有关说法正确的是
A. l mol S(g)与O2(g)完全反应生成SO2(g) ,反应放出的热量<297.0 kJ/mol
B. 在相同条件下,SO3(g)比SO2(g)稳定
C. 1 mol SO2(g)和1/2mol O2(g)生成1mol SO3(g)吸收98.7 kJ/mol
D. S(s)与O2(g)反应生成SO3(g)的热化学方程式S(s)+3/2O2(g)![]() SO3(g) △H=- 395.7 kJ/mol
SO3(g) △H=- 395.7 kJ/mol
下列物质溶于水后,溶液能导电,但属于非电解质的是
A.SO2 B.CH3COOH C.CaO D.Na
钼酸钠晶体(Na2MoO4·2H2O)常用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:

回答下列问题:
(1)提高焙烧效率的方法有_______________________。(写一种)
(2)“焙烧”时MoS2转化为MoO3,该反应过程的化学方程式为____________________,氧化产物是__________________
(3)“碱浸”时生成CO2的电子式为______________,碱浸”时含钼化合物发生的主要反应的离子方程式为____________________________。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为____________________。
(5)钼精矿在酸性条件下,加入NaNO3溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为____________________________________________________________。
为了除去固体KCl中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的KCl,可将固体溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:①过滤 ②加过量KOH溶液 ③加适量盐酸 ④加过量K2CO3溶液 ⑤加过量BaCl2溶液( )
A.②①⑤④③B. ④①②⑤③
C. ②⑤④①③D. ①④②⑤③
某无色溶液中,已知含有H+、Mg2+、Al3+等阳离子,逐滴加入NaOH(溶液),则消耗NaOH(溶液)体积(x轴)和生成沉淀量(y轴)之间的函数关系,可用下图表示,则下列图中正确的是( )

NA代表阿伏加德罗常数的值。下列叙述正确的是
A.60g丙醇中存在的共价键总数为10NA
B.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C.钠在空气中燃烧可生成多种氧化物。23g钠充分燃烧时转移电子数为1NA
D.235g核互![]() U发生裂变反应:
U发生裂变反应:![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() U+10
U+10![]() n,净产生的中子
n,净产生的中子
(![]() n)数为10NA
n)数为10NA
汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )。

A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液显色
C. 1 mol该物质与溴水反应,最多消耗1 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
镁及其化合物在现代工业、国防建设中有着广泛的应用。回答下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的_____,还生成少量的______(填化学式)。
(2) CH3 MgCl是一种重要的有机合成剂,其中镁的化合价为_______ ,CH3 MgCl水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:______________________________________________。
(3) Mg(OH)2是常用的阻燃材料。以白云石(CaCO3、MgCO3,不考虑杂质)为原料制备Mg(OH)2和CaCO3工艺流程如下:

①溶解度:Ca(OH)2 _______ (填“>”或“<”)Mg(OH)2。
②“煅烧”时称取27.6 g白云石,高温加热到质量不再变化,收集到的CO2为6.72 L(标准状况下),若工艺中不考虑Ca、Mg损失,则Mg( OH)2和CaCO3的质量分别为_________、____________。
下列说法正确的是 ( )
A.液氯是单质,HD是化合物,NO2是酸性氧化物
B.汽油、漂白粉、水玻璃、王水均为混合物
C.煤的气化、液化是物理变化,煤的干馏是化学变化
D.NH3 、NH3·H2O均为电解质,且都为纯净物
下列有关物质的性质类比正确的是
A.已知![]() ,则
,则![]()
B.Fe能与CuSO4溶液反应,可知Al与CuSO4溶液也能反应
C.CaSO3与稀盐酸反应生成SO2,可知CaSO3与稀硝酸反应也生成SO2
D.已知H2O2能氧化I-,可知H2O2也能氧化Cl-
化学与人类生活密切相关,下列说法不正确的是( )
A.静电除尘、血液渗析均与胶体的性质有关
B.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
C.聚乙烯一种热塑性树脂,聚乙烯塑料制品可用于食品的包装
D.高铁酸钾(K2FeO4)是一种高效、多功能水处理剂,既能消毒杀菌又能净水
(1)下图所示为按树状分类法对一组物质进行的分类。请填写下列标注。

(2)中国的“四大发明”之一——黑火药,在发生爆炸时,发生如下的反应:
2KNO3 + C+ S=K2S + 2NO2↑+ CO2↑。被氧化的元素是 ,氧化剂是 。
(3)氢氧化铁胶体分散质粒子大小在 之间。
(4)某气体与标准状况下同体积氧气的质量之比为2:1,则该气体的摩尔质量为 ,此气体在标准状况下的密度是 g/L。
(5)在2g质量分数为28%的KOH水溶液中,K+ 离子数与H2O分子数之比是_________。
- ......
- FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是
- 细胞相对表面积、细胞对外物质交换速率和细胞新陈代谢强度之间关系的叙述中正确的是( ) A.细胞的相对表面积越大,物
- 设则的大小关系为( ) A. B.C.
- Is thereanything I can help you? A. that
- 十一届全国人大三次会议审查通过了《关于2009年中央和地方预算执行情况与2010年中央和地方预算草案的报告》。作为“国家
- 14.某温度下向100 g澄清的饱和石灰水中加入5.6 g生石灰,充分反应后恢复到原来的温度。下列叙述正确的是()A.沉
- 2013年6月20日,小华同学通过全国太空授课得知“神舟”十号飞船在圆轨道上运转一圈的时间为90分钟,由此他将“神舟”十
- 在,角所对的边分别为,向量,且。 (1)求的值;(2)若,求的值。
- (历史选修4:中外历史人物评说) 材料 张之洞(1837—1909),洋务派代表人物之一。其任封覆大支的时间内,直接指
- 解不等式组
- 经济的繁荣与发展有利于和平力量的壮大,贫困落后则是国际形势动荡不安的一个重要因素。有效地制止战争,维护和平与稳定的国际环
- 下列溶液可以盛放在玻璃试剂瓶中,但不能用磨口玻璃塞的是( ) A.硅酸钠溶液
- 已知y是x的反比例函数,当x > 0时,y随x的增大而减小.请写出一个满足以上条件的函数表达式 .
- 下列说法中不正确的是 A.大米主要成分是淀粉,淀粉遇碘化钾溶液变蓝色B.鸡蛋清中加入饱和硫酸铵溶液,有白色沉淀 C.油脂
- 试比较a+b与a的大小.
- 看到小溪,有人赞美它飞珠溅玉,有人嘲笑它浮浅唠叨;看到江河,有人欣赏它一泻千里,有人害怕它奔腾咆哮;一滴一滴的水,有人不
- 已知数列是以3为公差的等差数列,是其前n项和,若是数列中的唯一最小项,则数列的首项的取值范围是
- If you run ____ two hares you will catch neither. A.into
- —Rather than ___ on a crowded bus, he always prefers ___ a b



