高中 化学
 B . 乙烯的球棍模型:
B . 乙烯的球棍模型:  D . 溴乙烷的官能团:-Br
D . 溴乙烷的官能团:-Br


 D .
D .  B . 比较两种物质的热稳定性
B . 比较两种物质的热稳定性 C . 实验室制取NH3
C . 实验室制取NH3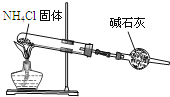 D . 分离沸点不同且互溶的液体混合物
D . 分离沸点不同且互溶的液体混合物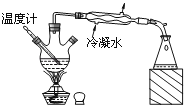
-
(1) ①写出MgO的名称;
②写出乙炔的结构式。
-
(2) 写出NaHCO3受热分解的化学方程式。
-
(3) 写出Cl2与NaOH溶液反应的离子方程式 。
-
(4) 海带中提取碘的过程中,将I-氧化生成I2时,若加入过量的氯水,则Cl2将I2氧化生成HIO3 , 同时还有一种强酸生成,写出该反应的化学方程式。
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
主要化合价 | +2 | +3 | +2 | +6、﹣2 | ﹣2 |
 和
和  两种溶液
D . 取用金属钠时,多余的钠应该放回原试剂瓶中
两种溶液
D . 取用金属钠时,多余的钠应该放回原试剂瓶中
-
(1) 基态氮原子的价电子排布式为。
-
(2) 14g氮气分子中原子轨道以“头碰头”方式形成的共价键数目为,以“肩并肩”方式形成的共价键数目为。
-
(3) C、N、O三种元素按第一电离能从大到小的排列顺序为。已知氧的第一电离能为1369kJ·mol-1、第二电离能为3512kJ·mol-1、第三电离能为5495kJ·mol-1 , 其第二电离能增幅较大的原因是。
-
(4) 某含氨配合物CrCl3·6NH3的化学键类型有配位键、极性共价键和。CrCl3·6NH3有三种异构体,按络离子式量增大的顺序分别是[Cr(NH3)6]Cl3、、[Cr(NH3)4Cl2]Cl·2NH3。
-
(5) NH4N3是高能量度材料,其晶胞如下图所示。N3-是直线型结构,N3-中氮原子的杂化类型是。在VSEPR模型中NH4+的几何构型名称为。

-
(6) 已知NH4N3的晶胞参数为anm和0.5anm,阿伏加德罗常数的值为NA , 则NH4N3的密度为g·cm-3。

某同学欲用托盘天平称量21.5g氯化钠(5g以下用游码),他把氯化钠放在右盘,砝码放在左盘,当天平两边平衡时,他所称取的氯化钠的质量实际是( )
A.16.5g B.18.5g C.20.5g D.23.5g
实验室为监测空气中汞蒸气的含量;往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI+Hg→Cu2HgI4+2Cu
(1)上述反应产物Cu2HgI4中,Cu元素显 价。
(2)以上反应中的氧化剂为 ,当有1 mol CuI参与反应时,转移电子 mol。
(3)CuI可由Cu2+与I-直接反应制得,请配平下列反应的离子方程式。
Cu2+ + I-→ CuI+ I3-
由铜、锌和稀盐酸组成的原电池中,铜是 极,发生 反应,电极反应式是 ;锌是 极,发生 反应,电极反应式是 。
常温下,用 0.10 mol·L-1 NaOH 溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示:
 | |||
 |
图1 图2
则滴定HC1溶液的曲线是 _▲ (填“图1”或“图2”),说明判断依据 ▲ 。a与b的关系是:a _▲ b(填“>”、“<”或“=”);E点对应离子浓度由大到小的顺序为 _▲ ;
利用下列实验装置能达到相应实验目的的是
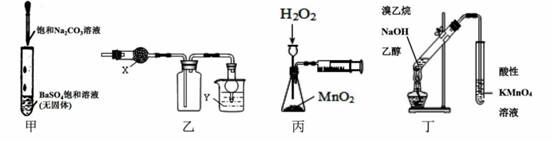
A.甲可用于研究沉淀的转化,可比较出Ksp(BaSO4)>Ksp (BaCO3)
B.乙中X为无水CaCI2,Y为NaOH溶液时,该装置可用于SO2的收集
C.丙装置可定量测定H2O2的分解速率
D.丁可用于证明实验中生成了乙烯
- 下面坐标是某绿色植物在光合作用最适温度下(未达到呼吸作用最适温度),测得植株氧气释放量与光照强度的关系,对其不恰当的解释
- ,则实数在数轴上对应的点的大致位置是( ) A. B.
- 2009年,影片《建国大业》热播,一个个动人的场面,一句句经典的台词,一个个熟知的人物让人久久不能平静。电影中出现了与蒋
- 文言文阅读 梁大夫有宋就者,尝为边县令,与楚邻界。梁之边亭,与楚之边亭,皆种瓜,各有数。梁之边亭人,劬①力数灌其瓜,瓜美
- 某生物科技小组对某农田生态系统进行实地调查,请你运用所学知识协助解决一些实际问题。 (1)该生态系统的结构包括_____
- 下列各项中,每对词语加点字读音完全不同的一项是( ) A.吞噬(shì) 讣告(pǔ) 轧路机(yà)
- 在场强为E=100V/m的竖直向下匀强电场中有一块水平放置的足够大的接地金属板,在金属板的正上方,高为h=0.8m处有一
- 分类归纳是学好化学必要的方法之一,下列物质的分类正确的是
- 阅读下面的文字,完成16―18题。雨夜的红灯笼林决定下来了,要走。林望了望那两间又低又矮的教室,心中便一片怆然。夕阳斜下
- 发源于南亚的宗教是() A. 基督教、伊斯兰教B. 伊斯兰教、佛教 C. 佛教、基督教D. 佛教、印度教
- TheFitting-in of Suzy Khan The first time I sawSuzy Khan,
- Our teacher asks us to clean the floor in the morning as our
- It was at twelve o’clock ___ we finally arrived at the villa
- 如图所示是用厚刻度尺测量木块的长度,正确的测量图是: ( )
- 农民将人粪尿收集起来,加水后浇在菜地里,能加快菜苗的生长。请问正常尿液的成分中不含下列何种物质( )A.尿素
- 氨水是氨气(化学式为NH3)溶于水后形成的,是一种常见的实验药品,它能使无色的酚酞溶液变成红色。 (1)氨气可以用氮气和
- 某同学在“观察人的口腔上皮细胞”实验中,为观察到更清晰的物像,进行了系列操作。下列有关操作与目的对应关系中,正确的是 A
- (14分)如图,在四棱锥中,, ,BC⊥AB,CD⊥AD,BC=CD=PA=a, (Ⅰ)求证:
- 根据实验室中测定硫酸铜晶体(CuS04·XH20)结晶水含量的实验,填写下列空白:(1) 从下列仪器选出无需用到的仪器是
- (6分)氮气其化合物是中学化学的基础知识,请你回答下列含氮化合物的有关问题。(1)汽车尾气中含有氮氧化物,严重污染大气。



