高三化学试题
下列有关实验的说法错误的是
A.向品红溶液中通入气体X,品红溶液褪色,则气体X可能是Cl2
B.CO2中含少量SO2,可将该混合气体通入足量饱和NaHCO3溶液中除去SO2
C.用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色,说明该食盐试样中不含KIO3
D.向NaHCO3溶液中滴加酚酞试液,加热时溶液由淡红色变为红色,冷却后溶液由红色变为淡红色,说明HCO3- 在水溶液中存在水解平衡
电力工业所需的钢制构件在镀锌前需要经过酸洗,其基本原理是用盐酸除去其表面的Fe2O3·2H2O及FeO等杂质。回收废酸同时生产含铁产品的流程如下:

已知:i.酸洗钢制构件后得到废酸的主要成分如下表所示。

ii pH <4时,Fe2+不易被氧气氧化。
(1)酸洗钢制构件时发生反应的离子方程式:2H++ FeO=Fe2++H2O、_______________。
(2)过程II中,发生的主要反应:FeCl2(s)十H2SO4(aq) ![]() FeSO4(s)+2HCl( aq)。
FeSO4(s)+2HCl( aq)。
①加入过量H2SO4的作用是_____________(至少写出两点)。
②用化学平衡原理解释鼓入空气的目的:_____________。
(3)过程III中,FeSO4隔绝空气焙烧得到的尾气中含有两种可用于生产硫酸的氧化物,此过程发生反应的化学方程式是_________________。
(4)过程IV发生反应的离子方程式是____________________。
(5)过程V:阴离子交换树脂可将FeCl4-选择性吸附分离,其过程可表示为ROH +X- ![]() RX +OH-。当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4-
RX +OH-。当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4- ![]() Fe3+ +4C1-。
Fe3+ +4C1-。
①吸附后溶液酸性下降的原因是_______________。
②洗脱液中主要含有的溶质是______________。
某有机物的结构简式如图所示,下列有关该有机物的说法不正确的是

A. 苯环上的一氯代物有3种
B. 含有2种官能团
C. 分子中的所有碳原子一定共面
D. 能发生氧化反应、取代反应、还原反应
.有人欲配制含有下列四种离子的溶液,其中能配制成功的是( )
A.Ca2+、H+、Cl-、HCO![]() B.Mg2+、Al3+、Cl-、SO
B.Mg2+、Al3+、Cl-、SO![]()
C.Na+、H+、NO![]() 、OH- D.NH
、OH- D.NH![]() 、Ag+、HCO
、Ag+、HCO![]() 、OH-
、OH-
下列关于11~17号元素性质的比较中,正确的是( )
①元素的最高正化合价依次升高 ②元素的非金属性逐渐增强 ③元素的金属性逐渐减弱 ④元素的最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强
A.只有①② B.只有③④
C.全都不正确 D.全都正确
关于右图所示实验装置的叙述错误的是
A.将水准管上提,液面高于量气管且不下降,说明装置不漏气
B.可用来测定气体摩尔体积
C.可用来测定锌的相对原子质量
D.用CCl4代替水,测得氢气的体积更准确
下列表示正确的是
A.硫离子结构示意图![]()
![]() B.甘氨酸的结构简式:H2NCH2COOH
B.甘氨酸的结构简式:H2NCH2COOH
C.甲烷分子的比例模型:![]() D.NH4I的电子式:
D.NH4I的电子式:
假若你是卫生防疫人员,为配制0.01 mol·L-1的KMnO4消毒液,下列操作导致所配溶液浓度偏高的是( )
A.取KMnO4样品时不慎在表面沾了点蒸馏水
B.溶解搅拌时有液体飞溅出
C.定容时俯视容量瓶刻度线
D.摇匀后见液面下降,再加水至刻度线
常温下,下列各组离子在指定溶液中能大量共存的是
A. pH=12的溶液中:K+、Na+、CO32-、SiO32-
B. c(Fe3+)=0.1 mol·L-1的溶液中:K+、Cu2+、SO42-、SCN-
C. 使甲基橙变红色的溶液中:Na+、ClO-、SO42-、l-
D. 无色溶液中:K+、Al3+、NO3-、HCO3-
课本实验设计得简要明了,但也常存在一些不足,在学习过程中对其进行分析与改进是研究性学习的一个重要课题。
Ⅰ.草酸晶体(H2C2O4·2H2O)受热易分解(分解温度为175℃),产生CO和CO2。关于草酸晶体受热分解及验证部分分解产物的实验装置如图。

(1)写出草酸晶体受热分解的化学方程式:
__________。
(2)设计该装置欲验证的分解产物是 。
(3)草酸晶体的某些物理性质如下表:
| 分子式 | 颜色、状态 | 水溶性 | 熔点/℃ | 密度/g·cm—3 | |
| 草酸晶体 | H2C2O4·2H2O | 无色晶体 | 易溶于水 | 101.5 | 1.650 |
有同学认为,用该装置进行实验,存在着不合理因素,请分析指出(任答两点):
①
②
Ⅱ.下图甲是 “铜丝在氯气中燃烧”的演示实验,铜丝在氯气中燃烧的主要现象是 。有人对该实验提出了如下改进方案:
①按下图乙所示连接好装置,并检查气密性;

②取下注射器并集满Cl2;
③点燃酒精灯加热1~2min后,再移开酒精灯。迅速将注射针插入石英玻璃管内,并将Cl2缓缓推入玻璃管中;
④拔出针头,再用同样方法快速向玻璃管中推入空气。请回答:
(1)步骤③中,移开酒精灯、推入Cl2时,观察到铜丝继续保持红热状态,由此可判断,该反应为 反应(填“放热”或“吸热”)。
(2)步骤④完成后,发现乙试管中的蒸馏水变为蓝绿色。此时缓缓拉动活塞,使少量NaOH溶液吸入乙试管中,看到试管中有 色的沉淀产生,该反应的离方程式为 。
(3)改进后的实验与课本实验相比较,其优点为
______________。
下图中数据是对应物质的熔点(℃),据此做出的下列判断中正确的是( )
 A.铝的化合物的晶体中有的是离子晶体
A.铝的化合物的晶体中有的是离子晶体
B.表中只有 BCl3 和CO2是分子晶体
C.同族元素的氧化物只能形成同类型的晶体
D.不同族元素的氧化物不能形成相同类型晶体
下列化学反应的方程式书写正确的是( )
A. 高温下加热硝酸铵固体:NH4NO3![]() NH3↑+HNO3↑
NH3↑+HNO3↑
B. 将铝片加入烧碱溶液中:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑
C. 向亚硫酸钠溶液中加入足量硝酸:SO32﹣+2H+=SO2↑+H2O
D. 工业制粗硅:C+SiO2![]() CO2↑+Si
CO2↑+Si
下列关于常见物质的用途说法不正确的是
A.金属钠具有强还原性,可以用来置换TiCl4中的Ti
B.二氧化氯具有强氧化性,可以用来漂白织物
C.碳酸钡可用于肠胃X射线造影检查
D.氢氧化铁胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可以净水
下图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去)其中常温下B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物。N为不溶于水的无机酸。
 |
请回答下列问题:
(1) 写出下列物质的化学式
A:_______________F:____________L:________________
(2) 写出G的一种同素异形体的化学式:
(3)已知工业上生产0.1molB放出4.62kj热量,写出该反应的热化学方程式:
(4)在反应C+E→G+F中,每生成1molG转移 mol电子。
右图所示为800 ℃ 时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )

A.A是反应物
B.前2 min A的分解速率为0.1 mol·L-1·min-1
C. 达平衡后,若升高温度,平衡向正反应方向移动
D.反应的方程式为:2A (g) ![]() 2 B(g) + C(g)
2 B(g) + C(g)
.电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时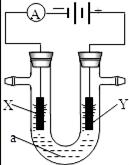 在两边各滴入几滴酚酞试液,则:
在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为 ;在X极附近观察到的现象是 .
②Y电极上的电极反应式为 ;检验该电极反应产物的方法是 .
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为 .
②Y电极的材料是 ,电极反应式为 .(说明:杂质发生的电极反应不必写出)
下列说法正确的是
A. 实验室用加热氯化铵固体制取氨气
B. 漂白粉属于混合物,液氯属于纯净物
C. 醋酸、烧碱和过氧化钠分别属于酸、碱和碱性氧化物
D. 煤的气化与液化均属于化学变化,煤的干馏属于物理变化
短周期元素X、Y、Z、W的原子序数依次增大,其原子的最外层电子数之和为14,X 与Z同主族,Y 与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.简单离子半径:Y<Z
B.W 元素的氧化物对应的水化物可能是弱电解质
C.X2Y2 加入酸性高锰酸钾溶液中,还原产物为X2Y
D.X、Z都能分别与Y 形成含非极性键的分子
有A、B、C、D、E、F、G、H、I九种物质,转化关系如下图所示(相关反应的某些产物在图中已略去).其中A为黑色粉末状固体物质,常用作氯酸钾分解制氧气的催化剂;D在C中燃烧,火焰呈苍白色;E与B接触有大量白烟产生;G为焰色反应呈黄色的强碱.

(1)写出下列物质的化学式:A E G I
(2)写出A+B→C的化学方程式: ;
(3)写出C+G→H+I+H2O的离子方程式: .
下列物质中,既含有极性键又含有离子键的是
A.Na2O2 B.NH4Cl C. CaH2 D.NaCl
- 依次填入下列各句横线处的词语,最恰当的一组是 ①赖昌星,这个中国最大的走私犯罪集团——远华集团的头目,申请加拿大政治
- .“中国为酷爱和平之民族,过去四年余之神圣抗战,原期侵略者之日本于遭受实际之惩创后,终能反省……不料残暴成性之日本,执迷
- 1897年,一代经学大师俞樾对生徒慨叹:“最近三年中,时局一变,风气大开,人人争言西学。”此时“人人争言西学”侧重于
- Here is some information aboutseveral famous local bakeries(
- 美国1787年宪法实际上是一系列妥协的产物,这些妥协包括( )①中央与各州之间的妥协 ②北方资产阶级和南方
- “凡年满六周岁的儿童,不分性别、民族、种族、应当入学接受规定年限的教育。条件不具备的地区,可以推迟到七周岁入学。”这一规
- 实验室中有四瓶失去标签的试剂,分别是四种无色溶液:Na2CO3、Na2SO4、Na2SO3、Na2SiO3,请你只用一种
- I travel a lot, and I find out different “styles”(风格) of dir
- 一金属块在空气中称重为27N,把它全部浸在水中弹簧测力计的示数为17N,则该金属快受到水对它的浮力是
- 阅读下面宋诗,完成后面问题 题西溪无相院① 张先 积水涵虚上下清,几家门静岸痕平。 浮萍破处见山影,小艇归时闻草声。 入
- 元素A和元素B的原子序数都小于18。已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-b
- 住楼房的同学有这样的体验,一楼居民在室内说话,五层的住户是不易听到的,但一楼的人轻轻敲击水管,声音就沿铁管传播出去,各层
- 下列叙述中,错误的是() A.苯与浓硝酸、浓硫酸共热并保持55~60 ℃反应生成硝基苯 B.苯乙烯在合适条件下催化加氢可
- 解:
- 如图∠DAB=∠CAE,请补充一个条件: 使△ABC∽△ADE.
- 近年来,以儒学为代表的传统文化再度复兴,孔子开始了走向全球的新周游列国记——过去五年,中国在全球98个国家和地区建立了3
- 如图所示,电流表的连接正确的是:
- 在正点电荷周围的电场中,有a、b两点.以下说法正确的是A.这两点的电场强度一定不相同,电势也一定不相同B.这两点的电场强
- 如图所示,在调节平衡后的杠杆两侧,分别挂上相同规格的钩码,杠杆处于平衡状态。如果两侧各去掉一个钩码,则 ( )
- —You are always full of .Can you tell me the secre




