高三化学试题
某医药中间体G的一种合成路线如下:

已知:(1)A的核磁共振氢谱有两组峰,且峰面积之比为3∶1;
(2)G的结构简式为:![]() ;
;
(3)![]() 。
。
回答下列问题:
(1)A的名称是_____________;B→C的反应类型是_____________。
(2)G的分子式为___________;G中官能团名称是_____________;1 mol G与NaOH溶液反应最多消耗______ mol NaOH。
(3)H的结构简式为_____________。
(4)D在浓硫酸加热的条件下会生成一种含六元环的化合物,写出该反应的化学方程式_________________________________。
(5)I与F互为同分异构体,则满足下列条件的I的结构有______种(不包括F)。
①苯环上有两个取代基;②遇FeCl3溶液显紫色;③能与NaOH反应。
(6)根据题中所给信息,写出由苯酚,甲苯为原料制备苯甲酸苯酚酯的合成路线(其它无机试剂任选):_________________________________________________________________________。
化学与生活密切相关。下列分析不正确的是( )
A.“煮豆燃豆萁,豆在釜中泣”,句中涉及的能量变化主要是化学能转化为热能和光能
B.食品添加剂可以改善食品品质及延长食品保存期,在添加时无需对其用量进行严格控制
C.“一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”简称,丝绸的主要成分是蛋白质。
D.绿色化学是指在化学产品的设计、开发和加工生产过程中减少使用或产生对环境有害物质的科学
下列操作或试剂不能达到目的是
| 选项 | 目的 | 操作或试剂 |
| A | 比较碳、氯的非金属性强弱 | 稀盐酸、纯碱 |
| B | 除去KNO3中少量NaCl | 冷却结晶 |
| C | 将MnO4—完全转化为Mn2+ | H2O2 |
| D | 除去水中的FeCl3杂质 | 蒸馏 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:A>B>C>D B.原子序数:d>c>b>a
C.离子半径:C3->D->B+>A2+ D.元素的第一电离能:A>B>D>C
在通常条件下,下列各组有机物的性质排列错误的是
A.沸点:正戊烷>异戊烷 B.密度:CH3CH2CH2Cl>CH3CH2Cl
C.熔点:CH3CH2CH2Cl>CH3CH2Cl D.水溶性:CH3CH2OH>CH3CH2CH2CH2OH
X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大, W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
(1)L的元素符号为 ;M在元素周期表中的位置为 。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 。
(3)Y的最高价氧化物的电子式为 。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一种新型无机非金属材料,其化学式是 。
用海水制盐工业中的母液来生产金属镁的一种工艺流程如下下列说法错误的是( )

A. 上述工艺流程中未涉及置换反应
B. 设计步骤①、②、③的主要目的是富集MgCl2
C. 脱水时在HCl气氛中进行可抑制MgCl2水解
D. 电解得到的炽热镁粉可在氮气中冷却
用相对分子质量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为
A.3 B.4 C.5 D.6
在实验室中不宜长期保存,必须现用现配的是:①溴水 ②银氨溶液 ③石灰水 ④氯水 ⑤氢硫酸 ⑥NaOH溶液 ⑦FeSO4溶液 ⑧FeCl3溶液 ⑨CuSO4溶液 ⑩醋酸
A.②③④⑧⑨ B.⑤⑦⑧⑨⑩
C.②③④⑤⑦ D.①⑥⑧
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。


已知:Fe(OH)2为絮状沉淀难以过滤除去,各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 1.5 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(2)堆浸后加入Fe粉发生的反应离子方程式为: 、 。
(3)加入A 物质的目的是 ,物质A可使用下列物质中的 。(填字母,双选)
A.KMnO4 B.O2 C.H2O2 D.NaOH
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(5)溶液B中主要溶质的化学式是 。
下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:则下列说法正确的是( )
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)⇌FeO(s)+CO(g)△H1 | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)⇌FeO(s)+H2(g)△H2 | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O (g)⇌CO2(g)+H2(g)△H3 | K3 | ? | ? |
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2﹣△H1=△H3
C.反应①②③的平衡常数满足关系:K1•K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
下列有关环境方面的说法不正确的是( )
A.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
B.采用天然石材装修家居,可减轻室内甲醛污染但会导致一定量的放射性物质的污染
C.汽油中添加含铅化合物Pb(C2H5)4,可提高汽油的抗爆震性能,有利于改善大气环境
D.PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重
最近有研究人员发现了一种处理高浓度乙醛废水的新方法——隔膜电解法,实验室以一定浓度的乙醛-Na2SO4溶液为电解质溶液,采用如图所示装置电解,电解后乙醛转化为乙醇和乙酸。则下列说法不正确的是( )

A.阳极产物为乙酸,发生氧化反应
B.电解时,阳极区附近pH 增大
C.阴极反应式为CH3CHO+2H++2e-=CH3CH2OH
D.若以CH4一空气燃料电池为直流电源,则燃料电池的a 极应通入空气
下列各选项中的两个反应,可用同一个离子方程式表示的是( )
| 选项 | Ⅰ | Ⅱ |
| A | Ba(OH)2溶液与过量NaHCO3溶液混合 | NaOH溶液与过量NaHCO3溶液混合 |
| B | 少量SO2通入Ba(OH)2溶液中 | 过量SO2通入Ba(OH)2溶液中 |
| C | BaCl2溶液与Na2SO3溶液混合 | Ba(OH)2溶液与H2SO3溶液混合 |
| D | 少量氨水滴入AlCl3溶液中 | 少量AlCl3溶液滴入氨水中 |
A.A B.B C.C D.D
聚酯增塑剂广泛应用于耐油电缆、煤气管、防水卷材、电气胶带;耐油耐汽油的特殊制品等。聚酯增塑剂G及某医药中间体H的一种合成路线如下(部分反应条件略去):

已知:

(1)B的名称(系统命名)为 。
(2)若反应①的反应条件为光照,最先得到的氯代有机物结构简式是 。
(3)写出下列反应的反应类型:反应②是 ,反应④是 。
(4)写出B与D反应生成G的反应方程式 。
(5)甲苯的二氯代物产物的同分异构体有 种。
(6)利用以上合成路线的信息,以甲苯和乙醇为原料合成下面有机物(无机试剂任选),
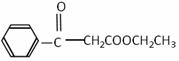
请写出合成路线。
如图所示,常温常压下气体X(见选项)与O2等物质的量混合后充满圆底烧瓶,挤压胶头滴管并打开止水夹,可观察到烧杯中的水沿导管进入烧瓶。长时间充分反应后,烧瓶中所得溶液的物质的量浓度最小的是(假设溶质不向烧瓶外扩散)

A.NH3 B.HCl C.SO2 D.NO2(假设不含N2O4)
FeS能跟盐酸反应生成H2S气体和FeCl2。把8.8FeS放入200mL2.0mol/L的盐酸中,以制备H2S。反应完全后,若溶液中H2S的浓度为0. 1mol/L,假定溶液的体积不变,试计算
(1)收集到的H2S的体积;(2)溶液中Fe2+、H+的浓度。
已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。
其制备反应及与水反应的化学方程式如下:
①CS2+3Cl2 ![]() CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓
CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓
则下列说法正确的是 ( )
A.反应①中CS2作氧化剂
B.反应②中S2Cl2既作氧化剂又作还原剂
C. 反应①中每生成1mol S2Cl2转移4mol电子
D.反应②中氧化产物与还原产物的物质的量之比为3:1
下列说法正确的是( )
A.pH=0的溶液不存在
B.使用广泛pH试纸测得某溶液的pH=3.5
C.中性溶液的pH不一定等于7
D.酸或碱溶液在稀释时,溶液的pH均减小
下列说法正确的是( )

A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体
B.图Ⅱ装置可验证非金属性:Cl>C>Si
C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3
D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化
- 下图所示的地点中,位于中国境内的是( )
- 下列说法正确的是( )A.氯水具有漂白作用,故氯水可使橙色的溴水褪为无色B.将F2通入NaBr溶液中,可使溶液变橙
- 与可持续发展不相符的一项是() A.当发展经济与保护生态环境相矛盾时,首先保护当代人的利益 B.经济与生态环境协调发展
- 水是人类生活中不可缺少的物质.下列关于水的说法中正确的是() A.水是取之不尽用之不竭的 B.用肥皂水可区分硬水和软水
- 法国1875年宪法修正条文规定“凡曾经统治过法国的家庭不得当选为共和国总统”,其作用是 A.阻塞了所有君主
- 从4名男生和3名女生中选出3人,分别从事三项不同的工作,若这3人中有且只有1 名女生,则选派方案共有 A.108种
- 阅读下面的文言文,完成后面题目。 赵延进,澶州顿丘人。父晖,周太子太师。延进颇亲学,尝与乱军入民家,少年同行者竞取财贿,
- 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200 mL C(OH-)= 0.1mol/L的溶液,然后逐滴加入
- “a=1”是“函数y=cos2ax-sin2ax的最小正周期为π”的( ) A.充分不必要条件
- In 1947 Angela Mortimer was captain of the team which wont
- 相同质量的下列物质分别与等浓度的NaOH溶液反应至体系中均无固体物质,消耗碱 量最多的是 A.Al
- 依次填入下列两句中横线处的语句,上下文语意连贯的一组是( ) ⑴王维新是中国水彩画坛的画家。在他的画中,
- 2010年4月30日,举世瞩目的上海世界博览会盛大开幕。回答下题。 上海世博会也是志愿者的盛会。20多万世博会志愿者正通
- The news about the terrible flood there greatly discouraged
- Let those in needthatwe will go all out to help them. A.to u
- 下图反映的是罗马教廷兜售赎罪券的情景。有关该图的历史阐释正确的是( )①罗马教廷在德意志常常通过这种方式搜刮财富,
- 已知正项等比数列中,,且成等差数列. (1)求数列的通项公式; (2)若,求数列的前项和.
- 等比数列的各项都是正数,且,则( ) A. B. C.
- Can you imagine the singer _____ so much in public? A. being
- 两个电子以大小不同的初速度沿垂直磁场的方向射入同一个匀强磁场中。设r1、r2为这两个电子的运动轨道半径,T1、T2是它们



