高三化学试题
氧化还原反应是重要的反应类型,下列有关说法正确的是
A.1molAl和足量的NaOH溶液反应,失去的电子数为3NA(NA表示阿伏加德罗常数)
B.原电池的负极发生氧化反应,电解池的阳极发生还原反应
C.Cu能被FeCl3溶液腐蚀,其离子方程式为:Cu+Fe3+==Cu2++Fe2+
D.Na+、Ba2+、NO3-、SO32-四种离子在溶液中因发生氧化还原反应而不能大量共存
碳与浓硫酸共热产生的气体X和铜与浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法不正确的是

A.洗气瓶中产生的沉淀是碳酸钡 B.在Z导管出来的气体中有二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡 D.在Z导管口有红棕色气体出现
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2 mol CuO,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的物质的量为
A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 1.0 mol
利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为CH4(g)+H2O(g)⇌CO(g)+3H2(g).
(1)甲烷与水蒸气反应,被氧化的元素是 ,当生成标准状况下35.84L合成气时转移电子的物质的量是 .
(2)将2mol CH4和5mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度、压强的关系如图所示.
①若达到A点所需的时间为5min,则v(H2)= ,100℃时平衡常数K=﹣2 .
②图中的p1 p2(填“<”、“>”或“=”),A、B、C三点的平衡常数KA、KB、KC的大小关系是 .
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0.
下列措施中能使![]()
![]() 增大的是 (填编号).
增大的是 (填编号).
A.降低温度
B.恒温恒容下充入He(g)
C.将H2从体系中分离
D.再通入一定量的水蒸气.


氮和碳的化合物与人类生产、生活密切相关。
(1)已知:N2(g)+O2(g)===2NO(g); ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g); ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH= 。
(2)在压强为0.1 MPa条件,将CO和H2的混合气体在催化剂作用下转化为甲醇的反应为
CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
①下列能说明该反应达到平衡状态的是 。
a.混合气体的密度不再变化 b.CO和H2的物质的量之比不再变化
c.v(CO)=v(CH3OH) d.CO在混合气中的质量分数保持不变
②T1℃时,在一个体积为5 L的恒压容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.75,则T1℃时,CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K= 。
CH3OH(g)的平衡常数K= 。
 ③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平
③在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平
衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当
![]() 时,达到平衡状态,CH3OH的体积分数可能是图象中的
时,达到平衡状态,CH3OH的体积分数可能是图象中的
点。
(3)用催化转化装置净化汽车尾气,装置中涉及的反应之一为:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)

①探究上述反应中NO的平衡转化率与压强、温度的关系,得到如图1所示的曲线。催化装置比较适合的温度和压强是___________。
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图2所示。则前10 s内,CO和NO百分含量没明显变化的原因是____________。
 (4)右图所示的装置能吸收和转化NO2和SO2。
(4)右图所示的装置能吸收和转化NO2和SO2。
①阳极区的电极反应式为 。
②阴极排出的溶液中含S2O![]() 离子,能将NO2气体转化为
离子,能将NO2气体转化为
无污染气体,同时生成的SO![]() 可在阴极区再生。写出该反应的离子方程式: 。
可在阴极区再生。写出该反应的离子方程式: 。
二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图:
 |
⑴ 粗食盐水中含有Ca2+、Mg2+、SO![]() 等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是 (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是 (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO![]() ,其原因是
,其原因是
。(已知:Ksp(BaSO4)=1.1×10-10 ;Ksp(BaCO3)=5.1×10-9)
⑵上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成ClO2。电解时生成的气体B是 ;反应Ⅲ的化学方程式为 。
⑶ ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O![]() =2I-+S4O
=2I-+S4O![]() )
)
① 准确量取10.00 mL ClO2溶液的玻璃仪器是 。
② 滴定过程中,至少须平行测定两次的原因是 。
③ 根据上述步骤可计算出原ClO2溶液的物质的量浓度为 mol·L-1(用含字母的代数式表示)。
甲、乙两同学欲分别完成“钠与氯气反应”的实验。
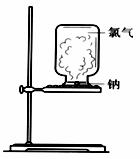


Ⅰ.甲同学的方案为:取一块绿豆大的金属钠(除去氧化层),用滤纸吸净煤油,放在Ⅰ石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶抽去玻璃片后倒扣在钠的上方(装置如图Ⅰ)。该方案的不足之处有 _____________ 。
Ⅱ.乙同学所采用的装置如图Ⅱ,回答下列问题:
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为 ;待整套装置中 后,点燃酒精灯。
(2)点燃酒精灯后,玻璃管中出现的现象是 。
(3)乙同学欲将虚框内装置改为图Ⅲ所示装置,并测量多余气体的体积。
①为提高测量的准确性,图Ⅲ量气管装置中的液体可用 ;收集完气体后并读数,读数前应进行的操作是冷却至室温并 。
②若未冷却至室温立即按上述操作读数,则会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)
③ 如果开始读数时操作正确,最后读数时俯视右边量气管液面,会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。
在强酸性溶液中,下列各组离子能够大量共存的是( )
A. Fe2+、NH4+、Cl-、NO![]() B.Na+、K+、Cl-、AlO2-
B.Na+、K+、Cl-、AlO2-
C.K+、Ba2+、Cl-、NO3- D. Fe3+、Al3+、Cl-、SCN-
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫
酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的
量浓度之比是C
A.3∶2∶2 B.1∶2∶3 C.1∶3∶3 D.3∶1∶1
(1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能符合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1=-285.8KJ/mol
C8H18 (1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH3=-5518KJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式________
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-53.7 kJ·mol-1平衡常数 K1
CH3OH(g)+H2O(g) △H=-53.7 kJ·mol-1平衡常数 K1
乙:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H=+41.2 kJ·mol-1平衡常数K2
CO(g)+H2O(g) △H=+41.2 kJ·mol-1平衡常数K2
①CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应H_____0(填“大于”或“小于”)。
CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应H_____0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________(填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)
| 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
| 543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
| 543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
| 553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
| 553 | Cu/ZnO纳米片材料 | 12.0 | 71.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________(填字母符号)。
(3)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)=CH3OH(g)。在体积均为2L的三个恒容密闭Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。图1为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。CO的平衡转化率在不同压强下随温度的变化如图所示。


①0~5 min时间内容器Ⅱ中用CH3OH表示的化学反应速率为__________。
②三个容器中一定达到平衡状态的是容器________(填写容器代号)。
③工业实际合成CH3OH生产中,采用图2中M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由_________________________。
关于如图所示实验的说法不正确的是( )


A.乙中产生的气泡是C02
B.丙中液体可产生丁达尔现象
C.若忽略溶液体积的变化,烧杯中c(Cl﹣)不发生变化
D.若将CaC03换成CaS04也可得到相同的实验现象
甲流感问题已成为目前人们关注的热点。防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感。
(1)下列含氯化合物中氯元素化合价最高的是____________(填编号,下同)。
A. HCl B. KClO3 C. HClO D. ClO2
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了还原反应的是____________。
A.MnO2 B.KMnO4溶液 C.稀硫酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温下放在黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:5HClO2=4ClO2↑+H++Cl-+2H2O。当1 mol HClO2发生分解反应时,转移的电子个数是____________________。
(4)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在酸性条件下与Na2SO3反应制得。请写出该反应的离子方程式____________ 。
向100 mL0.2mol/L的NaOH溶液中通入标准状况下的CO2448 mL,则最终溶液中粒子间关系不正确的是
A.C(Na+)+C(H+)==C(HCO3—)+C(CO32—)+C(OH—)
B.C(H+)+ C(H2CO3)— C(CO32—) == C(OH—)
C.C(Na+)>C(HCO3—) >C(OH—) >C(H+)>C(CO32—)
D.C(HCO3—) + C(CO32—) + C(H2CO3) == 0.2mol/L
下列有关元素及其化合物的说法中正确的是
A.浓硫酸中存在的主要是硫酸分子,常温下就能与铜片剧烈反应
B.工业上常用H2和Cl2直接化合的方法生产氯化氢以制取盐酸
C.SO2具有漂白性,所以能使碘的淀粉溶液由蓝色变为无色
D.向FeCl2溶液中滴加氯水,溶液变为棕黄色,说明氯水中含有HClO分子
常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)基态亚铜离子(Cu+)的价层电子排布式为________;高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:______________________________________________。
(2)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是___________________________。
(3)GaCl3和AsF3的立体构型分别是____________,____________。
(4)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为______________。
②[B(OH)4]-的结构式为________________。
(5)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是________________(用化学式表示);
②金刚石的晶胞参数为a pm(1 pm=10-12 m)。 1cm3晶体的平均质量为______________(只要求列算式,阿伏加德罗常数为NA)。
设NA为阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,2.24 L H2O中含有极性共价键的数目为0.2 NA
B.0.1 mol·L-1 NH4Cl溶液中含有NH4+的数目小于0.1 NA
C.100 mL 12 mol·L-1的浓HNO3与过量Cu反应转移电子的数目为0.6 NA
D.标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA
工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业.
(1)写出NaCl的电子式 .
(2)若采用无隔膜法电解冷的食盐水时,Cl2会与NaOH反应,导致产物仅是NaClO和H2.无隔膜法电解冷的食盐水相应的离子方程式为 .
(3)氯碱工业耗能高,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.

①经精制的饱和NaCl溶液应从图中电解池的 (填写“左”或“右”)池注入.
②图中X是 (填化学式);图示中氢氧化钠溶液质量分数a%与b%的关系是 (填字母).
A.a%=b% B.a%>b% C.a%<b%
③上述设计的主要优点有(写出一个方面) .
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaClO | NaHCO3 | NaHSO3 |
| pH | 11.6 | 10.3 | 9.7 | 5.2 |
下列说法中,不正确的是 (填字母).
a.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
b.四种溶液中,水的电离程度最大的是NaClO
c.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
d.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3﹣)>c(SO32﹣)>c(OH﹣)
e.NaHCO3溶液中c(H+)+c(H2CO3)=c(OH﹣)+c(CO32﹣)
某同学用下列装置制备并检验Cl2的性质,下列说法正确的是


A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条退色
利用下列实验装置能完成相应实验的是
A.除去氯气中的氯化氢 B.实验室制氨气
B.实验室制氨气
制取并收集氯化氢
D.证明乙醇发生消去反应生成了乙烯
下列说法正确的是
A. 氯水应保存在棕色广口瓶中并置于阴凉处
B. 用玻璃棒蘸醋酸溶液点在用水润湿的pH 试纸上,测定该溶液pH
C. 焰色反应时,先用稀盐酸洗涤铂丝并在酒精灯火焰上灼烧至无色,然后再进行实验
D. 用容量瓶配制溶液时,先用蒸馏水洗涤,再用待装溶液润洗
- (本小题12分)过原点且斜率为的直线与直线:2x + 3y -1=0交于点,求过点且圆心在直线上,并与直线相切的圆的方程
- 仿照示例,从“金钱”“权力”“网络”“时尚”中选择一个词语,用比喻的手法(不 得使用同一喻体)写一句话,对其
- 下列有关基因工程中载体的说法正确的是 A.在进行基因工程操作中,被用作载体的质粒都是天然质粒 B.所有的质粒都可以作为基
- 我国粮食连续四年增产,使我国粮价趋于稳定,有利于调动农民的种粮积极性,有利于维护人民的切身利益,保持我国独立自主的地位。
- (一)文言文阅读(19分) 阅读下面的文言文,完成10—13题。 崔慰祖,字悦宗,清河东武城人也。父庆绪,永明中为梁州刺
- 下列植物中常用扦插繁殖的是() A.玉米 B.马铃薯 C.月季
- 下列句子中,加点的成语使用恰当的一项是( ) A.张炜创作的450万字的鸿篇巨制《你在高原》,长篇累牍地描绘了广
- 如图B-2所示为医院为病人输液的部分装置,图中A为输液瓶,B为滴壶,C为进气管,与大气相通.则在输液过程中(瓶A中尚有液
- (11分)(1)若2.6g乙炔(C2H2气态)完全燃烧生成液态水和CO2时放热130kJ。则此反应的热化学方程式为:
- 为探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组设计了如下图所示的实验装置。试填空。 (1)请你预测C12
- 已知向量=(2,-1)与向量共线,且满足=-10,则向量=____________.
- The patient______ H1N1 were separated with others and taken
- 一滴水只有放进大海才永远不会干涸;没有班集体中人与人之间的团结协作,个人的智慧就难以发挥作用。下列选项中能够正确说明这个
- 已知函数 (1)求函数的最小正周期; (2)求使函数取得最大值的x集合; (3)若,且,求的值。
- 据中新网上海6月1日电:世博会开园一个月来,客流平稳,累计至当晚19时,参观者已超过8000000人次。试用科学记数法表
- 下列属于无性繁殖方式的是: A、播撒小麦种子种地
- Our Chinese teacher as well as all of us ________ going to t
- 两宋时期出现较高艺术成就的主要条件是() A.隋唐时期奠定了良好基础 B.民族融合进一步加强 C.城市手工业
- 阅读下面的文言文,完成下面试题 指 喻 方孝孺 浦阳郑君仲辨,其容阗然①,其色渥然②,其气充然,未尝有疾也。他日,左手
- 先化简,再求值:,其中。



