高三化学试题
已知:①2Na(s) +![]() O2(g)=Na2O(s) △H=-414 kJ/mol
O2(g)=Na2O(s) △H=-414 kJ/mol
②2Na(s) +O2 (g)=Na2O2(s) △H=-511 kJ/mol
下列说法不正确的是
A.反应①和②均属于放热反应
B.①和②产物的阴阳离子个数比相同
C.①和②生成等物质的量的产物,转移电子数不同
D.反应Na2O2(s)+2Na(s)=2 Na2O(s)的△H =- 317 kJ/mol
短周期主族元素X![]() 、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族。下列说法正确的是
、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族。下列说法正确的是
A.元素X、W的简单阴离子具有相同的电子层结构
B.由Y、Z两种元素组成的化合物是离子化合物
C.W的简单气态氢化物的热稳定性比Y的强
D.原子半径:r(X)<r(Y)<r(Z)<r(W)
工业上可采用惰性电极处理含Na2SO4的废水,得到其它工业产品。其原理如图所示,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

![]()
下列叙述不正确的是
A.通电后中间隔室的SO42-离子向正极区迁移,电解后正极区PH减小
B.ab为阳离子交换膜,负极区得到NaOH溶液
C.负极区反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.每有1molO2生成,会有4molNa+进入负极区
R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;
X2+ + Z=X + Z2+;Z2+ + Y=Z + Y2+。这四种离子被还原成0价时表现的氧化性大小符合( )
A.R2+>X2+>Z2+>Y2+ B.X2+ >R2+ >Y2+>Z2+
C.Y2+>Z2+>R2+>X2+ D.Z2+>X2+>R2+>Y2+
下列说法正确的是 ( )
A.铜锌原电池,锌为正极
B. 化学反应的反应热不仅与反应体系的始态和终态 有关,还与反应的途径有关
C.在氧化还原反应中,还原剂失去电子的总数等于氧化剂得到电子的总数
D.通过化学变化可以直接将水转变为汽油
纳米级Fe粉是新型材料,具有超强磁性、高效催化性.某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉.其实验设计如图(加热、支持装置省略)
(1)a的名称是 ;浓硫酸的作用是 .
(2)打开分液漏斗活塞,一段时间后再对C装置加热,这样操作的目的是 ;反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应的化学方程式为 .
(3)反应中若观察到B装置中气泡产生过快,则应进行的操作是 .
(4)反应一段时间后,B中产生气泡太慢,再滴加硫酸反应速率略有加快但不明显;若向硫酸中加少量硫酸铜再滴入与Zn反应,反应速率明显加快,原因是 .
(5)检验碳酸亚铁中含有铁元素的实验方法是 .


下列各组离子中的离子,能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl-、OH- B.H+、Ca2+、CO32-、NO3-
C.Cu2+、K+、SO42-、NO3- D.Na+、H+、OH-、Ca2+
在含有NaI、Na2SO3和FeBr2 各1mol的溶液中通入足量的Cl2,将溶液在空气中加热蒸干并充分灼烧,最终得到剩余的固体物质是( )
A.NaCl、FeCl3、Na2SO4 B.NaCl、FeBr3
C.NaCl、Fe2O3、Na2SO4 D.Na2SO4
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下表所示,其中Q是无机非金属材料的主角。下列判断正确的是( )

A.离子半径:T<W<G
B.等物质的量的W、G单质分别与足量铁粉反应,后者消耗的铁粉多
C.最简单气态氢化物的热稳定性:Q<R
D.T和G组成的化合物溶于水,其水溶液呈中性
短周期主族元素A、B、C、D、E、F原子序数依次增大,A的某种核素没有中子,B、C、D、E在周期表中位置如图,且四种元素原子序数之和为37,下列说法不正确的是
![]()
A.含B元素的化合物在自然界中种类最多 B.A、C、D三元素可组成促进水电离的化合物
C.原子半径由大到小顺序:E>F>C>A D.氢化物的稳定性:D<E
环境与可持续发展是现在国际性环保的主题,利用海水是可持续发展的一个任务,对于海水的利用认识错误的是( )
A.海水中有大量人类需要的物质,人类可以大量开发海水中的物质,以满足资源短缺的问题
B.海水可以成为廉价的能源基地,但不能开发过度,要适度使用和开发
C.可以用太阳能电解海水以获取氢能源
D.人类在利用海水时要兼顾海洋生物和海洋生态平衡
向27.2g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是( )
Cu与Cu2O的物质的量之比为2:1
硝酸的物质的量浓度为2.6mol/L
产生的NO在标准状况下的体积为4.48L
Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
许多环境问题是跨国界的,甚至是全球性的。根据《蒙特利尔议定书》的有关要求,我国政府采取了一系列措施来保护地球环境,如2002年起我国汽车业就全面禁用氟里昂(Freon)空调、2005年开始停止生产“哈龙(Halons)1211灭火器”等。这主要是由于氟里昂、哈龙等物质都是 ( )
A.有机化合物 B.极易挥发的物质
C.破坏臭氧层的物质 D.引起温室效应的物质
叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。

(1)甲中显酸性的官能团是 (填名称)。
(2)下列关于乙的说法正确的是( )
A.分子中碳原子与氮原子的个数比是7:5
B.属于芳香族化合物
C.既能与盐酸又能与氢氧化钠溶液反应
D.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为__________。
a.含有![]()
b.在稀硫酸中水解有乙酸生成
(4)甲可以通过下列路线合成(分离方法和其他产物已经略去):
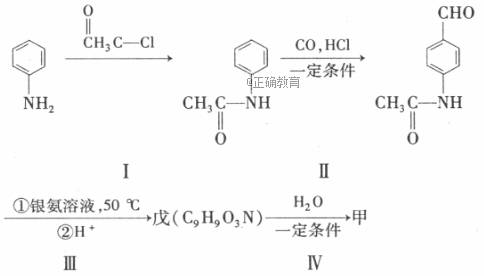
①步骤Ⅰ的反应类型是________________。
②步骤Ⅰ和Ⅳ在合成甲过程中的目的是_____________________________________________。
③步骤Ⅳ反应的化学方程式为_____________________________________________________。
在下列元素中,不属于主族元素的是
A.铁 B.铍 C.砷 D.碘
下列物质:①H2O ②NaCl ③H2SO4 ④Ca(OH)2 ⑤Fe2O3 ⑥CuSO4·5H2O ⑦HNO3 ⑧AgNO3 ⑨NaHCO3 其中属于氧化物的是________,属于碱的是________,属于酸的是________,属于盐的是______
铬铁矿(FeCr2O4)中含有Al2O3、Fe2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程示意图如下(部分操作和条件略):

(1)铬铁矿(FeCr2O4)改写为氧化物的形式为______________________。
(2)反应①中发生了两个主要反应,其中一个主要反应的化学方程式为Na2CO3 + Al2O3![]() 2NaAlO2 + CO2↑,另一个主要反应的化学方程式为_____________________。
2NaAlO2 + CO2↑,另一个主要反应的化学方程式为_____________________。
(3)写出反应②中生成固体B的离子方程式_______________________。
(4)下表是相关物质的溶解度数据:
| 物质 | 溶解度(g/100g H2O) | 物质 | 溶解度(g/100g H2O) | ||||
| 0℃ | 40℃ | 80℃ | 0℃ | 40℃ | 80℃ | ||
| KCl | 28 | 40.1 | 51.3 | K2Cr2O7 | 4.7 | 26.3 | 73 |
| NaCl | 35.7 | 36.4 | 38 | Na2Cr2O7 | 163 | 215 | 376 |
pH﹤5时,发生反应的化学方程式之一为Na2Cr2O7 + 2KCl ![]() K2Cr2O7 + 2NaCl。该反应能发生的理由是____________________________________________________________________________。
K2Cr2O7 + 2NaCl。该反应能发生的理由是____________________________________________________________________________。
(5)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化为乙酸,自身被还原为三价铬离子,该反应的离子方程式为__________________________________。
(6)已知Ksp[Fe(OH)3] = 4.0×10-38,Ksp[Cr(OH)3] = 6.0×10-31 。含铬废渣废水的随意排放对人类生活环境有极大的危害,电解法是处理铬污染的一种方法,电解时,在阴极区有Fe(OH)3和Cr(OH)3沉淀生成,已知电解后的溶液中c(Cr3+)为3.0×10-5 mol·L-1,则溶液中c(Fe3+)为________mol·L-1。
 为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。![]()
![]()
![]()
试验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。![]()
![]()
![]()
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ(1)A中产生黄绿色气体,其电子式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 ,得电子能离逐渐减弱。
【物质结构与性质】(12分)
元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是![]() 其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子,W原子的2p轨道上有3个未成对电子。
其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子,W原子的2p轨道上有3个未成对电子。
(1)Y与W、Z可形成多种化合物。
①元素Y与Z中电负性较大的是 (用元素符号描述)。
②离子ZY32-的空间构型为 (用文字描述),杂化方式 。
③ZY2空间构型 ,杂化方![]() 式 ,分子的极性 (填“极性”或“非极性”)。
式 ,分子的极性 (填“极性”或“非极性”)。
④元素Y与W中第一电离能较大的是 (用元素符号描述)。
(2)Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是 。
(3)含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH![]() 3)]。
3)]。
①基态X2+的电子排布式是 。
②1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为 。
③画出X原子的价电子排布图 ;
④ [X(CN)5(NH3)]3-配离子中存在的化学键类型有 (填序号):
a、配位键 b、氢键 c、极性共价键 d、非极性共价键 e、离子键
下列酸性H 2CO 3>HClO>HCO 3 —,下列有关叙述中正确的是
①向NaClO溶液中通入少量二氧化碳的离子反应方程式为:2ClO —+CO 2+H 2O=2HC1O+CO 3 2 —
②向KI和KBr混合溶液中,加入足量FeCl 3溶液,用CCl 4萃取后取上层中的液体少许并加入AgNO 3溶液,有淡黄色沉淀生成
③向FeI 2溶液中滴加少量氯水。反应的离子方程式为:2Fe 2++Cl 2=2Fe 3++2Cl —
④卫生间的洁厕灵不能跟84消毒液混用,其离子方程式为:ClO —+Cl —+2H +=Cl 2↑+H 2O
| A.②④ | B.①③ | C.②③ | D.①④ |
- 如图11所示实验中,当塞子从试管口喷出时,水蒸气的 能转化成为塞子的 能。
- 根据汉语拼音写出汉字。(4分)①烦 (zào) ② (xiáng)和 ③眼花(liáo) 乱 ④言简意 (gāi
- 每年5月的第二个星期日就是母亲节。今年母亲节的主题是:“只要妈妈快乐,我们就快乐!”请问胎儿在母体内的发育场所是(
- 下列语句出自不同时期的历史文献或历史人物之口,其中分析不恰当的是( ) 甲:“戮力本业,耕织致粟帛多者,事末利及怠而
- 将30 mL 0.5mol·L—1的NaOH溶液加水稀释到500 mL,稀释后NaOH的物质的量浓度为 A.0.3 mo
- 近亲结婚,患遗传病可能性大的原因是血缘关系越近() A.生活环境也相同
- 下面是以绿色为主色调的“2010上海世博会”会徽标识,请从构形角度说明该标识的创意。要求语意简明,句子通顺,不超过80字
- 在明清之际出现了反对君主专制的进步思想,根本原因是 ( )A.知识分子具有忧国忧民思想
- 为帮助延边朝鲜族自治州快速发展,吉林省在项目建设和财政支出上加大支持力度,落实国家“兴边富民”政策,重视发展朝鲜族的民族
- 如图所示,连接平行金属板P1和P2(板垂直纸面)的导线的一部分CD和另一连接电池的回路的一部分导体GH平行,CD和GH均
- 3.在含1.17克NaCl和0.84克NaF的溶液中,加入过量的AgNO3溶液,产生2.87克沉淀,由此可以推断( )A
- 莫里循是澳大利亚人,曾任《泰晤士报》驻华首席记者,中华民国总统政治顾问。他居住北京20余年(1887—1920年),亲历
- 跳伞运动员从350米高空跳伞后,开始一段时间由于伞没打开而做自由落体运动,伞张开(张开时间不计)后做加速度为2 m/s2
- 16.下面是2016年9月在我国杭州召开的G20峰会会标,请写出图标中除文字以外的构图要素,并说明寓意,要求语言简明,句
- 平面内与两个定点F1(-3,0)、F2(3,0)的距离的和等于10的点P的轨迹是椭圆,点P的轨迹方程是________,
- 厄立特里亚气候干旱,2007年人均国民收入仅270美元,农业是国民经济的支柱,但粮食不能自给。农业生产技术相对落后,很少
- 若某蛋白质的相对分子质量为11935,在合成这个蛋白质分子的过程中脱去水的相对分子质量为1908,假设氨基酸的平均相对分
- (8分)从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:(1)甲中含氧官能团的名称为 ,乙
- 下列群落演替的实例中,属于初生演替(或原生演替)的是( ) A.火灾后草原的演替 B.
- 如图甲所示是某实验小组同学探究“平面镜成像特点”的实验情景:(1)该小组同学应该选取两根 相同 (选填“相同”或“不相同



