高三化学试题
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,其中A在常温下能与水发生剧烈反应,B是目前使用最多的金属。物质之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙 ; F ;
(2)写出下列反应的离子方程式:
①金属A和水反应的离子方程式 。
②D和G的水溶液反应的离子方程式 。
(3)将G浓溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在 之间,验证的简单方法是: 。
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
下列实验操作正确的是 ( )
A.中和滴定实验时,用待测液润洗锥形瓶
B.盛放Na2SiO3溶液时,使用带玻璃塞的磨口瓶
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热
某溶液仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
| 阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 阴离子 | Cl- CO32- NO3- SO42- I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是____________________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是______________________。
(3)甲同学最终确定原溶液中所含阳离子有____________,阴离子有____________;
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为___________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为____________g。
下列各组中前者的碱性比后者强的是( )
A. KOH和Al(OH)3 B. Mg(OH)2 和NaOH
C. Al(OH)3和Mg(OH)2 D. Mg(OH)2和Ca(OH)2
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如右图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的( )


A.Y元素最高价氧化物对应的水化物化学式为H3YO4
B.原子半径由小到大的顺序为:X<Z<Y<W
C.与同浓度的盐酸反应,Z比W更剧烈
D.X的氧化物不能与Z单质反应
表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题.

请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
某同学按下图所示的装置进行试验。A、B为两种常见金属,它们的硫酸盐可溶于水。当K闭合时,在交换膜处SO42﹣从右向左移动。下列分析错误的是( )

A.金属活动性A强于B
B.B的电极反应:B﹣2e-=B2+
C.X电极上有H2产生,发生还原反应
D.反应初期,x电极周围出现白色沉淀,不久沉淀溶解
下列有机物中,不属于烃的衍生物的是( )
A.卤代烃 B.酒精 C.氯仿 D.邻甲乙苯
根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中滴加 | 原溶液中有Fe2+,无Fe3+ |
| B | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
| C | 向碘水中加入等体积的CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
| D | 向某溶液中先加入Ba(NO3)2溶液,有白色沉淀生成;再加入足量盐酸,白色沉淀不消失 | 原溶液中一定含有SO |
A.A B.B C.C D.D
C和CuO在一定温度下反应,产物有Cu、Cu2O、CO 、CO2。若将2.00gC与16.0gCuO混合,隔绝空气加热,将生成的气体全部通入足量的澄清石灰水,反应一段时间后共收集到1.12 L (标准状况)气体,生成沉淀的质量为5.00 g。下列说法不正确的是
A.反应后的固体混合物中Cu的质量为12. 8 g
B.反应后的固体混合物中含有碳
C.反应后的固体混合物总质量为14. 4 g
D.反应后的固体混合物中氧化物的物质的量为0.05 mol
下列四幅图示所表示的信息与对应的叙述相符的是

A.由图1可知H2的标准燃烧热为241.8kJ·mol-1
B.图2表示某吸热反应分别在有、无催化剂的反应过程中的能量变化
C.反应热与途径无关,由图3可知△H3>△H2
D.由图4可知该反应△H=(E2-E1)kJ·mol-1
在14.0g银铜合金中加入500mL一定浓度的浓硝酸,合金全部溶解,收集到NO2和NO体积共2.24L(标准状况下),再向该溶液中加入bml,4mol/L的NaOH溶液,刚好使溶液中的阳离子沉淀完全;若将收集到的气体全部与标准状况下的O21.12L充分混合后,通入水中二者刚好完全反应.下列有关说法不正确的是( )
A.银的质量为10.8g
B.NO与NO2的体积比之比(相同条件下)为2:1
C.原硝酸的物质的量浓度(0.1mol+4b×10﹣3mol)/0.5L
D.沉淀中Cu(OH)2的物质的量为0.05mol
.下列实验操作能达到实验目的的是
A.将饱和FeCl3溶液逐滴加到沸水中继续煮沸至液体呈红褐色,可制备Fe(OH)3胶体
B.电解熔融的氯化铝,可制备铝单质
C.加热使I2升华,可除去铁粉中的I2
D.加入足量氨水,充分振荡、过滤,可除去硫酸铜溶液中的硫酸铝杂质
氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是
A. Q1+Q2 = Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3
H2O和CS2分子中的原子都达到稳定结构。
(1)上述四种元素电负性由大到小的顺序是:___________________。
(2)上述四种元素第一电离能比同周期相邻两种元素都小的元素是:_______。
(3)CS2分子中![]() 键与
键与![]() 键的数目比为:_________。
键的数目比为:_________。
(4)用“大于”、“小于”或“等于”回答本问题:
①CS2在其晶体中的配位数_______H2O在其晶体中的配位数
 ②硫氰酸(H—S—C≡N)的熔点_____异硫氰酸(H—N=C=S)的熔点
②硫氰酸(H—S—C≡N)的熔点_____异硫氰酸(H—N=C=S)的熔点
(5)已知TiCl4熔点为37℃,沸点为136℃,熔融态不导电,可知TiCl4为____晶体。
(6)六方氮化硼(BN)的晶胞结构如右图所示。
![]() ①晶胞内的四个原子(如白球所示)所形成的空间结构为______形
①晶胞内的四个原子(如白球所示)所形成的空间结构为______形
②硼原子的杂化方式为_________。
③晶胞边长为a nm则其密度为____g·cm-3(设阿伏加德罗常数的值为NA)
NA代表阿伏加德罗常数的值。下列叙述正确的是
A.60g丙醇中存在的共价键总数为10NA
B.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C.钠在空气中燃烧可生成多种氧化物。23g钠充分燃烧时转移电子数为1NA
D.235g核互![]() U发生裂变反应:
U发生裂变反应:![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() U+10
U+10![]() n,净产生的中子
n,净产生的中子
(![]() n)数为10NA
n)数为10NA
将标准状况下,将VL A气体(摩尔质量为M g/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度![]() (mol/L)为
(mol/L)为
A![]() .
.![]() B.
B.![]()
C.![]() D.1000VρM(MV+2240)
D.1000VρM(MV+2240)
含有相同氧原子数的二氧化硫和三氧化硫其物质的量之比为 ,质量比为 ,分子数之比为 ,硫原子个数比为 。
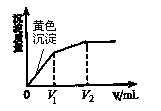 向10 mL含等浓度的I-和Cl-的溶液中逐滴加入0.1 mol·L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。下列说法不正确的是( )
向10 mL含等浓度的I-和Cl-的溶液中逐滴加入0.1 mol·L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。下列说法不正确的是( )
A.该实验可以证明AgI比AgCl更难溶
B.V1= V2-V1
C.向最终的沉淀中加入Na2S溶液,沉淀变成黑色
D.加入V2 mL AgNO3溶液后,溶液中不含I-
- 三个实验小组设计了三种方案粗略测定黄铜(铜锌合金)中锌的质量分数(黄铜已加工成粉末)。 ①供选择的实验装置:②实验
- 《汉书·艺文志》记载“凡诸子百八十九家……蜂出并作,各引一端,崇其所说,以此弛说, 取舍诸候。”其意在说明“百家争鸣”的
- 设、是方程的两个实根。那么“且”是“两根、均大于”的( )A.充分但不必要条件
- 大雨过后,蚯蚓往往要爬到地面上是因为 A.蚯蚓喜欢干燥的环境 B.土中缺氧,无法呼吸 C.到地面寻找食物
- 函数的图象关于直线对称。据此可推测,对任意的非零实数,关于的方程的解集都不可能是( ) A.
- 如右框图,当时,等于____ (A) 7 (B) 8 (C)10 (D)11
- 阅读下面的文字,完成下题。 李小文:特立独行的布鞋院士 这几天,院士李小文颇有些苦恼。被强推到聚光灯下的不自在,源自他
- 下列各式中,正确的是( ) A. B. C. D.
- 《史记》记载:“(秦)民勇于公战,怯于私斗。”《资治通鉴》记载道:“秦被甲百万。山东之士被甲蒙胄以会战,秦人捐(除去)甲
- 韩非子主张建立“事在四方,要在中央,圣人(君主)执要,四方来效”的中央集权政府。韩非子提出这一主张的背景是( )A、
- I'm sorry but what he thinks is not of the _____ importance
- 纪念五四运动90周年大会会场悬挂着横幅:“……团结动员广大青年继承和发扬五四运动光荣传统,为夺取全面建设小康社会新胜利、
- 下列各组词语中,有错别字的一组是 A.宏论 洪亮
- 右图是电子显微镜视野中观察某细胞的一部分,下列有关该细胞叙述中,错误的是 ( ) A、结构1和5中含有DNA
- 17.“眼珠子,鼻孔子,朱子高于孔子;眉先生,胡后生,后生长于先生。”这是一副中国近代比较典型的双关语对联,对于“朱子高
- 在101 kPa时,1 mol甲烷完全燃烧生成二氧化碳和液态水放出890.3 kJ的热量,甲烷的燃烧热为多少?1 000
- 下列句子中加点词语使用恰当的一项是(3分)A.对于张小阳同学这种妨碍他人学习的行为,学校和老师给予了严厉的制裁。B.此次
- .If you ___ it, I will lend the novel to you. A.has read
- 已知数列{an}的前n项和为Sn,且a1=2,a2=8,a3=24,{an+1﹣2an}为等比数列. (1)求证:{}是
- 下列关于ATP的叙述错误的是 A. ATP是细胞中的“能量通货” B.ATP在细胞中易于再生 C.ATP分子含



