高三化学试题
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:![]() 它所对应的化学反应为:__ ___
它所对应的化学反应为:__ ___
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1,2 | 3 |
①T10C时,该反应的平衡常数K=_______
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度_______ (填选项字母)。
A. =0.8 mol·L-1 B. =1.4 mol·L-1 C. <1.4 mol·L-1 D. >1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平衡时各气体的体积分数与甲容器完全相同的是_______(填选项字母)。
A. 0.6 mol、1.0 mol、0.5 mol、1.0 mol
B. 0.6 mol、2.0 mol、0 mol、0 mol
C. 1.0 mol、2.0 mol、1.0 mol、2.0 mol
D. 0.25 mol、0.5 mol、0.75 mol、1.5 mol
(3)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,已知CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
(4)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g) ![]() CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S___0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
下列说法正确的是
A.将密封有NO2的玻璃球浸泡在热水中,气体颜色会变浅
B.向K2CrO4溶液中加入稀硫酸,溶液颜色由橙色变为黄色
C.向盛有0.1mol/LMgCl2溶液的试管中加入NaOH溶液,有白色沉淀生成,再滴入0.1mol/L FeCl3溶液,沉淀最终变为红褐色
D.向盛有Na2CO3溶液中的试管加入酚酞试液,溶液呈红色,再加入足量BaCl2溶液,产生白色沉淀,溶液仍然呈红色
16分某同学欲用已知浓度的NaOH溶液滴定未知浓度的CH3COOH溶液,请填写下列空白:
(1)用洁净的 式滴定管量取待测液10.00 mL,并转移至锥形瓶中。
(2)以下是几种酸碱指示剂变色的pH范围:
①甲基橙3.1~4.4;②石蕊5~8;③酚酞8.2~10,上述指示剂应选择 。
(3)用标准NaOH溶液滴定待测CH3COOH溶液时,左手控制滴定管阀门,右手不停地摇动锥形瓶,两眼注视 。当 时,即达到滴定终点。
(4)下列操作,会使所测CH3COOH溶液浓度偏高的是 。
A.用于量取待测液的滴定管洗涤后未用待测液润洗
B.盛装待测液的锥形瓶洗涤后,残留有蒸馏水
C.滴定时,滴定管尖端处有气泡,滴定完毕排出气泡
D.在滴定过程中,摇动锥形瓶时,因用力过猛,使少量溶液溅出
E.滴定前读数时俯视,滴定完毕读数时仰视
(5)当达滴定终点时,锥形瓶中溶液呈 性(填“酸”“碱”或“中”),其原因是:________(用离子方程式表示)。
(6)在0.1 mol·L-1的CH3COONa溶液中,下列粒子浓度关系式正确的是 。
A.c(Na+)> c(CH3COO-)> c(H+)> c(OH-)
B.c(OH-)=c(H+)+ c(CH3COO-)
C.c(Na+)+c(H+)=c(OH-)+ c(CH3COO-)
D.c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
已知K2O、K2O2、KO2的名称依次是氧化钾、过氧化钾、超氧化钾。那么BaO2的名称是( )
A、氧化钡 B、过氧化钡 C、超氧化钡 D、无法确定
下列实验操作中不正确的是
A.蒸馏时,应将温度计水银球置于蒸馏烧瓶支管口处
B.定容时,如果加水超过了刻度线,则可用胶头滴管吸出多余部分
C.配制稀硫酸时,先在烧杯中加入一定量水,再沿玻璃棒慢慢加入浓硫酸
D.称量NaOH时,NaOH置于小烧杯中放在托盘天平左盘,砝码放在右盘
氢能的存储是氢能应用的主要瓶颈,开发新型储氢材料是氢能利用的重要研究方向,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.
①基态Ti2+中含有的电子数为 ,电子占据的最高能级是 ,该能级具有的原子轨道数为 .
②BH4﹣中的B原子的杂化方式是 .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+ (填“>”“<”或“=”)H﹣.
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如表所示:
| I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
该氢化物的化学式为 .
(3)液氨是富氢物质,是氢能的理想载体.
①NH3的相对分子质量小于PH3,但NH3的沸点却远高于PH3,其原因是 氨 .
②NH3容易和分子中有空轨道的BF3反应形成新的化合物(用“→”表示配位键),该化合物的结构式为 ![]() .
.
(4)2008年,Yoon等人发现Ca与C60(分子结构如图甲)生成的Ca32C60能大量吸附H2分子.


①C60晶体易溶于苯、CS2,C60是 (填“极性”或“非极性”)分子.
②1mol C60分子中,含有σ 键数目为 个.(阿伏加德罗常数数值为NA)
(5)某金属氢化物储氢材料的晶胞结构如图乙所示,该金属氢化物的化学式为 .已知该晶体的密度为a g•cm﹣3,金属元素R的相对原子质量为M,阿伏加德罗常数数值为NA,则该晶胞的体积为 ![]() cm3.
cm3.
次氯酸锂稳定性远髙于次氯酸钠,也可用于杀菌消毒。制备次氯酸钠方法较多,常用的一种合成路线如下:

己知:
1.次氯酸叔丁酯((CH3)3COCl),相对分子质量为108.5,是具有挥发性的黄色油状液体,密度为0.802g/mL,且有强烈刺激性臭味;
2.(CH3)3COCl+LiOH=LiClO+(CH3)3COH
请回答:
(1)实验第一步的反应装置如图所示(夹持装置省略),B装置中支管的作用是 ;浓盐酸逐滴滴加而不是一次性加入的原因是 。

(2)请写出在装置A中发生反应的化学方程式 。
(3)对于操作1,下列说法不正确的是 。
A.可以选用250mL规格的分液漏斗
B.操作1须在通风橱内进行
C.进行分液时,可提早关闭旋塞,以防止次氯酸叔丁酯从下口流出
D.装置B不合适进行操作1
(4)进行操作3时,并不是直接加热蒸发溶液,而畢选择在40°C下缓慢蒸发溶液,试解释其原
因 。
(5)该实验中次氯酸锂的产率为______________ 。
某有机化合物的结构简式为 ,它可以发生的反应类型有
,它可以发生的反应类型有
①取代反应 ②加成反应 ③消去反应 ④酯化反应 ⑤水解反应 ⑥中和反应
A.①③④⑥ B.①②③④⑥ C.②⑤⑥ D.全部
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为
A.NO2 B.N2O2 C.N2O D.N2O4
一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。
| t / min | 0 | 2 | 4 | 6 |
| V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是

A. 0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B. Fe3+的作用是加快过氧化氢的分解速率
C. 反应①是吸热反应、反应②是放热反应
D. 反应2H2O2(aq)![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦
性没食子酸溶液用于吸收少量氧气),下列说法正确的是

A.①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
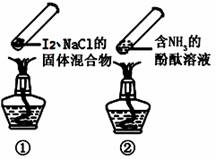
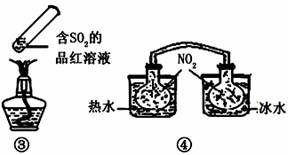
A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差
B.加热时,②、③中的溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅
D.四个“封管实验”中都有可逆反应发生
25℃时,下列各组离子在指定溶液中可能大量共存的是( )
A.碱性溶液中:Na+、Fe3+、Cl﹣、SO42﹣
B.含MnO4﹣的溶液中:H+、K+、Cl﹣、I﹣
C.0.1mol•L﹣1的FeCl2溶液中:H+、Al3+、SO42﹣、NO3﹣
D.由水电离出的c(OH﹣)=1×10﹣14 mol•L﹣1的溶液中:K+、Na+、SO42﹣、CO32﹣
下列离子方程式书写不正确的是( )
A. A1C13 溶液与烧碱溶液反应,当n(OH-) :n(A13+)=7 : 2 时,
2A13++7OH-==A1(OH)3↓+ AlO2-+2H2O
B. 当向饱和Na2CO3溶液中通入过量CO2时,CO32-+CO2 + H2O==2HCO3-
C. CuCl2 溶液与 NaHS 溶液反应,当n(CuCl2):n(NaHS) = l : 2 时,
Cu2++2HS-==CuS↓十H2S↑
D. Fe 与稀硝酸反应,当 n(Fe) : n(HNO3)=l : 2 时,3Fe+2NO3-+8H+==3Fe2+ +2NO↑+4H2O
下列叙述中正确的是
①标准状况下,1 L HCl和1 L H2O的物质的量相同;
②常温常压下,1 g H2和14 g N2的体积相同;
③28 g CO的体积为22.4 L;
④两种物质的物质的量相同,则它们在标准状况下的体积也相同;
⑤在同温同体积时,气体的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比。
A.①③④⑥ B.②⑤⑥
C.⑤⑥ D.①⑤⑥
下列说法正确的是
A. 弱电解质溶液的导电能力一定比强电解质溶![]() 液弱
液弱
B. 将等体积、等浓度的NaOH溶液和氨水各稀释一倍后,两者中和等浓度盐酸的能力氨水强于NaOH溶液
C. 物质的量浓度相同的磷酸钠溶液和磷酸溶液所含PO3-4浓度也相同
D. 如果盐酸中c(H+)是醋酸溶液中c(H+)的2倍,则c (HCl) <2c (CH3COOH)
X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X的氢化物的电子式为_____________。
(2)元素Y的一种中子数为8的同位素可测定文物年代,这种同位素的符号是__________。
(3)元素Z能与氢元素形成+1价阳离子,该阳离子粒子符号是__________。
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为______________。
(5)ZW3常温下呈液态,可与水反应生成一种弱酸和一种弱碱,反应的化学方程式为
________________________________________。
(6)探寻物质的性质差异性是学习的重要方法之一,X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是________________(用酸的化学式表示)。
反应P(g)+Q(g)![]() M(g)+N(s) ΔH<0,达到平衡时,下列说法正确的是
M(g)+N(s) ΔH<0,达到平衡时,下列说法正确的是
A.减小容器体积,平衡不移动 B.加入催化剂,M的产率增大
C.增大c(P),P的转化率增大 D.降低温度,Q的转化率增大
含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是

A. 反应①利用了H2Te的还原性
B. 反应②中H2O作氧化剂
C. 反应③利用了H2O2的氧化性
D. H2Te2O5转化为H2Te4O9发生了氧化还原反应
下列离子方程式书写正确的是 ( )
A.向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑
B.0.1 mol/L NH4Al(SO4)2溶液与0.2 mol/L Ba(OH)2溶液等体积混合:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
D.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O
- ---Have you get used to the weather here? ---Yes. But I
- An ancient philosopher’s wisdom can be compared in value to
- 甲物体的重力是乙物体的3倍,它们从同一地点同一高度处同时自由下落,则下列说法正确的是( ) A.甲比乙先着地 B.甲
- 将金属X置于氯化铝溶液中,Y表面无固体析出;而将其置于硝酸银溶液中,会发生反应:X +2 AgNO3 === X(NO3
- 下列人体细胞中分化程度最低的是( ) A.胚胎干细胞 B.造血干细胞 C.胰腺细胞
- 8.下列有关某生物体各细胞分裂示意图的叙述,正确的是A.图①处于减数第一次分裂的中期,细胞内有2对姐妹染色单体 B.图②
- 设处于平衡状态时相邻分子间的距离是r0,则关于分子力的下列说法中错误的是( )A、分子间距离由r0逐渐减小时,
- 足球守门员在发球时,将一个静止的质量为0.4kg的足球以10m/s的速度踢出,.足球沿草地做直线运动,受到的阻力是足球重
- He arrived in Hollywood in 1964,____some time later,he becam
- 1903年,在美国檀香山的一次集会中,演讲者提出“我们必须倾覆满洲政府,建设民国”。据此推断演讲者是 A.林则徐
- 科学家在研究线粒体组分时,首先将线粒体放在低渗溶液中获得涨破的外膜,经离心后将外膜与线粒体内膜包裹的基质分开。再用超声波
- 如图所示,物块m随转筒一起以角速度ω做匀速圆周运动,以下描述正确的是( )
- —Dick has a bad cough because of smoking. —Why doesn’t he
- 已知,点P(a,b)在反比例函数的图象上,则直线一定不经过的象限为( ) A. 第一象限 B.
- 2013年11月18日,印度尼西亚的两座火山先后爆发,要获取火山爆发的卫星主要应用的地理信息技术是 A、全球定位系统
- 如图所示,“神舟”飞船升空后,进入近地点为 B,远地点为 A 的椭圆轨道 I 上飞行。飞行数圈后变轨.在过远地点 A 的
- 我们所指的文化多样性,主要是指( ) A、历史文化的多样性 B、民族文化的
- 下列除去物质中所含少量杂质的方法正确的是 物 质 所含杂质 除去杂质的方法 A NaCl 泥沙 溶解、过滤、蒸发 B
- 阅读下面一首诗,然后回答问题。(6分) 月 夜 杜甫 今夜鄜州月,闺中之独看。 遥怜小女儿,未解忆长安。 香雾云鬓湿,
- ......



