高一化学下学期下册试题
下列化学用语表示不正确的是
A. 葡萄糖的分子式:C6H12O6 B. H2O的结构式:H-O-H
C. 乙醇的结构简式:CH3CH2OH D. 氯原子的结构示意图:![]()
下图是部分短周期元素的常见化合价与原子序数的关系:
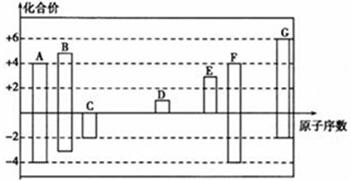
(1)元素A在周期表中的位置。C2﹣、D+、G2﹣离子半径大小顺序是____________(填离子符号)。
(2)用电子式表示D2G2的形成过程________________________。
(3)C、G的氢化物中沸点较低的是____________(填化学式)。
(4)C与D形成的具有强氧化性的化合物的电子式为____________。
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物是生活中一种常用调味品.下列说法正确的是( )
A.简单离子半径:W<X<Z B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y D.最高价氧化物的水化物的酸性:Y>Z
下列说法或表示方法不正确的是( )
A. 盖斯定律实质上是能量守恒定律的体现
B. 在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H = –57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ
C. 由C(石墨)→C(金刚石);△H = +73 kJ/mol,可知石墨比金刚石稳定
D. 在101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H = –285.8kJ/mol
下列物质在一定条件下可与CH4发生化学反应的是( )
A. 氯水 B. 氧气 C. 溴水 D. 酸性KMnO4溶液
氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molCl2中的化学键消耗的能量为Q2 kJ,形成1molHCl中的化学键释放的能量为Q3kJ,下列关系式正确的是( )
A. Q1 + Q2 >Q3 B. Q1+ Q2 > 2Q3 C. Q1 + Q2 < Q3 D. Q1 + Q2 < 2Q3
下表为某有机物与各种试剂的反应现象,则这种有机物是( )
| 试剂 | 钠 | 溴水 | 新制Cu(OH)2悬浊液 | 乙酸 |
| 现象 | 放出气体 | 褪色 |
| 不反应 |
A.CH2=CHCH2OH B.CH2=CHCHO ![]() C.CH2=CHCOOH D.CH3COOH
C.CH2=CHCOOH D.CH3COOH
已知25℃、101kPa时:等质量的Al分别与足量O2和O3完全反应生成Al2O3固体时,放出的热量为akJ·mol-1和bkJ·mol-1,且a<b。下列说法正确的是( )
A.O3比O2稳定,由O2![]() 转化为O3是吸热反应
转化为O3是吸热反应
B.O2比O3稳定,由O2转化为O3是放热反应
C.等质量的O2比O3能量低,由O2转化为O3是吸热反应
D.等质量的O2比O3能量高,由O![]() 2转化为O3是放热反应
2转化为O3是放热反应
NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 1L0.1mol/L的氨水中含有0.1NA个OH-
B. 常温下,在18g D2O中含有NA个氧原子
C. 常温下,7.8 g苯中所含C—H数为0.6NA
D. 标准状况下,11.2L乙烯含有非极性共价键数目为3NA
有一块镁铝合金,其中镁与铝的质量比是8:9。加入足量稀H2SO4使其完全溶解后,再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是
A.  B.
B. 
C.  D.
D. 
对于ⅣA族元素,下列叙述中不正确的是( )
A. SiO2和CO2中Si和O,C和O之间都是共价键
B. C、Si、Ge的最外层电子数都是4,次外层电子数都是8
C. CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应
D. 该族元素的主要化合价是+4和+2
一定条件下反应2AB(g) ![]() A2(g)+B2(g)达到平衡状态的标志是 ( )
A2(g)+B2(g)达到平衡状态的标志是 ( )
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
)如图装置制取溴苯,回答下列问题:

(1)写出A中反应的化学方程式:__________________________________________
(2)C中盛放CCl4的作用是_____________________________________________
(3)D中加入硝酸银溶液,实验后溶液中能看到的的实验现象为
(5)E物质分子式为C8H10,且苯环上的一氯代物只有一种,则E的名称为
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是

A. 1mol N2(g)和1mol O2(g)完全反应放出的能量为180kJ
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量
D. NO是一种红棕色的气体,能与水反应生成硝酸
如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
①X的气态氢化物与Y的最高价氧化物的水化物能发生反应生成盐
 ②Y、Z的气态氢化物水溶液的酸性Y<Z
②Y、Z的气态氢化物水溶液的酸性Y<Z
③Z的单质在常![]() 温下是液体,可与铁粉反应
温下是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.只有①②③④ B.①②③④⑤ C.只有③ D.只有①④
金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2 + bCl2 + cC ![]() aTiCl4 + cCO ……反应I
aTiCl4 + cCO ……反应I
TiCl4 +2Mg ![]() Ti + 2MgCl2 ……反应II
Ti + 2MgCl2 ……反应II
关于反应I、II的分析不正确的是 ( )
① TiCl4在反应I中是还原产物,在反应II中是氧化剂;
② C、Mg在反应中均为还原剂,被还原;
③ 在反应I、II中Mg的还原性大于Ti,C的还原性大于TiCl4;
④ a=1,b=c=2;
⑤ 每生成0.1molTi,反应I、II中共转移0.4mol e-。
A.①②④ B.②③④ C.② D.②⑤
短周期主族元素A、B、C、D、E原子序数依次增大 ,A是元素周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物W分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为_______。W的电子式_________。
(2)在某温度下容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)![]() X(g) DH=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g) DH=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |
|
|
|
①计算该温度下此反应的平衡常数K =_________________。
②三个容器中的反应分别达平衡时下列各组数据关系正确的是___________(填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
(3)熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池,是未来民用发电的理想选择方案之一,其工作原理如图所示。现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出该碳酸盐燃料电池(MCFC)正极的电极反应式____________________________。

下列递变规律不正确的是( )
A. Na、Mg、Al的还原性依次减弱 B. I、Br、Cl的非金属性性依次增强
C. C、N、O 的原子半径依次增大 D. P、S、Cl的最高正化合价依次升高
一定温度下,可逆反应3X(g)+Y(g) ![]() 2Z(g)达到限度的标志是:
2Z(g)达到限度的标志是:
A.单位时间内生成3n mol X,同时消耗n mol Y
B.X的生成速率与Z的生成速率相等
C.X、Y、Z的浓度相等
D.X、Y、Z的分子数之比为3∶1∶2
(1)写出实验室中由固体物质制取氨气的化学方程式 ;
(2)欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为
发生装置![]() (氨气流方向,用小写字母表示)
(氨气流方向,用小写字母表示)

- 白头叶猴和人类的共同祖先是 A.黑猩猩 B.大猩猩 C.长臂猿 D.森林古猿
- (本小题满分12分) 已知椭圆的离心率为,以原点为圆心,椭圆的短半轴长为半径的圆与直线相切. (1)求椭圆的方程; (2
- 假如用化学药物强烈地抑制肿瘤细胞的DNA复制,这些细胞就停留在细胞周期的( ) A.间期
- 某肽链由51个氨基酸组成,如果用肽酶把其分解成1个二肽、2个五肽、3个六肽、3个七肽,则这些短肽的氨基总数的最小值、肽键
- 下列不属于次生演替的是 A.海底火山爆发形成的新岛上逐渐长出了很多植物 B.弃耕后的农田长出杂草,几年后又长出多年生植物
- 如图所示,固定的光滑圆柱体半径R=(m),匀质柔软绳长度L=3m,质量m=0.9kg,搭放在圆柱体上,绳子右端A刚好与圆
- 下图为细胞膜示意图,以下相关说法正确的是A.细胞膜主要由脂质和蛋白质分子构成,为双层膜结构 B.a是细胞膜的基本骨架,其
- 25°C时,某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变
- 要使右图装置中的小气球鼓起来,则使用的固体和液体可以是 ①石灰石和稀盐酸 ②镁和稀硫酸 ③固体氢氧化钠和水 ④生石灰
- 如图所示的电路,电源电压不变,当开关S闭合后,移动滑动变阻器的滑片P,使电压表的示数从6V变化到2V,同时观察到电流表的
- 将4 mol A气体和2mol B气体在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)2C(g
- 如图,在中,,以为直径的交于点,过点作,垂足为点.(1)求证:; (2)判断直线与的位置关系,并说明理由.
- 右图是某个农业生态系统的结构模式图,该图中表示生态系统能量流动的箭头是()A.①③ B.②③⑤ C.①③④ D
- 修改下面的一个病句
- 如图所示,底面积不同的薄壁圆柱形容器内分别盛有液体甲和乙,液面相平。已知甲、乙液体对容器底部压强相等。若分别在两容器中放
- 小球从斜面的顶点,以v0=2 m/s,a=2 m/s2向下匀加速滑行,在到达底端前一秒内所通过的路程是斜面长度的7/15
- 粤菜、鲁菜、湘菜都是我国著名的菜系,其正宗来源地分别是( ) A.四川省、广东省、山东省 B.广
- 氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸;在空气中迅速被氧化成绿色
- 如图12,在□ABCD中,AD=8,点E、F分别是BD、CD的中点,则EF=
- 用长为l的铁丝弯成下部为矩形、上部为半圆形的框架(如图所示),若矩形底边AB长为2x,求此框架围成的面积y与x的函数关系



