高中 化学
 、Cl-、NO
、Cl-、NO  能够大量共存
C . 在由水电离出的c(H+)=10-12mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯
D . 在加入Al能放出大量H2的溶液中:NH
能够大量共存
C . 在由水电离出的c(H+)=10-12mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯
D . 在加入Al能放出大量H2的溶液中:NH  、SO
、SO 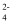 、Cl¯、HCO
、Cl¯、HCO 
|
选项 |
操作 |
现象 |
结论 |
|
A |
测定等浓度的NaCO3和Na2SO3溶液的pH |
前者pH比后者大 |
非金属性:S > C |
|
B |
滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 |
试纸不变蓝 |
不能确定原溶液中 含NH4+ |
|
C |
将HI溶液与CCl4溶液在试管中混合,加入 Fe(NO3)3溶液,振荡,静置 |
下层液体显紫红色 |
氧化性:Fe3+> I2 |
|
D |
将淀粉溶液与少量稀硫酸混合加热,然后加入新制的Cu(OH)2 , 悬浊液,并加热 |
无砖红色沉淀 |
淀粉未发生水解 |
-
(1) 原混合物中PCl3和PCl5的物质的量之比 ;
-
(2) 写出计算过程。
 2K2CO3+6H2O 请填空:
2K2CO3+6H2O 请填空:
-
(1) 放电时:负极的电极反应式为.
-
(2) 通入甲醇一端的电极是极,电池在放电过程中溶液的pH将(填“上升”、“下降”或“不变”).
-
(3) 若在常温、常压下,1g CH3OH燃烧生成CO2和液态水时放出22.68kJ的热量,表示该反应的热化学方程式为.
①取代反应 ②加成反应 ③氧化反应 ④加聚反应 ⑤酯化反应

其中:常温常压下ⅹ是一种有特殊气味、易挥发的无色液体,由三种常见的短周期元素组成。
请回答:
-
(1) 组成X的3种元素是(填元素符号),沉淀C的化学式是。
-
(2) X反应生成A和B的反应方程式是。
-
(3) B可与乙醇以物质的量之比1∶2发生取代反应生成一种酯,写出反应方程式。
-
(4) 实验室保存少量物质X的仪器是_______。A . 无色广口瓶 B . 棕色广口瓶 C . 无色细口瓶 D . 棕色细口瓶
-
(5) 请设计一种不同于上述流程的实验方案,检验中相对原子质量最大的元素。
 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理示意图见图。下列说法正确的是( )
的原理示意图见图。下列说法正确的是( )
 B . 电解时阴极反应式:
B . 电解时阴极反应式: C . 电解过程中,阳极区的
C . 电解过程中,阳极区的 溶液浓度保持不变
D . 电解过程中每转移2mol电子,理论上消耗标况下
溶液浓度保持不变
D . 电解过程中每转移2mol电子,理论上消耗标况下
 的
的 溶液滴定
溶液滴定 的
的 溶液,测得滴定过程中溶液的
溶液,测得滴定过程中溶液的 变化如图所示。下列说法不正确的是( )
变化如图所示。下列说法不正确的是( )
 B . ②点溶液中:
B . ②点溶液中: C . ③点溶液中:
C . ③点溶液中: D . 在相同温度下,①、②、③三点溶液中水电离的
D . 在相同温度下,①、②、③三点溶液中水电离的 :③<②<①
:③<②<①

选项 | 劳动项目 | 化学知识 |
A | 厨房帮厨:炒菜时,时常会添加料酒 | 将乙醇氧化为可调昧的乙酸 |
B | 工厂消毒:向各个办公场所喷洒“84”消毒液 | NaClO具有强氧化性,能使蛋白质变性杀灭病毒 |
C | 社区服务:用泡沫灭火器演练如何灭火 | 铝离子与碳酸氢根离子在溶液中相互促进水解 |
D | 自主探究:锌、铜和柠檬为原料制作水果电池 | 锌能与柠檬中酸性物质发生氧化还原反应 |
城市地下潮湿的土壤中常埋有纵横交错的管道和输电线路,当有电流泄漏并与金属管道形成回路时,就会引起金属管道的腐蚀。原理如图所示,但若电压等条件适宜,钢铁管道也可能减缓腐蚀,此现象被称为“阳极保护”。下列有关说法不正确的是

A.该装置能够将电能转化为化学能
B.管道右端腐蚀比左端快,右端电极反应式为Fe-2e-![]() Fe2+
Fe2+
C.如果没有外加电源,潮湿的土壤中的钢铁管道比较容易发生吸氧腐蚀
D.钢铁“阳极保护”的实质是在阳极金属表面形成一层耐腐蚀的钝化膜
钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC 热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:

已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)·4H2O; ②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:_______________。
(2)用盐酸酸浸时发生反应的离子方程式为:________________________________________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_______________________________________。
②如何证明晶体已洗净?__________________________________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是(用化学方程式解释):______________________________________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:___________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c([Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为____mol/L。
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是( )

A.40 ℃之前,温度升高反应速率加快,变蓝时间变短
B.40 ℃之后溶液变蓝的时间随温度的升高变长
C.图中b、c两点对应的NaHSO3的反应速率相等
D.图中a点对应的NaHSO3的反应速率为5.0×10-5mol·L-1·s-1
下列说法正确的是
A. 焰火的五彩缤纷是某些金属元素化学性质的展现
B. Na2O中阴、阳离子的个数比为1∶1
C. 向氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是a%和b%的两种溶液,则a和b的关系是a<b
下列物质中,在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是( )
A.甲烷 B.乙烯 C.苯 D.乙醇
下列离子检验的方法正确的是( )
A.某溶液![]() 有白色沉淀,说明原溶液中有Cl-
有白色沉淀,说明原溶液中有Cl-
B.某溶液![]() 有白色沉淀,说明原溶液中有SO42-
有白色沉淀,说明原溶液中有SO42-
C.某溶液![]() 有蓝色沉淀,说明原溶液中有Cu2+
有蓝色沉淀,说明原溶液中有Cu2+
D.某溶液![]() 生成无色气体,说明原溶液中有CO32-
生成无色气体,说明原溶液中有CO32-
槟榔碱在医疗上常用于治疗青光眼,其一种合成路线如图:


已知:Ⅰ.不饱和化合物与氨(NH3)或胺(R﹣NH2)反应能生成新的胺类化合物
如:R1﹣CH=CH2+R2﹣NH2![]()
![]() R1﹣CH2﹣CH2﹣NH﹣R2
R1﹣CH2﹣CH2﹣NH﹣R2
Ⅱ.![]()
![]() +R3
+R3![]()
![]()
![]()
![]()

 +R2OH
+R2OH
(1)B中含氧官能团的名称为 .
(2)反应①的反应类型为 ;反应②的反应条件为 .
(3)反应③的化学方程式为  .
.
(4)C的结构简式为  .
.
(5)下列说法正确的是 (填字母).
a.反应④为取代反应
b.槟榔碱与化合物G互为同系物
c.1mol D最多能与2mol NaOH发生反应
(6)已知A在NaOH溶液中水解的产物之一是一种新型功能高分子材料(PAANa)的单体,写出生成PAANa的化学方程式  .
.
(7)已知:CH2=CHCH3+Cl2![]()
![]() CH2=CHCH2Cl+HCl,以丙烯和乙醇为起始原料,选用必要的无机试剂合成A,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
CH2=CHCH2Cl+HCl,以丙烯和乙醇为起始原料,选用必要的无机试剂合成A,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)  .
.
- 如图所示,将一矩形花坛ABCD扩建成一个更大的矩形花园AMPN,要求B在AM上,D在AN上,且对角线MN过C点,|AB|
- 图13是“植被类型与温度、降水量的关系示意图”,图中植被类型分别为草原、苔原、荒漠、阔叶林、针叶林、热带雨林。读图完成下
- 制作年代尺,可以更有效的记忆时间,下面是小明制作的夏、商、周时一条年代尺。其中残缺部分的内容是A.盘庚迁殷 B.牧野之战
- 有人说纸燃烧后,得到的纸灰的质量比纸的质量减少了,这不符合质量守恒定律,这种说法对吗,请根据你所学的化学知识解释其原因。
- 如图,在梯形ABCD中,AD∥BC,AD=6,BC=16,E是BC的中点.点P以每秒1个单位长度的速度从点A出发,沿AD
- 下列说法正确的一项是( ) A、《骆驼祥子》塑造了一位个性鲜明的女性形象——大胆泼辣而有些心理扭曲的小福子。 B、《
- (13分)在水平桌面上沿一条直线放两个完全相同的小物块A和B(可看作质点)质量均为m,它们相距s。B到桌边的距离是2s。
- 下图示生物新物种形成的基本环节,对图示分析正确的是 ( )A.图中A表示基因突变和基因重组,
- 蔗糖不易点燃,如果在蔗糖上撒点香烟灰就很容易点燃燃烧,此时“烟灰”的作用是 A.降低着火点 B.催化
- 在中,角A、B、C的对边分别是、、,且,,则的外接圆直径为( ) A. B.5 C
- Shortly after we ______, a waiter came over to us with a smi
- 164. It is said that the headmistress _____ three months ago
- 下图为“世界铁路大陆桥示意图”,下列关于甲、乙、丙图所示“大陆桥”的说法不正确的有( ) A.“大陆桥”是
- 总书记在中共十七届四中全会上强调,只有抓紧解决党员干部队伍中存在的突出问题,使全党同志始终坚持立党为公、执政为民,始终坚
- —Look ! The piece ofmeat is too large,let’scut __________. A
- The government will ______billions of yuanbuilding a Disneyl
- 下列命题中,m,n表示两条不同的直线,、、表示三个不同的平面. ①若②若,则;③若,则;④若.正确的命题是
- I've won a holiday for two to Florida. I _____my mum. A
- 五边形的内角和是( )A.180° B.360° C.540°
- A、B、C、D 表示四种物质,其微观示意图见下表,A和B在一定条件下反应生成C和D。若64g B参加反应,则生成C的质量



