实验6 酸、碱、盐的化学性质 知识点题库
取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象.
则下列说法中正确的是

A.氨水和盐酸易挥发
B.图示黑点表示石蕊溶液变成了红色
C.氨水与盐酸没有发生化学反应
D.(比较分子运动速率的快慢)

实验操作 | 现象 | 结论 | |
A | 向久置于空气中的NaOH溶液滴加稀H2SO4 | 有气泡产生 | NaOH和H2SO4发生了化学反应 |
B | 向某溶液中滴加BaCl2溶液 | 有白色沉淀 | 原溶液含有SO42﹣ |
C | 向集满CO2的软塑料瓶中加入约 | 塑料瓶变瘪, 溶液变红 | CO2能与石蕊反应 |
D | 将质量相同的Mg、Zn分别投入到足量的稀HCl中 | 镁条表面产生气体更多、更快 | 金属活动性:Mg>Zn |

-
(1) A实验中,碳酸钙和稀盐酸反应的基本类型为,当反应结束时,气球已经完全鼓起,天平指针向右偏,出现该现象的原因可能是.(填字母序号)
a.该反应前后原子数目减少 b.生成气体的反应不遵循质量守恒定律
c.空气的浮力干扰了实验结果 d.该反应生成物的总质量小于反应物的总质量
-
(2) B实验中,试管中装有足量同样的稀盐酸,两个气球中分别装有质量相同的金属A和B(都为+2价),提起气球,加入金属,反应开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束恢复到室温时,甲气球鼓起的比乙气球大,该实验说明:
①金属活动性AB(填“>”或“<”,下同);②相对原子质量AB.
-
(3) C实验,用来验证二氧化碳与氢氧化钠能够发生反应,加入试剂的顺序是
(填字母序号“a.先加入盐酸后加入氢氧化钠溶液”或“b.先加入氢氧化钠溶液后加入盐酸”),整个实验过程中,气球的变化是,请写出二氧化碳与氢氧化钠反应的方程式.
-
(4) D实验中,小气球的作用是,玻璃管中的反应方程式为,
(填“能”或“不能”)根据通入的CO的质量计算生成的铁的质量.


-
(1) 写出上图D装置中甲仪器的名称;
-
(2) 用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为,收集较纯净的氧气可选择(填装制编号);
-
(3) 实验室制取二氧化碳通常选择下列药品中的(填药品序号);
a、稀盐酸 b、熟石灰 c、块状石灰石 d、稀硫酸
-
(4) 常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是(填装置编号,下同).实验室制取氢气应该选择的发生和收集装置组合可以是;
-
(5) 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质.

①为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变;
②图中A所表示的物质类别是;
③镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量有(填序号).
A、两种金属的颗粒大小 B、盐酸的浓度 C、温度.
A.酚酞试液 B.石蕊试液
C.稀盐酸 D.
①C→CO→CO2
②Al→Al2O3→AlCl3
③Na2CO3→NaCl→NaNO3
④CaCO3→CaO→Ca(OH)2
-
(1) 下列含碳元素的物质中,属于有机物的是___(填字母序号).A . 碳酸钙 B . 乙醇(C2H5OH) C . 二氧化碳
-
(2) 近期,浙江大学实验室里诞生了世界上最轻的材料﹣﹣“碳海绵”.(如图甲所示),由碳元素组成,具有多孔结构,弹性好.它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状.下列关于碳海绵的说法正确的是___(填字母序号).A . 具有吸附性 B . 可重复利用 C . 可处理海上石油泄漏
-
(3) 如图乙,二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环.
图甲
 图乙
图乙 
图丙

①步骤1的化学方程式为.
②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量溶液,若观察到试管内.则分解不完全.
③上述设想的优点有(填字母序号).
a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用
④CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为,若要检验1%甲酸水溶液是否显酸性,能选用的有(填字母序号).
a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸
-
(4) 如图丙,在A瓶中盛满CO2气体,将装有96℃以上但未沸腾热水的B瓶,放入装有相同热水的烧杯中,进行如下实验:
①先用注射器抽取20mL的水,注入A瓶中,充分振荡,其化学方程式为,但未见B瓶中发生现象.
②再用另一只注射器抽取20mL的浓NaOH,注入A瓶中,充分振荡,观察到的现象为,产生此现象的原因是.

-
(1) 填写图1空白处,以完善知识网络图;
-
(2) 为了验证反应①,小明将无色酚酞试液滴入KOH溶液中,溶液变成色;
-
(3) NaOH必须密封保存,同理KOH固体也必须密封保存,否则在空气中要变质。写出KOH在空气中变质的化学方程式 ;
-
(4) 小明用微观示意图(图2)来说明反应③的发生,该反应属于中和反应,其实质是 。在图2所示的反应过程中,小明对反应溶液的pH进行了三次测定,当溶液pH=10时,溶液中溶质为(填化学式,下同);pH=7时,溶质为;pH=3时,溶质为 ;
-
(5) 写出符合④反应的化学方程式。
[提出问题一]为什么有的小组会出现白色不溶物?
-
(1) [实验探究一]在4支试管中分别加入相同质量、相同溶质质量分数的稀盐酸,形状大小相同、用砂纸打磨过的镁条,实验记录如表:
镁条的长度/cm
1
2
3
4
不溶物
无
少量
较多
很多
[实验结论]通过上表可知,出现白色不溶物与有关,由此你对化学反应有什么新的认识。
-
(2) [提出问题]白色不溶物是什么?
[查阅资料]①AgNO3与可溶性氯化物反应,生成不溶于水,也不与稀硝酸反应的白色沉淀。②Mg(OH)2和Mg(OH)Cl均为白色固体,不溶于水但能与稀盐酸、稀硫酸等反应生成盐和水。
[提出猜想]
猜想l:是没有参加反应的镁条;
猜想2:是生成的MgCl2过多而析出晶体
猜想3:是生成的Mg(OH)2白色沉淀;
猜想4:是生成的Mg(OH)Cl白色沉淀。
[实验探究]
将上述试管反应后的物质过滤,并将得到的白色不溶物分成三份,分别放入三支试管中进行实验。
实验序号
实验操作
实验现象
实验结论
实验1
滴加适量稀盐酸。
。
猜想1不成立
实验2
加入适量蒸馏水,充分振荡
白色不溶物没有减少
猜想2不成立
实验3
①滴入足量的稀硝酸
②再向①中继续滴入足量的硝酸银溶液
。
白色不溶物一定含有氯元素,说明猜想3不成立,猜想4成立
-
(3) [实验反思]
①甲同学对上述实验3的结论提出质疑,他认为实验3设计不严密,要验证猜想4是否成立,在进行实验3之前应该进行的操作是。
②在老师的指导下,实验小组最终确定白色不溶物是Mg(OH)Cl,请写出Mg(OH)Cl与稀盐酸反应的化学方程式。

-
(1) A点所表示的物质为N2 , 则横坐标上X对应物质类别为,工业上可用方法获得N2。
-
(2) B点表示的物质化学式为。
-
(3) E点表示的物质稀溶液能使紫色石蕊试液变红,是因为溶液中含有。
-
(4) 某化合物的化学式为AgNO3 , 代表它的点是。AgNO3见光会分解生成银、氧气和C点代表的物质,写出反应的化学方程式。
- (10·全国ⅠA篇)OPENING TIMES: 20 Mar to 19 Oct Mon to Sat: 9:00a
- Can you help ,please? A. me
- 小阅读语段训练:阅读下面语段,选出符合要求的一项地球上生命的历史也就是生物与它们的环境相互作用的历史。动植物的形体和习性
- 单词拼写1. The vegetable market isalways ___________ (拥挤) in the
- (1)如图1,△ABC内接于⊙O,AB为直径,∠CAE=∠B,试说明AE与⊙O相切于点A; (2)在图2中,若AB为非直
- 红细胞中Fe2+含量降低时,红细胞运输氧的能力相应减弱,这个事实说明Fe2+的作用是( ) A、调节血液的酸碱平
- 下列各组词语中加点的字是多音字,其中读音全都不相同的一组是( ) A.号角/名角 铁椎/脊椎骨
- (8分)全国著名发明家邹德俊发明了一种“吸盘式”挂衣钩,如图所示,将它紧压在平整、清洁的竖直瓷砖墙面上时,可挂上衣帽等物
- 图11所示的三个实验中,可以说明分子之间有相互作用力的是______图。 图10
- “一杯鲜豆浆,天天保健康。”豆浆营养丰富,味美可口,素有“绿色牛乳”之称。豆浆中的养料主要储存在大豆种子的
- 如图,⊙A、⊙B、⊙C两两不相交,且半径都是2cm,图中的三个扇形(即三个阴影部分)的面积之和是多少?弧长的和为多少?
- Hecame to my house and required that I ________ him. A.help
- 如图所示烧杯中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是( ) A.(4) (3)(2) (1)
- 禹死后,__________继承父位,从而__________制代替了禅让制。
- 19.依次填入下面一段文字横线处的语句,衔接最恰当的一句是( ) “社会情绪能力”是继“情商”之后,目前国际上脑研究
- 下列加点字的注音完全正确的一项是() A.濒临bīn 拖曳yè 媲美pì 稼穑qiáng B.吊唁yà
- 设0≤x≤2,y=4x--3·2x+5,试求该函数的最值.
- 阅读下面短文,回答文后题目。《闻一多先生的说和做》(16分)闻一多先生还有另外一个方面,——作为革命家的方面。这个方面,
- 阅读材料,解决问题:材料1:在研究数的整除时发现:能被5、25、125、625整除的数的特征是:分别看这个数的末一位、末
- 编写一个程序,输入正方形的边长,输出它的对角线长和面积的值。
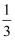 体积滴有石蕊试液的水,旋紧瓶盖,振荡
体积滴有石蕊试液的水,旋紧瓶盖,振荡


