初中 化学
 、
、 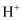 、
、  、
、  B .
B .  、
、 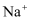 、
、  、
、  C .
C .  、
、  、
、  、
、  D .
D . 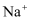 、
、 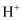 、
、  、
、 
选项 | 物质(括号内为杂质) | 除杂方法 |
A | CaO (CaCO3) | 高温煅烧 |
B | NaCl溶液(Na2CO3) | 加入适量的稀盐酸 |
C | CaCl2溶液(HCl) | 加入过量的CaCO3 , 再过滤 |
D | CO2(HCl) | 先通过足量NaOH溶液,再通过浓硫酸 |
-
(1) 保持水的化学性质的最小粒子是;
-
(2) 四个氢氧根离子
-
(3) 2个氯离子;
-
(4) 三个二氧化硫分子;
-
(5) 地壳中含量最多的非金属元素和金属元素形成的化合物
-
(6) 三氧化二铁中铁元素显+3价.
课外小组同学将100g盐酸分5次加入到35g某石灰石样品中(已知杂质不与盐酸反应),得到如下部分数据和图象。(最后结果保留一位小数)
| 次数 | 1 | 2 | 3 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
计算:
(1)表中“a”的数值是 g
(2)该石灰石样品可制取二氧化碳的质量。
(3)稀盐酸中溶质的质量分数。
 用纸槽将固体粉末送入试管
B .
用纸槽将固体粉末送入试管
B .  倾倒液体
C .
倾倒液体
C .  加热试管内液体
D .
加热试管内液体
D .  熄灭酒精灯
熄灭酒精灯
 B . 丝绸
B . 丝绸  C . 茶叶
C . 茶叶  D . 中草药
D . 中草药 
-
(1) 该转化过程属于(填“物理”或“化学”)变化;其催化剂是两种(填“金属”或“非金属”)。
-
(2) 在能源领域中,一氧化碳是液态氢的一种重要的补充能源,液态氢是一种(填“化石能源”或“清洁能源”)。它们都能燃烧,反应的化学方程式分别为:。
-
(3) 为减少温室气体的排放,人们应尽量减少的燃烧,使用无污染的清洁能源,如。
-
(4) 甲醇(CH3OH)也可用作赛车燃料,其燃烧产物与酒精燃烧的产物相同。则其反应的化学方程式为:。
-
(5) 在干旱的地方,人们经常利用二氧化碳的固体来做。(填一种)
|
反应时间t∕s |
t0 |
t1 |
t2 |
t3 |
t4 |
t5 |
t6 |
|
反应后固体的质量m∕g |
80 |
75 |
70 |
66 |
62 |
58 |
58 |
请回答下列问题:
-
(1) 当石灰石完全反应后,生成CO2的质量为g。
-
(2) 求该石灰石中CaCO3的质量分数,写出计算过程

 向氢氧化钠溶液中加水稀释
B .
向氢氧化钠溶液中加水稀释
B .  表示向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液至过量
C .
表示向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液至过量
C .  电解水生成氢气和氧气的质量与反应时间的关系
D .
电解水生成氢气和氧气的质量与反应时间的关系
D .  向等质量的 Zn、Fe 中滴加等浓度等质量的稀盐酸
向等质量的 Zn、Fe 中滴加等浓度等质量的稀盐酸

-
(1) 你认为设计该实验是为了测定;
-
(2) 实验过程中,下列操作正确的顺序是(填序号)
①检查装置的气密性②实验前夹紧止水夹③冷却后再打开止水夹
-
(3) 通电后使红磷燃烧,燃烧的现象是;
该反应的文字表达式是;
-
(4) 红磷燃烧了一段时间后,自动熄灭了,原因可能是;
-
(5) 出该实验你得到的结论是;
-
(6) 用通电的方法引燃红磷与用酒精灯引燃红磷相比,优点是.(写一条即可)
-
(1) 实验一:如图是甲同学进行粗盐提纯实验的操作示意图。

操作⑤中有一处明显的不正确,请你帮他们指出来。图中不正确改正后,粗盐提纯实验的正确操作顺序为(填操作示意图的序号)。
-
(2) 实验二:某兴趣小组查阅资料发现除去泥沙等杂质的粗盐,可能还含有 CaCl2、MgCl2、Na2SO4等杂质。他们将实验一所得氯化钠溶液杂质成分进行探究和除杂。
【阅读思考】若实验一所得氯化钠溶液中含有 CaCl2、MgCl2、Na2SO4等杂质,则该溶液中氯化钠的质量分数(填“>”、“<”或“=”)5%。
-
(3) 【实验探究】小组同学设计了如下实验探究该氯化钠溶液杂质成分并除杂。
实验步骤
实验现象
分析结论
Ⅰ取适量该氯化钠溶液于试管中,加入过量的NaOH溶液。
有白色沉淀产生。
该氯化钠溶液中含有MgCl2杂质。该反应的化学方程式为
Ⅱ、向步骤I的试管中继续滴加过量Na2CO3溶液,充分反应后过滤。
该氯化钠溶液中含有CaCl2杂质。
Ⅲ、向步骤Ⅱ所得滤液中滴加过量BaCl2溶液,充分反应后过滤。
有白色沉淀产生。
该氯化钠溶液中含有Na2SO4杂质。
VⅠ。向步骤Ⅲ所得滤液中滴加稀HCl至溶液呈中性。
无明显现象。
加稀盐酸除去的物质是
-
(4) 【反思交流】
①小组同学认为 Na2SO4 还不能确定是否存在,原因是;可向步骤 III 的沉淀中滴加过量的,若观察到沉淀部分溶解,证明粗盐中确实存在 Na2SO4。
②小红认为杂质也未完全除去,可对调四个步骤中的两种试剂的位置就能达到完全除杂目的,这两种试剂为(填序号)。
A.NaOH 溶液、Na2CO3溶液 B.Na2CO3溶液、BaCl2溶液 C.BaCl2溶液、稀盐酸
根据下图回答问题:

(1)写出仪器①的名称:_________________。
(2)实验室若用装置A制取较纯净的氧气,反应的化学方程式为______________,可以选______________(填装置序号)作收集装置。
(3)实验室制取CO2,应选择的发生和收集装置的组合是_____________(填装置序号)。在装入药品前,必须要进行的实验操作是______________。
如图表示氯酸钾和二氧化锰混合加热制氧气,从起始至完全反应的过程中固体质量随时间的变化情况,请计算:

(1)制得的氧气质量是________克;
(2)混合物中氯酸钾的质量分数是多少_______?
健康的身体离不开合理的饮食,下列说法正确的是
A.多吃富含维生素的蔬菜水果 B.用甲醛溶液浸泡鱼虾防腐
C.用霉变的花生做食品 D.食盐中加碘,碘元素的摄入越多越好
生活中的下列做法,你认为不合理的是
A.木柴燃烧时,把木柴架空 B. 油锅着火时,用水灭火
C.用铅笔芯粉末打开生锈的锁头 D.用过的菜刀涂食用油防锈:
- 8gNa2O2、Na2O、Na2CO3、NaOH的混合物与200g质量分数3.65%的盐酸恰好反应,蒸干溶液,最终所得固
- 实验室用加热高锰酸钾法制氧气,若要制得3.2g氧气,计算参加反应的高锰酸钾的质量。
- 生活中处处是化学,我们可以用化学的视角去解决、解释生活中的某些问题。下列说法中正确的是 A.生活污水中富含氮、磷的
- 植物组织培养依据的原理、培养过程的顺序及诱导的植物激素分别是 ①体细胞全能性 ②离体植物器官、组织或细胞 ③根、芽④
- 关于松嫩平原与其他区域关系的叙述,正确的是( )①.松嫩平原属于三江平原
- ÷=________.
- — May I remind you that a Mr Li is waiting outside, sir???—
- (1)《中华人民共和国国歌》的词作者是 ,曲作者是聂耳。 (2)吾尝终日而思矣,
- Ifyou want to take an adventure travel lasting a day or two,
- 下列措施不能够防止发酵液被污染的是( ) A.榨汁机要清洗干净,并晾干 B.发酵瓶要清洗干净,用体积分数为70%的
- 阅读下面短文,从每题所给的四个选项中,选出最佳答案。 Hi, dear boys and girls! Do you k
- 1.下列加点字的注音没有错误的一组是( )(3分)A.迤逦(yǐ) 稽手(qǐ) 芙蓉浦(pǔ)
- 下图模拟的是呼吸时膈肌的运动情况,请根据图回答下列问题:(每空2分,本题共12分)(1)图中气球代表的是肺,瓶底的橡皮膜
- 已知a1=1,an+1-an=2n-n. (1)求a2,a3; (2)求证:an=
- 用氧化物X测定空气受CO的污染的程度,发生化学反应的方程式为:X+5CO=I2+5CO2 根据CO2的多少,可测定CO的
- 要得到函数的图象,只需将函数的图象 A.右移个单位 B.右移个单位 C.左移个单位 D
- 下列加点字注音有误的一项是( )A.长袍(páo)菜肴(yáo)几碟(dié)扉(fēi)页B.停滞(zì) 扼(è)
- 北宋兴起的景德镇后来发展成为著名的瓷都。( )
- 象征意象就是代表某一实体事物或某种精神内容的意象。出现在诗歌中的只是象征体,而被象征的本体则隐去了,这样就使得诗歌更耐人
- (23分)“创新是一个民族的灵魂。”中国作为一个历史悠久的多民族国家,在政治制度创新方面多有建树,而且其体系之完备,经验



